Ильин А.П., Гордина Н.Е. Химия твердого тела
Подождите немного. Документ загружается.

91
Пространственная группа Fm3m. Каждый ион натрия окружен шестью иона-
ми хлора, а каждый ион хлора – шестью ионами натрия. Поэтому говорят:
координационное число натрия по хлору равно координационному числу
хлора по натрию и равно 6.
Каждый ион натрия (хлора) окружен шестью ионами хлора (натрия),
расположенными по вершинам октаэдра. Координационный многогранник –
октаэдр (рис. 2.23). Такую же структуру имеют другие галогениды щелочных
металлов, кроме галогенидов цезия (табл.2.6).
Таблица 2.6
Параметры решетки (в Å) щелочноземельных металлов со структурой
типа NaCl
Br Cl F I
Ag
K
Li
Na
Rb
5.77
6.60
5.50
5.97
6.85
5.55
6.29
5.13
5.64
6.58
4.92
5.35
4.03
4.62
5.64
*
7.07
6.00
6.47
7.34
Структурный тип сфалерита. Сульфид цинка кристаллизуется в виде
кубического сфалерита (цинковой обманки) или гексагонального вюрцита.
Такие же структуры характерны для многих полупроводниковых кристаллов.
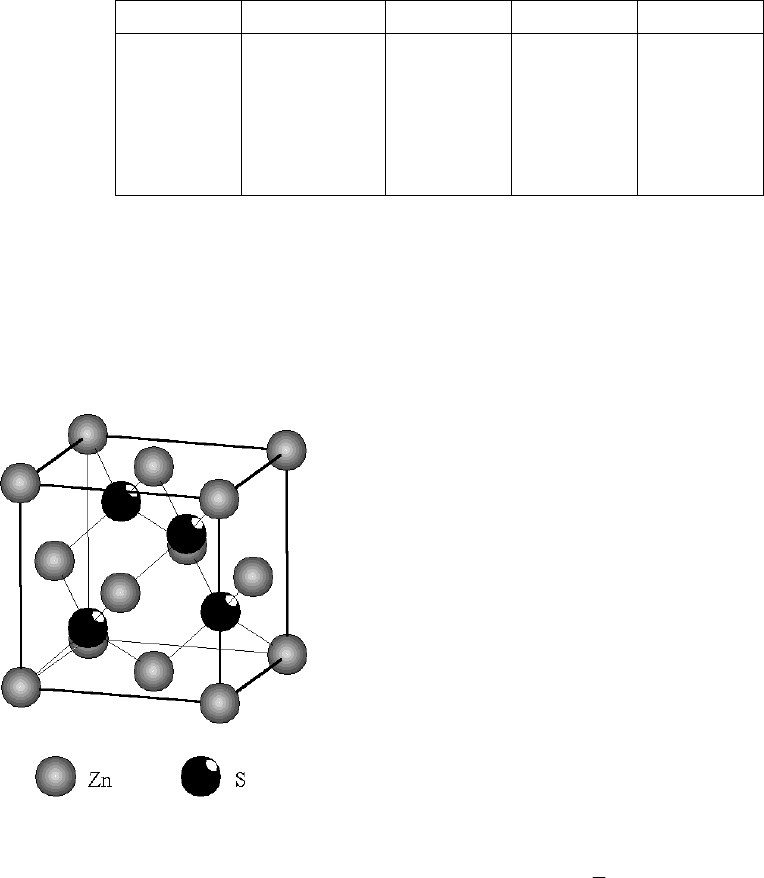
Рис. 2.24. Кристаллическая решетка сфа-
лерита. Элементарная ячейка.
В сфалерите (рис. 2.24) каждый ион
цинка тетраэдрически окружен ионами серы, а
каждый ион серы – ионами цинка, располо-
женными также по вершинам тетраэдра. Эта
структура рассматривается как плотнейшая
упаковка серы, в которой ионы цинка занимают половину тетраэдрических
пустот. Решетка сфалерита принадлежит к виду F
4
3m. Структура решетки
92
сфалерита сходна со структурой алмаза. Это станет возможным, если в ре-
шетке алмаза все узлы гранецентрированной ячейки занять атомами цинка и
в центры четырех из восьми октантов поместить атомы цинка. Структуру
сфалерита можно описать как две гранецентрированные решетки серы и
цинка, смещенные друг относительно друга на четверть телесной диагонали
кубической ячейки. Ионы цинка и серы находятся во взаимозаменяемых по-
ложениях. Координационное число цинка по сере равно координационному
числу серы по цинку и равно четырем. Координационный многогранник –
тетраэдр (КЧ
Zn
= КЧ
S
=4; КМ –тетраэдры).
В свою очередь, координационное число цинка равно координацион-
ному числу серы по сере и равно двенадцати. Это служит характерным при-
знаком плотнейшей упаковки.
Структурный тип рутила – TiO
2.
К этому структурному типу относят-
ся SnO
2
, MnO
2
, PbO
2
, CoF
2
, MnF
2
, ZnF
2
и др. Атомы кислорода образуют
плотнейшую гексагональную упаковку, в которой 1/2 октаэдрических пустот
занято атомами титана.
КЧ
Ti
=6; КЧ
O
=3.
Структурный тип флюорита CaF
2.
В структурном типе флюорита
кристаллизуются соединения элементов двухвалентных катионов с однова-
лентными анионами (SrF
2
, BaF
2
и др.), а также соединения одновалентных
катионов и двухвалентными анионами Li
2
O, Na
2
S, K
2
O и др. Элементарная
ячейка флюорита кубическая F – гранецентрированная (рис.2.25). Ионы Ca
2+
занимают узлы гранецентрированной ячейки и образуют плотнейшую куби-
ческую упаковку, ионы F
-
занимают центры 8 октантов. Каждый атом каль-
ция окружен восьмью атомами фтора. Координационное число кальция
относительно фтора равно 8 (координационный многогранник – гексаэдр),
координационное число фтора относительно кальция равно 4
(координационный многогранник – тетраэдр). Решетку образуют два сорта
атомов.
93
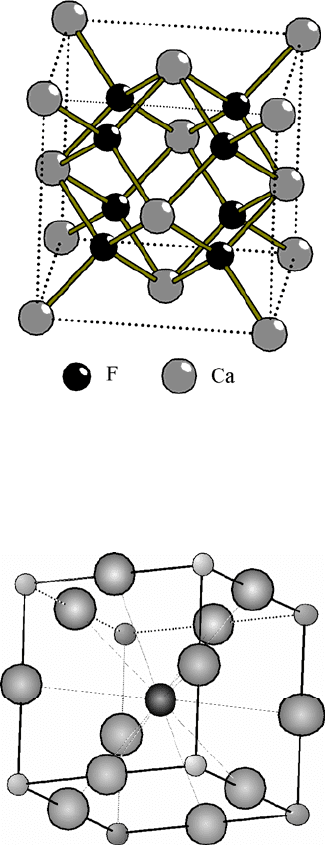
Рис. 2.25. Кристаллическая решетка флюо-
рита CaF
2
. Элементарная ячейка.
На одну элементарную ячейку приходится
4 атома (иона) типа А и 8 атомов (ионов) типа В.
Следовательно, для соединения типа АВ
2
(CaF
2
)
число структурных единиц будет n = 4
(4Ca
2+
+8F
2-
= CaF
2
).
Структурный тип перовскита. В структурном типе перовскита кри-
сталлизуются соединения BaTiO
3
, FeTiO
3
, CaZrO
3
, PbTiO
3
и др.
В элементарной ячейке перовскита ионы
титана занимают вершины куба, ионы кислорода
помещены в середины ребер, а ион кальция -
внутри ячейки (рис. 2.26).
Рис. 2.26. Элементарная ячейка перовскита
CaTiO
3.
Несмотря на то, что в центре ячейки имеется ион, решетка не объемно-
центрированная, а примитивная. Для объемно-центрированной решетки не-
обходимо, чтобы ионы или атомы, находящиеся в вершинах куба и центре,
были одного (цвета) сорта. В решетке же перовскита в вершинах куба ионы
титана, а в центре ион кальция. Таким образом, решетка Бравэ перовскита
относится к типу Р, а пространственная группа Pm3m.
Ион кальция принадлежит ячейке целиком. Ионы титана, находящиеся
в вершинах куба, принадлежат ячейке каждый на 1/8 часть и дают общий
вклад 8·1/8=1. Ионы кислорода, расположенные на ребрах ячейки, принадле-
жат ей на 1/4. Ребер в кубе 12, следовательно, ионы кислорода вносят вклад в
ячейку: 12·1/4=3 иона. Стехиометрическое отношение: Ca:Ti:C=1:1:3, т.е. оп-
94
ределенное нами число ионов Ca, Ti, O образует CaTiO
3
– одну структурную
единицу, n =1.
Определение координационных чисел и координационных многогран-
ников в структуре CaTiO
3
сложнее, чем в структурах типа АХ и АХ
2
. Наибо-
лее отчетливо можно наблюдать окружение катиона кальция кислородом.
Координационное число кальция по кислороду 12, координационный много-
гранник – кубооктаэдр. Ионы титана находятся в окружении 6 ионов кисло-
рода. Координационное число титана по кислороду 6, а координационный
многогранник – октаэдр. Можно выделить и другие координационные окру-
жения. Так, наиболее близко к кальцию находятся восемь ионов титана.
Структура шпинели. Структура шпинели, структурный тип MgAl
2
O
4
,
характерна для соединений типа Ме
2+
Ме
3+
О
4
2-
, где Ме
2+
и Ме
3+
двух и трех-
валентный металл, из которых хотя бы один принадлежит к группе переход-
ных элементов, О
2-
– кислород.
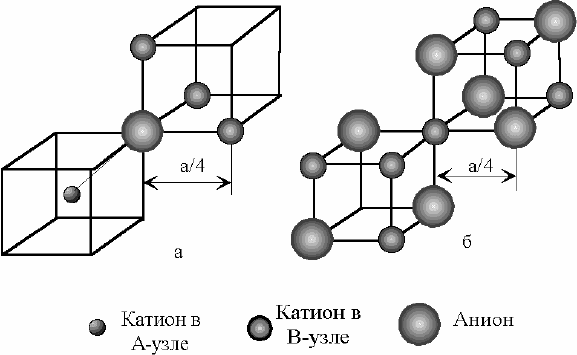
Рис. 2.27. Фрагмент
ближайшего окружения
аниона (а) и катиона в В-
узле (б) в структуре шпине-
ли
В структурном типе
шпинели кристаллизуется
большая группа химических
соединений. MgAl
2
O
4
- благородная шпинель, является классическим приме-
ром широко распространенной кристаллохимической ячейки. В так называе-
мых нормальных шпинелях катионы двухвалентного металла представляют
Mg
2+
, Mn
2+
, Fe
2+
, Ni
2+
, Zn
2+
. Катионы трехвалентного металла: Al
3+
, U
3+
, Cr
3+
,
Fe
3+
, Mn
3+
. Известны химические соединения со структурой шпинели, в ко-
торых вместо кислорода анионом являются F
-
, Cl
-
, CN
-
, S
2-
, Se
2-
, Te
2-
.
Пространственная группа для структуры шпинели Fm3m. Разбирать
строение шпинели по чертежу довольно трудно (рис. 2.27). Поэтому вместе с
95
плоскостным изображением элементарной ячейки шпинели необходимо
иметь и ее модель (2.28). Элементарная ячейка шпинели состоит из 8 катио-
нов Ме
2+
, 16 катионов Ме
3+
и 32 анионов О
2-
. Ме
2+
: Ме
3+
: О
2-
=8:16:32. Так как
формула шпинели MgAl
2
O
4
, элементарную ячейку образуют 8 структурных
единиц, n =8. Катионы Mg
2+
образуют гранецентрированную ячейку Бравэ.
Они находятся в тетраэдрическом окружении анионов кислорода. Координа-
ционное число магния по кислороду равно 4, координационный многогран-
ник – тетраэдр. Катионы Al
3+
окружены шестью анионами кислорода. Коор-
динационное число алюминия по кислороду равно шести, координационный
многогранник – октаэдр.
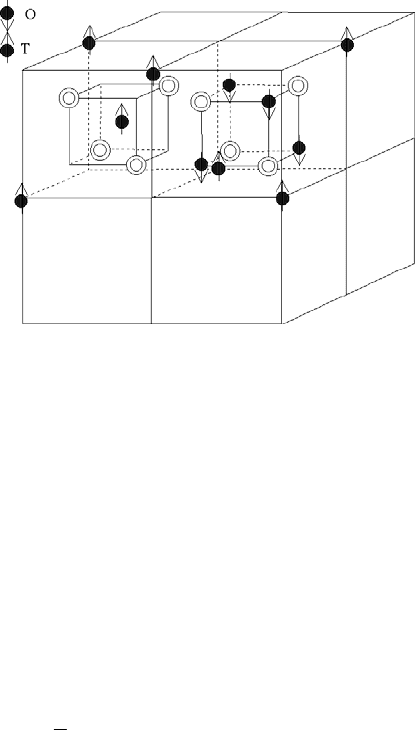
Рис. 2.28. Два смежных октанта в
структуре шпинели. Двойные кружки –
ионы кислорода, О – октаэдрические,
Т– тетраэдрические междоузлия
В свою очередь, анионы кислоро-
да образуют плотнейшую кубическую
упаковку, где каждый ион кислорода окружен двенадцатью ему подобными.
На модели определяются и другие координационные числа.
Структура корунда. Структуру корунда
α
-Al
2
O
3
можно описать как
ромбоэдрически деформированную структуру NaCl, в которой ион Na или
ион Cl заменен группой Al
2
O
3
(рис. 2.29).
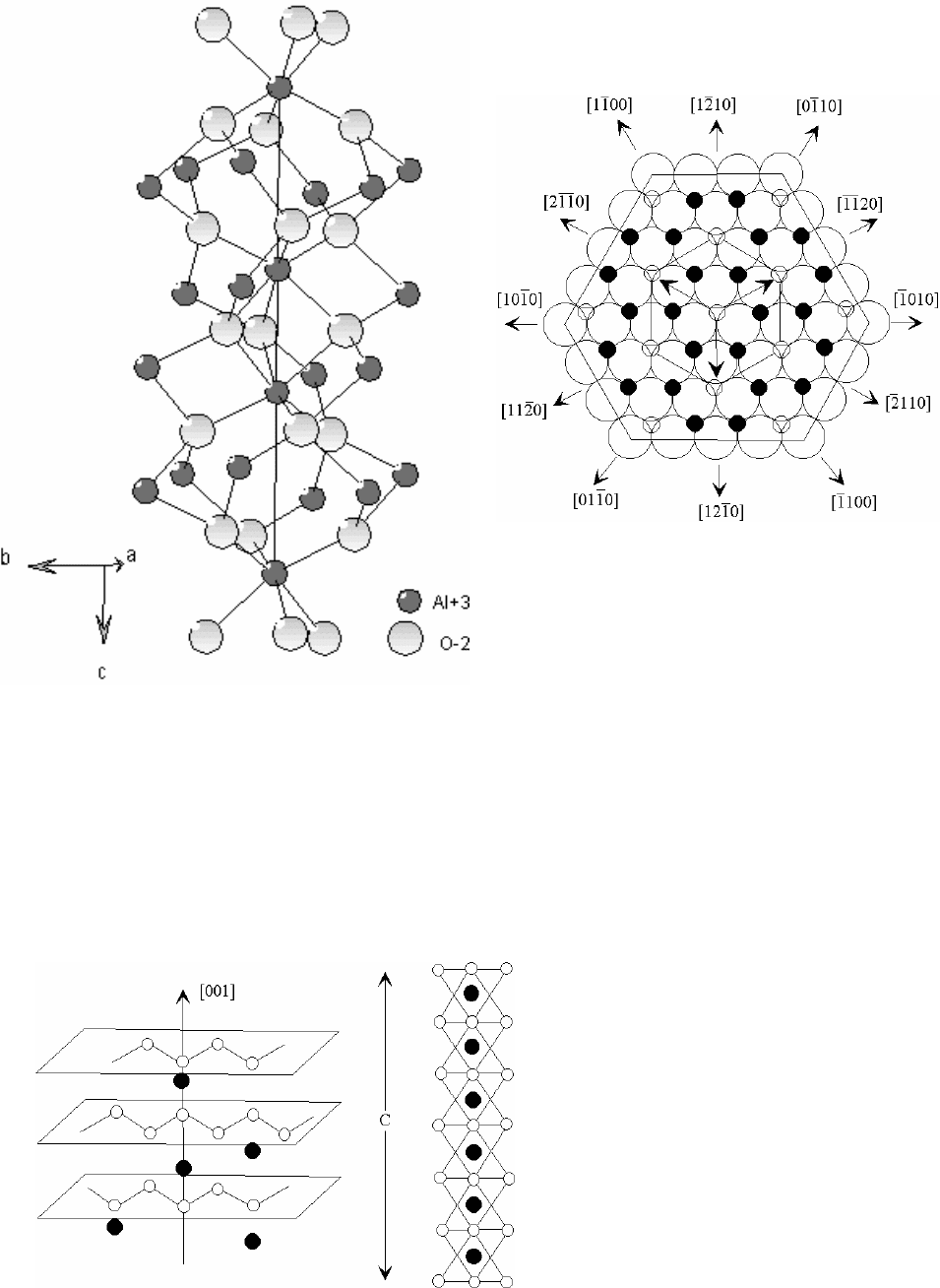
Двухвалентные ионы кислорода образуют приблизительно гексаго-
нальную плотнейшую упаковку ...АВАВАВ..., а трехвалентные ионы алюми-
ния заполняют две трети октаэдрических пустот, лежащих в направлениях
<
101
0
> (рис 2.30).
Группы из трех ионов кислорода образуют общую плоскость из двух
смежных октаэдров, связанных с одной и той же парой ионов алюминия. Па-
ры заселенных октаэдров, чередуясь с одним незаселенным, создают винто-
96
вые оси 3
1
, характеризующие так называемый корундовый мотив упаковки
вдоль оси с.
Рис. 2.29. Схема элементарной
ячейки структуры корунда
Рис. 2.30. Расположение ионов
в плоскости базиса (0001) в струк-
туре корунда. Черные кружки – ио-
ны алюминия, светлые кружки –
ионы кислорода (малые – в плоскости чертежа, большие – под плоскостью
чертежа)
Расположение структурных единиц вдоль оси с повторяется через 6
слоев ионов кислорода с шестью промежуточными слоями ионов алюминия
(рис. 2.31).
Рис. 2.31. Чередование
слоев кислорода и алюминия
вдоль главной оси симметрии
(слева) и схема расположения
слоев (справа) в структуре ко-
рунда (с – высота элементарной
ячейки)

97
Корунд кристаллизуется в классе
3
m
тригональной сингонии, про-
странственная группа
R
c
3
.
Чистые кристаллы корунда прозрачны и бесцветны. Примеси, которые
легко входят в структуру, окрашивают корунд в разные цвета: примесь хро-
ма– в красный (рубин), титана – в синий (сапфир), кобальта, урана – в зеле-
ный, железа, никеля, урана, титана – в желтый.
Рубин – кристалл корунда, в котором часть ионов алюминия изоморф-
но замещена трехвалентными ионами хрома. Содержание Cr
2
O
3
от 0,05 до 0,5
% придает рубину цвет от бледно-розового до темно-красного, а при даль-
нейшем увеличении концентрации хрома (выше 8 %) цвет кристалла стано-
вится зеленым, что обусловлено возникновением связей между атомами хро-
ма (чистый Cr
2
O
3
имеет зеленый цвет). Радиус ионов хрома (0,65Å) больше
радиуса ионов алюминия (0,57 Å), поэтому при изоморфном замещении алю-
миния трехвалентным хромом параметры решетки а и с корунда увеличива-
ются, и хотя каждый ион хрома окружен шестью ионами кислорода, т.е. на-
ходится в октаэдрической координации, но он оказывается не в центре окта-
эдра ионов кислорода, а несколько смещен вдоль оси с. Из-за этого в струк-
туре возникают напряжения, растущие по мере увеличения концентрации
хрома.
Плотнейшие упаковки могут быть трех типов:
1) анионные;
2) катионные CaF
2
, Сa
5
F(PO
4
)
3
;
3) смешанные катионно-анионные CaTiO
3
.
Существуют два способа подсчета координационных чисел:
1) упрощенный (формальный) подсчет без учета плотнейших упаковок;
2) подсчет с учетом плотнейшей упаковки.
2.8. Типы химической связи в кристаллах
На первый взгляд такие характеристики твердых тел, как тип решетки
Бравэ, число формульных единиц N, координационные числа, координаци-
98
онные многогранники, формальны. На деле оказывается, что атом попадает в
то или иное окружение, ту или иную позицию не случайно. Например, атомы
Na в структуре галита NaCl располагаются в центрах октаэдра, вершины ко-
торого заняты атомами хлора, атомы Cs в структуре СdСl – в кубах из атомов
хлора. Координационные числа и тип построек из тех или иных атомов явля-
ется функцией химической связи между ними.
Химическая связь между частицами в структурах кристаллов может
быть представлена четырьмя ее предельными типами: металлическая, кова-
лентная, ионная и Ван-дер-Ваальсовая.
Типы связей в структурах. Основные типы кристаллических решеток
По природе входящих в состав кристалла частиц и по типу химической
связи кристаллические решетки подразделяются на молекулярные, ионные,
атомные (ковалентные) и металлические.
В узлах молекулярных решеток располагаются молекулы. Вещества,
имеющие молекулярные решетки, обычно обладают низкими температурами
плавления и кипения, высоким давлением насыщенного пара. К такому типу
веществ относятся, например: H
2
, O
2
, N
2
, галогены, CO
2
, все благородные га-
зы при низких температурах и многие органические вещества. Координаци-
онное число, например, для атома аргона равно 12. Связь между частицами в
решетке осуществляется силами Ван-дер-Ваальса. Энергия связи 4-40
кДж/моль.
В узлах ионных решеток находятся ионы противоположных зарядов.
Связь между частицами осуществляется за счет электростатических сил при-
тяжения, хотя может налагаться и сила взаимодействия перекрывающихся
орбиталей. Ионные кристаллы отличаются высокой температурой плавления.
Такую решетку имеют кристаллы NaCl. В узлах кристаллической решетки
могут находиться не только простые ионы, но и сложные, например, как в
кристаллах NH
4
NO
3
и (NH
4
)
2
SO
4
.Ионная связь является очень прочной.
Энергия связи 600-1000 кДж/моль.
99
В узлах атомной решетки, находятся связанные друг с другом кова-
лентной связью атомы. Вещества с такого типа решетками имеют высокую
температуру плавления и низкое давление насыщенного пара. Характерным
примером является алмаз, в кристаллической решетке которого все межъя-
дерные расстояния и все узлы между связями равны. Это обусловливает его
очень низкую энергию и, как следствие, – высокую твердость. Прочность ко-
валентной связи высока 600-1200 кДж/моль.
Металлическая решетка является разновидностью атомной и отличает-
ся тем, что в ее узлах находятся атомы и положительно заряженные ионы
(катионы). В пространстве между узлами перемещаются электроны, обеспе-
чивающие электронейтральность вещества. Эти подвижные электроны при-
дают металлам характерные свойства: металлический блеск, высокую элек-
тропроводность и теплопроводность, пластичность. Энергия металлической
связи 80-800 кДж/моль.
Рассмотренные предельные типы химической связи в чистом виде про-
являются чрезвычайно редко. Как правило, в кристаллах реализуются раз-
личные типы связей, из которых один зачастую преобладает над остальными.
Структуры, в которых между всеми атомами действуют силы одного
типа, называются гомодесмическими («десмос» – греч.– связь). Например:
хлорид натрия – NaCl, алмаз, кристаллы благородных газов.
Гетеродесмическими являются структуры, в которых действуют раз-
личные по типу связи. Например: графит, сера.
Существует классификация кристаллических структур, критерием ко-
торой служит характер межъядерных расстояний между частицами (геомет-
рический фактор) структуры. Выделяют пять различных структур: координа-
ционные, островные, цепочные, слоистые и каркасные.
В координационных структурах атомы не образуют каких-либо конеч-
ных или бесконечных группировок, а распределяются по всему кристалличе-
скому пространству равномерно, т.е. эти структуры гомодесмичны. Приме-
ром координационных структур могут служить структуры: NaCl – с ионной

100
связью, алмаза – с ковалентной связью, кристаллы благородно-газовых эле-
ментов с Ван-дер-Ваальсовой связью, Cu, Mg, Fe – с металлической связью.
Четыре остальные типа структур – гетеродесмические.
Островные структуры состоят из отдельных конечных группировок
(часто молекул), внутри которых реализуется один тип связи, а между ними–
другой.
Так, в кальците СaCO
3
внутри карбонатной группы (CO
3
)
2-
связь кова-
лентная, а между анионом (CO
3
)
2-
и катионом Са
2+
связь, в основном, ионная.
В островной структуре кристаллического хлора, построенной из отдельных
двухатомных молекул Сl
2
ковалентная связь, а между атомами хлора сосед-
них молекул молекулярная.
Цепочные структуры могут иметь как нейтральные, так и валентно-
насыщенные цепи. Примером первого типа является структура селена, где
между атомами Se, встроенными в цепи, реализуется ковалентная связь, а
между атомами разных цепочек – связи, близкие к Ван-дер-Ваальсовым.
К слоистым структурам можно отнести структуру графита, где кова-
лентные с примесью металлической связи реализованы внутри слоя, а Ван-
дер-Ваальсовы между слоями.
Каркасные структуры – представляют трехмерную структуру из атом-
ных группировок с достаточно большими пустотами. Например, различные
модификации кремнезема, где трехмерную ажурную постройку образуют
кремнекислородные тетраэдры [SiO
4
]
4-
, сочленяющиеся через общие верши-
ны.
Классификация силикатов
Рентгенографические и спектроскопические исследования в инфра-
красной части спектра показали, что силикаты – это наиболее обширный тип
химических соединений, в которых сочетаются ионные и ковалентные типы
химических связей. Значительно меньшую роль в них играют ван-дер-
ваальсовские и водородные связи. Основным элементом структуры силика-
