Шпора по физической и коллоидной химии (физический раздел)
Подождите немного. Документ загружается.


0ln
1
2
V
V
R
T
Q
.
При необратимом (самопроизвольном) расширении идеального газа от V
1
до V
2
(например,
ввакууме, рис.3.3) процесс происходит без совершения газом работы, так как Р=О и, соответственно,
передача энергии от резервуара не происходит: Q=0, т.е. изменение внутренней энергии (
U) для газа равно
нулю.
Рис. 3.3. При самопроизвольном расширении идеального газа от V
1
до V
2
ввакууме процесс происходит без
совершения газом работы, так как Р = О и,
соответственно, передачи энергии от резервуара не происходит: Q = 0,
т.е. изменение внутренней энергии (
U) для газа равно нулю
Однако состояние газа врезервуаре изменилось навеличину
1
2
ln
V
V
R
, асостояние резервуара
– нет. Поэтому вцелом состояние системы изменилось навеличину
1
2
ln
V
V
R
, т.е.
0ln
1
2
V
V
R
, так
как
12
VV
.
Таким образом, протекание самопроизвольного процесса визолированной системе вобщем
случае связано свозрастанием некоего параметра состояния системы. Этот параметр получил название
энтропии.
Из примера следует, что самопроизвольно визолированной системе протекают те процессы,
которые приводят к возрастанию энтропии системы.
Если энтропия системы висходном состоянии может быть выражена как S
1
=Rln V
1
,
авконечном состоянии S
2
= R ln V
2
, то изменение энтропии врезультате протекания обратимого процесса
следующее:
S = S
2
- S
1
= R ln V
2
/V
1,
или
S
(обр.процесс)
=
Т
Q
обр
. (3.12)
Соответственно для необратимого процесса (самопроизвольного)
S
(необр.процесс)
>
Т
Q
необр
. (3.13)
Справедливость последнего выражения следует из первого начала термодинамики.
В соответствии сI началом:
U = Q – W. (3.14)
Переведем систему из состояния 1 всостояние 2 обратимым и необратимым путем:
U
(обр)
=Q
обр
– W
обр,
(3.15)
U(необр) = Qнеобр – Wнеобр. (3.16)
Если
U является функцией состояния, то
U
(обр)
=
U
(необр)
. Известно, что W
обр
W
необр
,
следовательно Q
обр
Q
необр
.
S не зависит от пути процесса, так как является функцией состояния, т.е.
S
(обр)
=
S
(необр).
Тогда
ТQS
необрнеобр
)(
(3.17)
или вобщем случае
T
Q
S
; (3.18)
T
dQ
dS
. (3.19)
Знак равенства относится к обратимым, неравенства – к необратимым процессам.
3.4. Изменение энтропии изолированной системы
Для изолированной системы Q = 0, так как система не обменивается сокружающей средой ни
веществом, ни энергией, и
S
0. (3.20)
Для обратимого процесса
S = 0;
для необратимого энтропия системы увеличивается:
S
0. (3.21)
Какие бы процессы ни протекали визолированной системе, ее энтропия не может уменьшаться.
11

Так как самопроизвольные процессы визолированных системах идут сувеличением энтропии, то
при достижении равновесия энтропия изолированной системы будет максимальной, аее изменение равно
нулю:
S
равн.
= S
max,
S = 0.
Уравнения (3.22; 3.23) – критерии равновесия изолированных систем.
3.5. Статистическая природа второго начала
термодинамики
В то время как первое начало термодинамики является всеобщим законом природы, не знающим
ограничений и применимым к любым системам, второе начало термодинамики представляет собой
статистический закон, справедливый для макроскопических систем, состоящих из очень большого числа
частиц (молекул, атомов, ионов), для которых применимы физические понятия, имеющие статистическую
природу (например, как температура, давление).
Известно, что состояние и свойства любой макроскопической системы, состоящей из
совокупности большого числа частиц, могут быть описаны спомощью статистической механики. Сущность
статистического описания макросистем состоит вприменении к совокупности большого числа частиц
основных положений теории вероятности, а к отдельным частицам – законов классической механики.
С точки зрения статистической механики второе начало термодинамики, как это впервые было
показано Л.Больцманом, сводится к утверждению: все самопроизвольные процессы вмакроскопических
системах протекают внаправлении от менее вероятного к более вероятному состоянию системы.
Таким образом, процессы, запрещенные вторым началом, например самопроизвольный переход
тепла от менее нагретого тела к более нагретому, оказываются не невозможными, акрайне маловероятными,
вследствие чего они не наблюдаются.
Любое состояние системы характеризуется определенной термодинамической вероятностью, и
чем больше последняя, тем ближе система к состоянию равновесия. В состоянии равновесия система
обладает максимальной термодинамической вероятностью.
Л. Больцман предложил следующее уравнение, устанавливающее связь между энтропией S и
термодинамической вероятностью
:
S = k ln
,
где k – постоянная Больцмана, численно равная отношению газовой постоянной R к числу Авогадрo N
A
, т.е.
A
N
R
k
;
– термодинамическая вероятность системы, т.е. число микросостояний, которыми можно
осуществить данное макросостояние системы.
Статистическая термодинамика показывает, что энтропия может рассматриваться как
сумма составляющих, относящихся к различным формам движения частиц.
Принято группировать их по характеру движения частиц, рассматривая следующие составляющие
энтропии: энтропию поступательного движения молекул (Sпост.), энтропию вращательного движения
молекул (Sвращ.), энтропию вращательного движения атомов и атомных групп, содержащихся вмолекуле
(Sвн.вращ
.
), энтропию колебательного движения атомов и атомных групп (Sкол) и энтропию движения
электронов (Sэл.).
Таким образом, энтропию можно представить как сумму следующих составляющих:
S = Sпост +Sвращ + Sвн.вращ + Sкол + Sэл.
При этом некоторые из них можно рассматривать как сумму более частных составляющих. Так,
Sкол. является суммой составляющих, относящихся к различным видам колебаний.
При рассмотрении обычных химических процессов не учитывают составляющие энтропии,
связанные ссостоянием атомных ядер (спиновой эффект) и сизотопным эффектом.
Для каждого данного вещества энтропия возрастает при всех процессах, вызываемых движением
частиц (испарение, плавление, расширение газов, диффузия и пр.). Энтропия возрастает при ослаблении
связей между атомами вмолекулах и при разрыве их, т.е. диссоциации молекул наатомы или атомные
группы. Наоборот, супрочением связей уменьшается энтропия.
Вместе стем второе начало термодинамики не настолько простое в смысле его применения.
Рассмотрим, например, условия и задачу, которая была решена Клаузиусом всередине XIX века
следующим образом. Если Вселенная является изолированной системой, и энтропия вобратимых процессах
не меняется, авнеобратимых только возрастает, то это возрастание должно приводить к постепенному
выравниванию температуры во всех ее частях. В плане Вселенной это должно привести вконце концов к
полному выравниванию температуры, т.е. к «тепловой смерти». Правомерность такого вывода
рассматривается сразных сторон такими учеными, как М. Смолуховский, Я.Ван-дер-Ваальс и др. Можем ли
мы внастоящее время наоснове тех знаний, которые у нас есть, его оспорить?
12

Лекция 4.
Третье начало термодинамики.
Расчеты изменения энтропии
при различных процессах
4.1. Формулировка третьего начала термодинамики
В 1912 году М. Планк высказал постулат: при абсолютном нуле энтропия правильно
образованного кристалла чистого вещества равна нулю.
Справедливость постулата Планка, называемого третьим началом термодинамики, следует из
экспериментальных данных о зависимости теплоемкости кристаллических веществ от температуры, а также
из статистического характера второго начала термодинамики. При абсолютном нуле данное макросостояние
кристалла чистого вещества, кристаллическая решетка которого не имеет каких-либо дефектов, предельно
упорядочено и может быть реализовано единственным способом. Следовательно, термодинамическая
вероятность при абсолютном нуле равна 1:
S = k ln 1 S = 0.
На основании постулата Планка можно вычислить абсолютное значение энтропии. Если
T
dQ
dS
, а
CdTdQ
, то
T
CdT
dS
, где С– молярная теплоемкость данного вещества.
Интегрируя последнее уравнение впределах от абсолютного нуля до Т, получим:
T
S
T
CdT
dS
T
00
или
S
T
=
T
T
CdT
0
.
4.2. Абсолютные и стандартные значения энтропии
Энтропию S
T
называют абсолютной энтропией. Она численно равна изменению энтропии при
равновесном переходе 1 моля кристаллического вещества от абсолютного нуля до данной температуры.
Вычисление абсолютной энтропии по уравнению (4.3) возможно лишь втом случае, если известна
зависимость теплоемкости данного вещества от температуры.
Абсолютную энтропию тела в стандартном состоянии при данном Т называют стандартной
энтропией и обозначают через S
0
T
; чаще всего Т=298.15К и ее обозначают через S
0
298
:
S
0
298
=
298
0
T
CdT
.
Зная стандартную энтропию, можно вычислить значение абсолютной энтропии данного вещества
при любой температуре Т:
S
T
= S
0
298
+
T
T
CdT
298
. (4.5)
Таблицы стандартных значений энтропий играют существенную роль при расчетах констант
химических реакционных равновесий и определении направления протекания химических реакций и других
процессов.
Необходимо подчеркнуть, что третье начало термодинамики дает возможность вычислить
абсолютное значение энтропии различного рода веществ при данном состоянии, тогда как для других
термодинамических функций (U, H) могут быть определены только их изменения при переходе данной
системы из одного состояния вдругое.
4.3. Расчеты изменения энтропии в различных процессах
Методов непосредственного измерения энтропии не существует, но можно рассчитать изменение
этой функции при различного рода процессах, пользуясь математическим выражением второго начала
термодинамики для обратимых процессов. Так как энтропия является функцией состояния, то ее изменение
при переходе системы из начального состояния вконечное будет одним и тем же независимо от того,
совершается ли этот переход обратимым или необратимым путем.
1. Расчеты изменения энтропии при изотермических процессах
Примерами изотермических могут служить такие процессы, как плавление, испарение, возгонка,
превращение одной полиморфной модификации в другую. При обратимом (равновесном) проведении этих
процессов давление остается постоянным.
При изотермическом процессе, проводимом обратимо, изменение энтропии рассчитывается по
следующей формуле:
T
H
S
0
0
. (4.6)
2. Расчет изменения энтропии в неизотермических процессах
Если процесс протекает не изотермически, то расчет изменения энтропии проводят, исходя из
следующего:
,
T
dQ
dS
но
CdTdQ
,
тогда
T
CdT
dS
.
Для конечных изменений
2
1
T
T
T
CdT
S
или
13

1
2
ln
T
T
CS
.
Уравнение (4.7) справедливо для тех случаев, когда теплоемкость вданном температурном
интервале практически не зависит от температуры.
3. Расчет изменения энтропии сложного процесса
Изменение энтропии сложного процесса, состоящего из нескольких стадий, равняется сумме
изменений энтропий каждой отдельной стадии этого процесса:
ncл
SSSS ......
21
.
Например, изменение энтропии при обратимом превращении 10,0 г льда, находящегося при -10С,
в пар при 120С, если
С
(Н2О, ТВ)
= 2,03 Дж г
-1
К
-1
;
Н
пл. льда
= 331,89 Дж г
-1
;
С
(Н2О, Ж)
= 4,18 Дж г
-1
К
-1
;
Н
исп. Н2О
= 2253,4 Дж г
-1
.
С
(Н2О, Г)
= 1,93 Дж г
-1
К
-1
;
Вычисляют следующим образом.
Данный процесс представим из пяти стадий:
1. Нагревание льда от -10С до 0С, S
1
.
2. Плавление льда, S
2
.
3. Нагревание жидкой воды от 0С до 100С, S
3
.
4. Испарение воды, S
4
.
5. Нагревание пара от 100С до 120С, S
5
.
Изменение энтропии в1,3,5стадиях рассчитывают по уравнению
1
2
ln
T
T
CS
.
В стадиях 2,4 – по уравнению
T
H
S
.
Общее изменение энтропии составит:
54321
SSSSSS
сл
.
4.4. Расчет изменения энтропии
при протекании химического процесса
Изменение энтропии химического процесса равно алгебраической сумме стандартных энтропий
участников реакции с учетом их стехиометрических коэффициентов, причем энтропии продуктов реакции
берутся со знаком плюс, а энтропия исходных веществ – со знаком минус.
Для реакции, протекающей по уравнению aА + bB
mM + nN
0000
BANM
bSaSnSmSS
.
В общем виде:
0
.
0
ввисхвпрциир
SSS
(с учетом стехиометрических коэффициентов).
4.5. Критерии направления протекания процессов
и достижения равновесных состояний
в5открытых и закрытых системах.
Понятие об энергии Гиббса
По изменению энтропии можно судить о направлении и пределах протекания процессов только
визолированных системах. В случае закрытых и открытых систем необходимо также учитывать
изменение энтропии окружающей среды. Решение последней задачи сложно или невозможно. Поэтому
втермодинамике для изучения открытых или закрытых систем используют другие термодинамические
функции, так называемые термодинамические потенциалы, изменение которых позволяет определить
направление процессов и пределы их протекания без учета изменений вокружающей среде. В частности, к
термодинамическим потенциалам относится функция состояния, называемая энергией Гиббса, которую
обозначают черезG.
Понятие об энергии Гиббса было введено на основе объединенного уравнения первого и второго
начал термодинамики. Это уравнение может быть выведено следующим образом. Из первого начала
термодинамики следует:
;UQW
UWQ
; (4.11)
из второго начала термодинамики для обратимого процесса получаем:
STQ
. (4.12)
Для необратимого процесса:
Q
ST
. (4.13)
Подставляя значение
Q
из уравнения (4.12) и уравнений (4.13) в(4.11), находим:
для обратимого процесса
USTW
обр
.
; (4.14)
для необратимого процесса
.необр
W
UST
. (4.15)
Уравнение (4.14) называют объединенным уравнением первого и второго начал термодинамики
для обратимых процессов. Так как внутренняя энергия и энтропия являются функциями состояния, то их
изменения не зависят от того, как протекает данный процесс, обратимо или необратимо, следовательно:
.... необрнеобробробр
USTUST
и
.обр
W
.необр
W
,
(4.16)
т.е. работа, совершаемая при обратимом процессе, больше работы, производимой системой при
необратимом процессе при условии, что начальное и конечное состояния системы одинаковы вобоих
случаях.
Имея ввиду, что работа, производимая системой при обратимом процессе, является
максимальной для данного изменения состояния системы, преобразуем уравнение (4.14):
1212max
UUSSTW
. (4.17)
Группируя величины содинаковыми индексами, получим:
14

2211max
TSUTSUW
,
так как
U
и
S
– функции состояния, то величина (
)TSU
должна быть также функцией
состояния.
Если система кроме полезной работы совершает работу против силы внешнего давления (Р =
const), то для обратимого процесса
VPWW
'
maxmax
или
VPWW
max
'
max
,
где
'
max
W
– максимальная полезная работа, совершаемая системой вобратимом изобарно-
изотермическом процессе. Из уравнения (4.18) получаем для обратимого процесса:
VPUSTW
'
max
.
Для необратимого процесса
'
max
W
=
VPUST
.
Учитывая, что
12
VVV
,
получим
121221
'
max
PVPVTSTSUUW
.
Группируя величины содинаковыми индексами, находим:
222111
'
max
VPTSUVPTSUW
.
Величину (
PVTSU
), которая является функцией состояния, так как
SU ,
и
V
есть функции состояния, называют энергией Гиббса и обозначают G.
Раньше эту функцию состояния называли изобарно-изотермическим потенциалом.
Таким образом,
G =
PVTSU
.
Имея ввиду последнее уравнение, можно записать:
21
'
max
GGW
,
или, так как
12
GGG
;
GW
'
max
.
Из уравнения (4.25) следует, что максимальная полезная работа, совершаемая системой в
обратимом изобарно-изотермическом процессе, равна уменьшению энергии Гиббса.
Для необратимого процесса путем аналогичного преобразования справедливо
'
.необр
W
G
, (4.26)
т.е. уменьшение энергии Гиббса в необратимом процессе больше производимой системой работы
(полезной).
Зная, что
HPVU
,
уравнение (4.24) запишем следующим образом:
TSHG
(4.27)
или
STHG
. (4.28)
Последнее уравнение может быть представлено следующим образом:
STVPUG
(4.29)
или
STVPGU
. (4.30)
Из этого следует, что изменение внутренней энергии системы можно представить как сумму трех
слагаемых:
G
– часть внутренней энергии, способная при изобарно-изотермических условиях
превращаться вработу;
VP
–часть внутренней энергии, затрачиваемая системой на совершение работы против
сил внешнего давления;
ST
–связанная энергия, представляющая собой часть внутренней энергии, которая
вуказанных условиях не может быть превращена вработу.
«Связанная энергия» тем больше, чем больше энтропия данной системы. Таким образом,
энтропию можно рассматривать как меру «связанной энергии».
Определим изменение энергии Гиббса при протекании обратимого и необратимого процессов.
Для этого продифференцируем уравнение (4.27), помня при этом, что дифференциал
произведения двух функций равен сумме производных, взятых впредположении, что вданных условиях
изменяется только одна из функций, адругая остается постоянной.
В результате дифференцирования получим:
TSSTdHdG
. (4.31)
Из соотношений (4.13) и (4.15) следует:
dWdUST
, (4.32)
где знак равенства относится к обратимым, азнак неравенства – к необратимым процессам.
Предполагая, что никакой работы, кроме работы расширения, не производится, получаем:
PdVdUTdS
. (4.33)
Подставляя найденное значение
TdS
вуравнение (4.31) и зная, что
PVUH
,
следовательно
VdPPdVdUdH
, имеем:
15

VdPSdTdG
.
Из уравнения (4.34) следует, что для обратимых процессов при постоянных Р и T и при условии,
что из всех видов работы может производиться только работа расширения,
0dG
,
так как
dT
и
dP
=0.
Поскольку обратимые процессы являются равновесными, т.е. такими, когда система в каждый
момент времени находится в состоянии равновесия, то уравнение (4.35) является критерием равновесия.
Протекание необратимых процессов, к которым относятся все самопроизвольные процессы,
сопровождается уменьшением энергии Гиббса (Р и Т постоянны), так как при этом
dG
0.
Поэтому неравенство (4.36) является критерием направления самопроизвольных процессов.
Из неравенства (4.36) следует, что при переходе системы из неравновесного состояния
вравновесное G уменьшается и вмомент равновесия достигает минимального значения:
G
равн.
= G
min
.
Уравнение (4.37) представляет собой второй критерий достижения равновесия в открытых и
закрытых системах.
16

Лекция 6.
Химическое равновесие в гетерогенных
и гомогенных системах
6.1. Взаимосвязь химического потенциала
с другими термодинамическими функциями
С точки зрения термодинамики живые клетки представляют собой открытые системы. Как
указывалось ранее, открытой называется система, которая обменивается свнешней средой материей и
энергией. Основополагающие термодинамические уравнения, написанные для изолированных и закрытых
систем, должны быть вэтом случае модифицированы. В них необходимо ввести члены, отражающие
изменения массы системы. В этом случае дифференцирование уравнения для термодинамических функций
U, Н и G будут иметь следующий вид:
2211
dndnPdVTdSdU
2211
dndnVdPTdSdH
2211
dndnPdVSdTdG
где
– химический потенциал, n – число молей соответствующего компонента. Каждому компоненту
системы вуравнении соответствует свой член
dn. Если вправой части каждого уравнения все переменные,
за исключением n
1
, будут оставаться постоянными, то мы получим следующий ряд равенств:
32
1
32
1
32
1
1
,,,,,,,,, nnPT
n
G
nnPS
n
H
nnVS
n
U
а также из уравнения (6.1)
32
1
1
,,, nnVU
n
S
T
Из приведенных выше уравнений видно, что взависимости от того, какие величины остаются
постоянными, химический потенциал представляет собой парциальную молярную внутреннюю энергию,
энтальпию или свободную энергию. Поскольку химические процессы в живых клетках и в большинстве
экспериментальных систем in vitro протекают при постоянной температуре и при постоянном давлении,
наиболее полезным является определение химического потенциала как парциальной молярной свободной
энергии. При обсуждении свободной энергии Гиббса мы подчеркиваем значение этой величины как
критерия равновесия всистемах при постоянных Т и Р: равновесие достигается при
G=0.
Следовательно, когда свободная энергия перестает всистеме меняться, химический потенциал
любого компонента системы остается постоянным.
Таким образом, условие равновесия может быть записано как
I
=0 при Р и Т=const.
Аналогично тому, как мы определяли стандартные изменения для других термодинамических
функций и получали стандартные ΔН
°
,ΔS
°
и ΔG
°
, мы можем определить также стандартный химический
потенциал μ
°
как изменение свободной энергии на1 моль вещества, образующегося, расходующегося или
переходящего из одной фазы вдругую всвоем стандартном состоянии (т.е. при давлении в1 атм, при
определенной температуре и встандартной эталонной форме).
6.2. Летучесть
Стремление к улетучиванию. При описании поведения гетерогенной фазы (например, жидкости,
контактирующей сгазовой фазой, или твердого вещества вприсутствии своих паров) очень часто
пользуются понятием летучесть.
Летучесть определяется притяжением между молекулами. Другими факторами,
определяющими летучесть, являются кинетическая энергия молекул вещества, его форма, размер и т.д.
Наиболее удобным параметром, отражающим летучесть, является давление пара данного вещества. Если
вгазовой фазе присутствует более чем одно вещество, равновесные давления каждого из них называют
парциальными давлениями пара всоответствии сопределениями, данными законом парциальных давлений
Дальтона.
6.3. Идеальный раствор
Как реальные газы при определенных температурах и давлениях по своим свойствам близки
идеальным газам, так и реальные растворы при определенных условиях разбавления приближаются к
идеальному раствору.
Идеальным является такой раствор, вкотором свойства, присущие растворителю и
растворенному веществу, не меняются из-за присутствия новых компонентов, если не считать
возможных изменений этих свойств при разбавлении.
Стремление к улетучиванию для молекул растворителя или растворенного вещества
уменьшается только в той мере, вкоторой наличие молекул другого компонента пространственно
затрудняет или вообще делает невозможным уход молекул из раствора. В случае идеальных растворов
объем является аддитивным, атемпература при смешивании не изменяется.
В реальных растворах растворитель и растворенное вещество взаимодействуют друг сдругом.
Например, если спирт обладает низкой летучестью из-за сильного диполь-дипольного взаимодействия, то
при смешивании его сбензолом вследствие разделения диполей полярные молекулы спирта легче переходят
вгазовую фазу, и парциальное давление его пара будет выше. Возможно и наоборот вслучае, например,
растворения неполярного вещества вполярном растворителе.
Для того, чтобы применять законы для идеальных растворов вслучае реальных, необходимо
введение некоторых ограничений. Один из таких принципов носит название предельного закона. Он гласит,
что если содержание растворенных молекул врастворе относительно мало, то взаимодействие между
ними будет минимальным и, следовательно, они будут слабо влиять наповедение растворителя.
Таким образом, законы идеальных растворов можно применять к реальным растворам, если речь
идет о разбавленных. Для рассмотрения свойств реальных растворов при относительно высоких
концентрациях растворенного вещества имеются также уравнения, однако они достаточно сложны.
Прежде чем приступить к обсуждению некоторых относительно простых уравнений, тем не
менее, позволяющих рассчитывать давление пара, точку замерзания, точку кипения, атакже осмотическое
давление растворов, познакомимся сдвумя фундаментальными соотношениями, лежащими воснове
предельных уравнений, – справилом фаз и уравнением Клаузиуса-Клапейрона.
Правило фаз. Нарис. 6.1 показана фазовая диаграмма, количественно описывающая поведение
гетерогенной системы, содержащей гомогенные области-фазы. Фазы отделены друг от друга заметными
границами, которые называют поверхностями раздела. Каждая фаза гомогенна, однако она не непрерывна.
Число фаз равно числу отделенных друг от друга структур, существующих вразличных физических
состояниях всистеме. В одной системе могут существовать несколько жидких или твердых фаз, например:
вода – масло, лед – твердая соль. Различают как число фаз, так и число компонентов, образующих фазу. Под
числом компонентов понимают число независимых химических индивидуальностей. Нарис. 6.1 показана
хорошо известная фазовая диаграмма воды. Она является однокомпонентной. Если вводе растворить соль,
то получим двухкомпонентную систему. Если растворить два белка вбуфере, получим пятикомпонентную
систему – два белка, вода, соль и кислота.
Изучение гетерогенных систем сильно упростилось после предложенного в1874 году Гиббсом
обобщения, которое получило название «правило фаз». Оно состоит из очень простого соотношения: а=
с– р + 2, где с– число компонентов системы, р – число фаз и f – число степеней свободы системы, т.е.
число независимых переменных – таких, как температура, давление и концентрация, которые необходимы
для полного описания системы.
17

Согласно альтернативной формулировке правила фаз, число степеней свободы – это число
независимых переменных, которые могут быть изменены без изменения числа фаз. Правило фаз применимо
только для систем, находящихся вравновесии.
Посмотрим нафазовую диаграмму воды. Поскольку вода является единственным компонентом,
значит с= 1. Вода существует втрех фазах – твердой, жидкой и газообразной. При этом число фаз, которые
существуют вравновесии, зависит от температуры и давления.
Рис. 6.1. Фазовая диаграмма воды и гипотетического 1 т идеального раствора (масштаб не соблюдается)
Линия ОА представляет собой кривую давления паров воды. Вдоль этой линии вода и пар
находятся вравновесии друг сдругом. Экспериментально такую линию получают путем измерения
давления пара чистой воды при разных температурах.
Линия ОВ является кривой сублимации льда. Выше этой кривой вода существует ввиде льда,
ниже – ввиде пара. В равновесии лед и пар находятся только вдоль линии ОВ, которая и является границей
этих двух фаз.
Линия ОС описывает зависимость точки плавления льда от давления; лед и жидкая вода этой
линии находятся вравновесии. Наклон линии ОС относительно оси ординат указывает нато, что при
увеличении давления точка плавления льда понижается. Три кривые имеют общую точку пересечения 0,
известную под названием «тройной точки».
6.4. Фазовая диаграмма содержит зоны,
линии и тройную точку
Для зоны с= 1, р = 1 и f = 2. Для линий с= 1, р = 2 и f = 1. Для тройной точки с= 1, р = 3 и f = 0.
Что означают различные степени свободы? То, что внутри зон f = 2, означает следующее: для описания
поведения системы мы должны использовать и температуру и давление, т.е. обе величины могут меняться
без изменения числа фаз, значит вода существует вжидком состоянии при различных температурах и
давлениях. f = 1 означает, что мы можем установить точку налинии, т.е. описать систему только
температурой или давлением. Т.е. вдоль линии каждой температуре соответствует строго определенное
давление пара. При любом давлении пара для льда существует только одна точка для температуры
плавления. В тройной точке система инвариантна, т.е. f = 0, т.е. система может находиться вравновесии
только при одном значении температуры и давления.
6.5. Уравнение Клаузиуса-Клапейрона
Из рис. 6.1 видно, что наклон ВО и ОА награфике задается производной dP/dT, которая
представляет собой скорость изменения давления пара от Т. Наклон ОС численно равен dP/dT – величина,
обратная скорости, скоторой точка плавления изменяется при изменении давления. Уравнение, которое
связывает эти изменения сдругими измеряемыми свойствами системы, было предложено в1834 году
Б.Клапейроном и позже модифицировано Р.Клаузиусом.
Это уравнение можно вывести, используя термодинамические соотношения для химического
потенциала. В принципе любые свойства (такие, как объем, энтальпия, свободная энергия) зависят от
количества вещества и являются экстенсивными. Однако если они относятся к одному молю вещества
встрого определенных условиях, они становятся характеристичными свойствами вещества при данных
условиях.
Объем, реально занимаемый одним молем растворенного вещества, называется парциальным
молярным объемом растворенного вещества. Он соответствует изменению общего объема очень
большого количества раствора при добавлении одного моля растворенного вещества. Очевидно, что при
добавлении одного моля растворенного вещества концентрация не будет меняться только при условии
бесконечно большого объема исходного раствора.
В этом случае для парциального объема можно записать:
3211
1
1
nnnPT
dn
V
V
s
,
где V – общий объем раствора, Т – температура, Р –давление, n – число молей других веществ. Величина V
является функцией Т и Р, атакже состава раствора.
Если компонент распределен между двумя фазами и , то при равновесии
. В случае
однокомпонентной системы химический потенциал равен величине свободной энергии, приходящейся на1
моль:
= G
и
=
G
.
Если
будет слегка меняться при небольших изменениях Т и Р, то аналогичное изменение будет
наблюдаться и для
(при сохранении равновесия). Поэтому можно записать
GdGd
.
Далее мы знаем, что
dG = VdP-SdT. (6.4.)
Подставим вэто уравнение выражение для парциальных молярных величин
V
dP -
S
dT =
V
dP -
S
dT. (6.5)
Преобразуем выражение (6.5) ввиде члена dP/dT
18
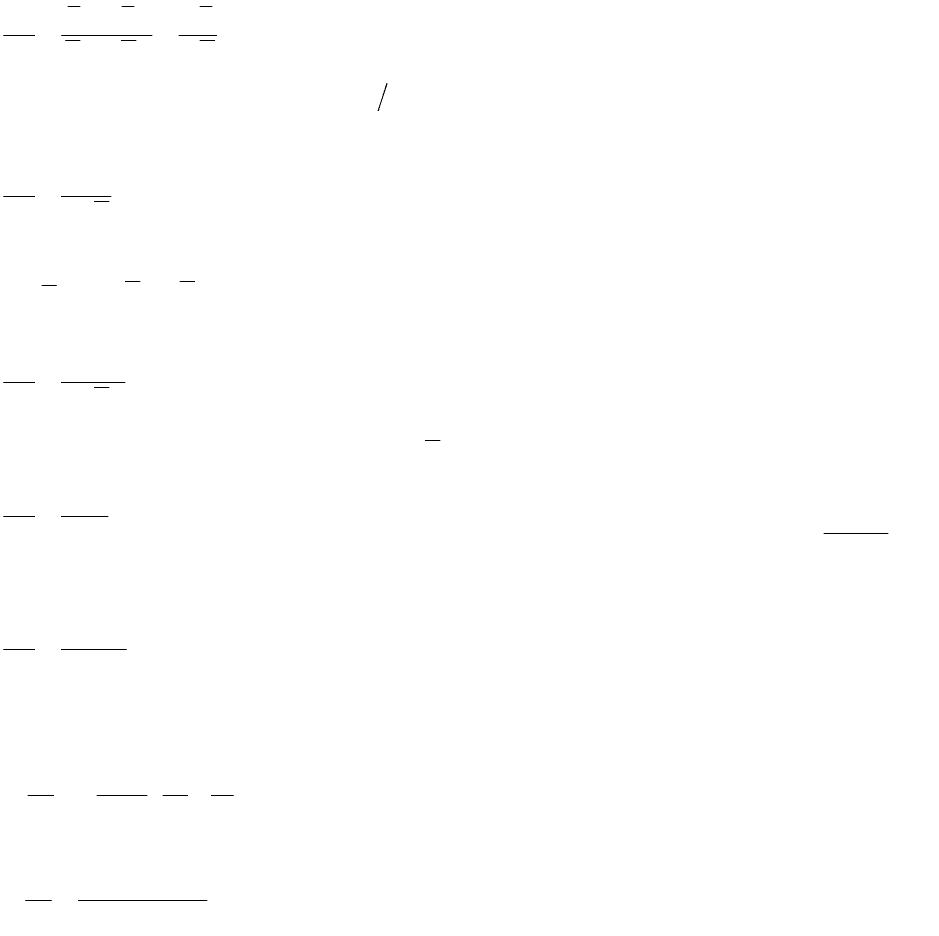
V
S
VV
SS
dT
dP
.
Выражение S по второму началу термодинамики
TQS
обр
, где Q
обр
представляет собой
молярную теплоту испарения или молярную теплоту плавления.
Подставим S вуравнение (6.6) и получим уравнение Клапейрона:
VT
Q
dT
dP
.
В таком виде это уравнение нельзя проинтегрировать. Р.Клаузиус предложил несколько
допущений, что позволяет преобразовывать уравнение вболее удобную форму – например, вслучае
равновесия пар–вода
V
равно (
жг
VV
). Величина V
ж
для воды составляет приблизительно
0,1% от V
г
и поэтому V
ж
можно не учитывать вчлене V
(г)
–
V
(ж)
. Тогда придем к уравнению
г
VT
Q
dT
dP
.
Если принять, что пар подчиняется законам идеального газа, то вместо
г
V
запишем RT / P:
2
RT
Q
dT
dP
.
Заменим выражение для Q более традиционным Н
V
, получим уравнение Клаузиуса-Клапейрона
вобычной форме:
2
RT
PH
dT
dP
V
.
Это уравнение можно проинтегрировать, если предположить, что молярная теплота испарения
Н
V
является постоянной, т.е. не зависит от температуры. После интегрирования впределах между Р
1
, Т
1
и
Р
2
, Т
2
получаем:
121
2
11
ln
TTR
H
P
P
V
или в форме
12
12
1
2
ln
TTR
TTH
P
P
V
.
6.6. Коллигативные свойства растворов
Рассмотрим, что происходит срастворителем, если внем растворяют твердое вещество
сисчезающе малым давлением пара. Некоторые свойства растворителя могут зависеть лишь от числа
добавленных новых частиц. Интересно, что некоторые эти свойства мало зависят от природы
растворенного вещества. Это происходит в том случае, если растворенное вещество не взаимодействует
срастворителем и не подвергается ассоциации и диссоциации, т.е. число молекул сохраняется
постоянным. В таком случае говорят околлигативных растворах или о коллигативных свойствах
растворов.
Четыре свойства из группы коллигативных свойств обычно рассматриваются вместе: понижение
давления пара, повышение точки кипения, понижение точки замерзания и осмотическое давление.
Закон Рауля. Точные измерения, которые позволили математически описать влияние
растворенного вещества нафизические свойства растворителя, были сделаны впервые Ф.-М.Раулем,
работавшим вуниверситете Гренобля всередине и конце XIX века (1830-1901 гг.).
Ф.-М.Рауль обнаружил, что давление пара раствора, содержащего нелетучее растворенное
вещество, прямо пропорционально концентрации растворителя. Математически это можно записать так:
Р = kx
1
,
где Р – давление пара раствора, k – константа пропорциональности, х
1
– молярная доля растворителя. Когда
растворенное вещество отсутствует х
1
= 1, то коэффициент k численно равен давлению пара чистого
растворителя – Р
0
. Значит
Р = Р
0
х
1.
(6.11)
Поскольку х
1
+ х
2
= 1,0, где х
2
– молярная доля растворенного вещества, то мы можем
преобразовать уравнение (6.11) в (6.12), подставив вместо х
1
=1- х
2
:
2
0
0
x
P
PP
.
(6.12)
Это уравнение показывает, что относительное понижение пара растворителя равно мольной
доле растворенного вещества и что давление пара раствора пропорционально молярной доле
растворителя. Уравнения (6.11) и (6.12) отражают закон Рауля впреобразованной форме. Закон Рауля и
уравнения (6.11) и (6.12) позволяют определить чистоту растворителя и наличие внем нелетучих веществ.
6.7. Понижение точки замерзания и повышение точки
кипения растворов
Понижение точки замерзания и повышение точки кипения растворов являются прямыми
следствиями понижения давления пара.
Рассмотрим двухкомпонентную систему. При растворении одного вещества число химических
индивидуальностей возрастает до 2. По правилу фаз
f = c – p + 2 = 2 – p + 2 = 4 – p.
Если существует лишь одна фаза, то у системы должно быть три степени свободы: температура,
давление и концентрация.
Рассмотрим вывод формулы для определения повышения точки кипения.
Для этого возьмем уравнение Клаузиуса-Клапейрона поскольку оно является основополагающим
соотношением, связывающим давление пара и температуру:
19
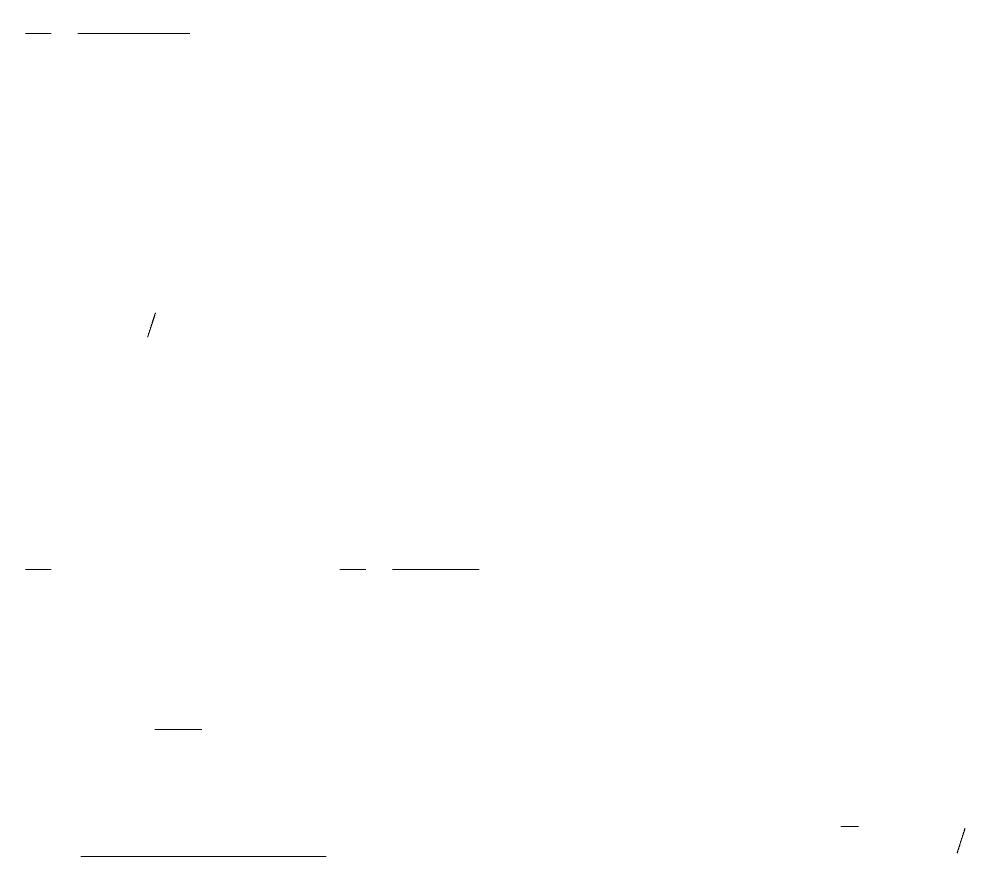
0
00
ln
RTT
TTH
P
P
,
где P
0
и Т
0
– давление пара и температура кипения чистого растворителя.
Сделаем некоторые упрощения.
а) Всоответствии сзаконом Рауля для идеальных растворов нелетучих веществ P = P
0
x
1
.
Логарифмирование обеих частей уравнения дает:
lnP = lnP
0
+ ln x
1
или
ln (P
0
/P) = –ln x
1
= –ln (1-x
2
).
Всоответствии стеоремой Маклорена имеем:
–ln(1-x
2
) = x
2
+
21
x
2
2
+ 1/3 x
2
3
+ …
Поскольку величина х
2
для разбавленных растворов значительно меньше1, то можно считать, что
–ln(1 – х
2
) х
2.
б) Молярная доля растворенного вещества х
2
равна n
2
/(n
1
+ n
2
); для разбавленных растворов
можно записать, что х
2
n
2
/n
1.
в) Поскольку изменение Т происходит вочень узком интервале температур, то Т практически
равно Т
0
. Поэтому вместо Т
0
Т подставим Т
0
2
. Величину Т–Т
0
вчислителе обозначим Т
кип
.
Сделав эти упрощения и подставив в уравнение Клаузиуса-Клапейрона, получим:
2
0
1
2
221
0
1lnlnln
RT
TH
n
n
xxx
P
P
кип
.
Для 1000г воды вкачестве растворителя n
1
= 1000/18 = 55,6, аn
2
– это моляльность раствора.
Подставим вэто уравнение вместо n
2
/n
1
значение 0,018m. Решая уравнение относительно величины Т
кип,
т.е. повышения температуры кипения, получаем:
H
RT
mT
кип
2
0
018.0
.
Т кипения воды при давлении 1атм равна 373,15°. При этой температуре и давлении 1 атм
молярная теплота ее испарения равна 18539кал, R=1,987кал/мольград. Тогда
513.0
53918
)15.373(987.1018.0
2
m
m
T
кип
.
Таким образом, мы получили значение эбулиоскопической константы для водных растворов.
Аналогично можно получить и соответствующее выражение для криоскопической константы. Размерность
этих констант град/моль.
В общем виде уравнение, связывающее изменение температуры кипения или замерзания
растворов в сравнении с чистым растворителем, выглядит так:
mKT
,
(6.16)
где К – эбулиоскопическая или криоскопическая константа, m – моляльная концентрация раствора.
6.8. Осмотическое давление
Живым системам присущи различные физико-химические механизмы транспорта растворителя и
растворенных веществ. Различают активный и пассивный транспорт. Активный транспорт характерен для
живых мембран. Мы пока остановимся напассивном транспорте, который более изучен и лучше может быть
описан математически. Так, в1748 году А.Ноллет впервые наблюдал, как растворитель проходит через
мембрану из разбавленного раствора вболее концентрированный. Если к более концентрированному
раствору приложить давление, то взависимости от его величины течение растворителя может быть
замедлено, остановлено или обращено.
Осмотическим давлением раствора называется то наименьшее давление, которое, помимо
давления самого растворителя, необходимо приложить к раствору, чтобы предотвратить перетекание
растворителя к раствору через мембрану, разделяющую раствор и растворитель, причем мембрана
непроницаема для молекул растворенного вещества (полупроницаема) внаправлении от чистого
растворителя к раствору. Растворитель может перетекать из более разбавленного раствора вболее
концентрированный даже втом случае, если единственной разделяющей поверхностью между двумя
растворами будет слой пара.
По-видимому, осмотические эффекты не должны зависеть от природы мембран, используемых
для их измерения. В противном случае можно бы было построить вечный двигатель, используя этот эффект.
В 1877 году В.Пфеффер измерил осмотическое давление П нескольких растворов,
приготовленных из одного и того же количества вещества вразных объемах растворителя. При этом он
показал, что при постоянной температуре произведение П V всегда одно и то же. Он обнаружил также, что
для данного раствора сповышением температуры осмотическое давление растет, однако отношение П/Т
сохраняется постоянным. Датский химик Я.Вант-Гофф обобщил результаты и предложил эмпирическое
уравнение для описания осмотического давления растворов. Это уравнение имеет вид:
П = CRT, (6.17)
где П – осмотическое давление, С– молярная или моляльная концентрация раствора, аТ – температура.
Линейная зависимость П от Си Т соблюдается только для идеальных растворов. Таким образом, уравнение
Вант-Гоффа служит еще одним примером предельного закона.
Однако уравнение осмотического давления можно однозначно вывести, исходя из теоретических
соображений. Осмотическое давление раствора можно интерпретировать как следствие того факта, что
давление пара раствора нелетучего вещества ниже, чем давление пара чистого растворителя.
Уравнение осмотического давления легко получить, если предположить, что пар растворителя
ведет себя как идеальный газ. Когда раствор отделен от чистого растворителя полупроницаемой мембраной
и система путем увеличения общего давления на раствор приведена к равновесию, свободная энергия на
моль растворителя должна быть одинакова по обе стороны от мембраны. Уменьшение свободной энергии на
моль растворителя в растворе (по сравнению с его свободной энергией в стандартном состоянии)
выражается уравнением (6.14):
0
ln PPRTG
.
(6.18)
Увеличение давления, которое приложено к раствору, должно быть достаточным для того, чтобы
восстановить свободную энергию растворителя врастворе до свободной энергии чистого растворителя. Это
увеличение свободной энергии зададим уравнением
dG = VdP при Т = const, (6.19)
так как жидкость несжимаема:
G = V
Р . (6.20)
20
