Шпора по физической и коллоидной химии (физический раздел)
Подождите немного. Документ загружается.


1
2
lg
303,2
a
a
zF
RT
E
.
Концентрационные элементы без переноса ионов состоят из двух электродов – твердых сплавов
или амальгам, отличающихся по содержанию активного вещества. Оба электрода погружены водин и тот же
раствор, содержащий ион активного вещества. В этих элементах существует граница между жидкими
фазами и нет диффузионного потенциала, искажающего результаты измерения ЭДС.
Примером такого элемента может служить кадмиевый амальгамный элемент.
В этом случае происходит перенос кадмия от более концентрированной амальгамы к менее
концентрированной. ЭДС такого элемента (при
21
aa
) равна
2
1
lg
303,2
a
a
zF
RT
E
.
Эта формула справедлива, если металлы, входящие всостав сплава (или амальгамы), не образуют
химических соединений.
31
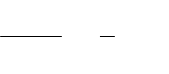
Лекция 12.
Поверхностные явления и адсорбция
12.1. Общая характеристика поверхностных явлений
К поверхностным явлениям относится совокупность явлений, связанных сособенностями свойств
пограничных слоев между двумя соприкасающимися фазами, обусловленных наличием избыточной энергии
у поверхности раздела. Эти явления могут быть разделены надве основные группы. К первой группе
следует отнести явления, связанные сизменением формы поверхностей раздела (капиллярные явления,
смачивание, прилипание и др.). Ко второй группе относятся адсорбированные явления, воснове которых
лежит изменение состава поверхностного слоя.
Молекулы вещества, расположенного внутри фазы, отличаются по энергетическому состоянию от
молекул, находящихся награнице раздела фаз.
Во внутренних слоях фазы силы взаимодействия для каждой молекулы в среднем по времени
одинаковы по всем направлениям, полностью скомпенсированы и их равнодействующая равна нулю.
Поэтому произвольное перемещение молекулы жидкости или газа внутри фазы влюбом направлении не
связано свыделением или поглощением энергии. Иначе обстоит дело смолекулами, находящимися
награнице раздела фаз. Они испытывают неодинаковое влияние сил межмолекулярного взаимодействия со
стороны каждой из соседних фаз, поскольку их физические свойства (плотность, поляризуемость и т.д.)
различны.
Поверхностная молекула награнице жидкость/пар испытывает одностороннее притяжение со
стороны жидкости, втягивающее ее внутрь жидкости.
В общем случае равнодействующая сил межмолекулярного взаимодействия поверхностных
молекул перпендикулярна поверхности раздела и направлена всторону фазы сболее интенсивным
межмолекулярным взаимодействием. Эта сила, отнесенная к единице площади поверхности раздела, носит
название внутреннего давления. Как правило, внутреннее давление тем больше, чем выше полярность
вещества. Втягивая поверхностные молекулы внутрь фазы, внутреннее давление стремится уменьшить
поверхность до минимума, возможного вданных условиях.
Увеличение площади поверхности раздела фаз связано свыделением молекул из глубины фазы
наповерхность, т.е. ссовершением работы против сил внутреннего давления. Эта работа W вобратимых
изотермических условиях пропорциональна площади образующейся новой поверхности S:
-dW =
dS.
Максимальная работа W, взятая со знаком минус, взависимости от условий (р = соnst, или V =
const) равна увеличению энергии Гиббса или энергии Гельмгольца.
Подобным же образом к увеличению поверхностной энергии Гельмгольца приводит и работа
разрыва связей при дроблении твердых тел (V = const), сопровождающаяся увеличением площади
поверхности раздела фаз.
Коэффициент пропорциональности
равен работе увеличения поверхности при постоянных
температуре, объеме и составе, отнесенной к единице поверхности. Он численно равен удельной
поверхностной энергии Гельмгольца и называется поверхностным натяжением. В случае двух
конденсированных фаз чаще используется понятие «межфазное натяжение». Сложилось так из-за того, что
это понятие было введено раньше, чем была развита термодинамика поверхностных явлений. Величину
рассматривали как силу, направленную тангенциально к поверхности и стягивающую ее, однако
использование такого понятия может привести к неправильному выводу о том, что существует особая,
отличная от межмолекулярных сила (поверхностная) и увеличение поверхности есть результат ее
растяжения, т.е. увеличения расстояния между молекулами вповерхностном слое. Размерность величины
– энергия наединицу поверхности (джоуль наквадратный метр), или, что то же, сила наединицу длины
(ньютон наметр).
12.2. Поверхностные явления в5дисперсных системах
В гетерогенных системах, в которых одна из фаз представляет собой сравнительно крупные
частицы, поверхность раздела фаз невелика. В таких системах поверхностные явления практически не
проявляются. По мере уменьшения размеров частиц (диспергирования) вещества одной из фаз возрастает
абсолютная величина поверхности раздела и поверхностные свойства в дисперсных системах приобретают
все большее значение.
Мерой раздробленности, или дисперсности, системы принято считать дисперсность D – величину,
обратную величине размера (диаметра) дисперсной частицы а.
Для сравнения поверхностей раздела принято пользоваться понятием удельной поверхности S
уд
.,
т.е. величиной поверхности всех частиц, заключенной вединицах массы вещества.
Величина удельной поверхности пропорциональна дисперсности системы (обратно
пропорциональна размеру частиц):
kD
a
k
ak
ak
S
уд
1
3
2
2
1
.
, (12.2)
где k
1
, k
2
и k – коэффициенты пропорциональности, связанные сформой частиц. Например, для частиц
шарообразной формы k
1
= ; k
2
= /6 и k = 6, а для кубической – соответственно 6,1 и 6. При размерах частиц
порядка 10 нм величина удельной поверхности – сотни квадратных метров награмм. Таким образом,
врезультате диспергирования вещества происходит увеличение роли поверхностных свойств в общих
свойствах системы и одновременно увеличивается абсолютное значение поверхностной энергии, что
определяет огромное значение поверхностных явлений для дисперсных систем. Поверхностные явления,
например, лежат воснове свойств коллоидных систем.
12.3. Поверхностное натяжение и природа вещества
Поскольку поверхностное натяжение является результатом нескомпенсированности
межмолекулярного взаимодействия вразных фазах, оно определяется разностью интенсивности
взаимодействия молекул внутри каждой фазы и взаимодействия молекул различных фаз. Интенсивность
молекулярных взаимодействий внутри фазы втеории поверхностных явлений обычно обозначают термином
«полярность». Полярность вещества вочень большой степени связана стакими параметрами, как дипольный
момент молекул, диэлектрическая проницаемость, поляризуемость молекул, способность к образованию
водородной связи между молекулами. Однако существенное значение играют также плотность вещества,
геометрия строения молекул, ориентация молекул вповерхностном слое, определяющая направление
силовых полей, возможная взаимная растворимость граничащих фаз, их химическое взаимодействие.
Экспериментальные методы определения поверхностного натяжения применимы к двухфазным
системам с легкоподвижной, обратимо изменяемой поверхностью раздела газа сжидкостью или двух
несмешивающихся жидкостей. Как правило, они основаны наизмерении силы, уравновешиваюшей
поверхностное натяжение. Прямое определение поверхностной энергии твердых тел невозможно, и
величина
для них оценивается лишь косвенно.
Самое малое поверхностное натяжение характерно для сжиженных инертных газов, поскольку
симметричные молекулы их обладают ничтожной поляризуемостью. Поверхностное натяжение
органических жидкостей возрастает сувеличением их полярности. Вода обладает очень большой величиной
поверхностного натяжения по сравнению сдругими жидкостями, что связано со склонностью воды к
образованию водородных связей.
Еще выше поверхностное натяжение расплавленных солей и металлов, для которых характерна
ионная связь, например:
жидкий гелий Т = –270,5˚С
10
3
, Дж/М
2
– 0,30
гексан (20) 9,8
фенол (20) 42,3
вода (20) 72,7
расплав NaCl (810) 113
32
жидкое железо (1515) 1880
Поверхностная энергия твердых тел, определяемая косвенными методами, оказалась существенно
большей, чем вслучае жидкостей.
12.4. Термодинамика поверхностных явлений
в5однокомпонентных системах
Для однокомпонентной жидкости поверхностное натяжение
численно равно работе внешних
сил при обратимом изотермическом увеличении площади поверхности наединицу при постоянном объеме
(т.е. увеличению энергии Гельмгольца F). Таким образом, F =
. По уравнению Гиббса-Гельмгольца
V
T
F
TFU
.
Обозначая полную поверхностную энергию через
, можно переписать уравнение (12.3) для
поверхности:
V
T
T
.
При повышении температуры кинетическая энергия движущихся молекул увеличивается,
поверхностное натяжение при этом уменьшается. При приближении к критической температуре Ткр.
плотности сосуществующих фаз (жидкости и пара) сближаются. При достижении Ткр. граница раздела фаз
исчезает и поверхностное натяжение становится равным нулю. Для многих веществ экспериментально
показано, что вне очень широком температурном интервале уменьшение
стемпературой выражается
формулой
0
dT
d
,
где
– константа, а
0
– поверхностное натяжение при выбранной начальной температуре. Величина
для разных жидкостей составляет 0,002 0,004 К
-1
.
12.5. Равновесие фаз при искривленной поверхности
раздела. Капиллярность
На практике нередко приходится иметь дело сискривленной поверхностью раздела. Например,
поверхность капли выпукла, аповерхность жидкости всмачиваемом капилляре вогнута.
Понятно, что молекула жидкости, находящаяся навыпуклой поверхности, будет испытывать
равнодействующую силу, направленную в глубь жидкости, меньшую, чем наплоской поверхности.
Навогнутой поверхности, наоборот, эта сила больше. Поэтому, если наплоской поверхности давление
вобеих сосуществующих фазах одинаково, то наискривленной поверхности вусловиях равновесия
возникает добавочное давление, направленное всторону той фазы, по отношению к которой поверхность
вогнута. Другими словами, при равновесии давление вфазе, отделенной от другой фазы вогнутой
поверхности, больше. Эта разность давлений, возникающая по обе стороны искривленной поверхности
жидкости, носит название капиллярного (или лапласова) давления.
Величина капиллярного давления зависит от кривизны поверхности и поверхностного натяжения
и выражается уравнением Лапласа.
Рассмотрим элементарный участок искривленной поверхности с площадью
S = l
1
l
2
.
Если r
1
и r
2
– радиусы кривизны криволинейных отрезков l
1
и l
2
, то площадь S равна
S = l
1
l
2
= r
1
1
r
2
2
, (12.7)
где
1
и
2
– соответствующие центральные углы (рис. 12.1).
Рис. 12.1. Элементарный участок искривленной поверхности
Если под действием, вызванным разностью давлений Р по обе стороны поверхности, сама
поверхность сместилась навеличину dr без изменения кривизны, то произошло увеличение этой
поверхности навеличину dS. Затраченная работа dW может быть вычислена двумя способами: работа dW
равна произведению силы напуть:
dW =
РSdr, (12.8)
но эта же работа dW равна произведению поверхностного натяжения наприрост поверхности:
dW =
dS. (12.9)
Поэтому
dS =
РSdr =
1
2
r
1
r
2
Рdr. (12.10)
Найдем dS:
dS =
1
2
(r
1
+dr)( r
2
+dr) -
1
2
r
1
r
2
. (12.11)
После несложных преобразований, пренебрегая членом (dr)
2
как величиной бесконечно малой
второго порядка, получим:
33
dS =
1
2
r
1
dr -
1
2
r
2
dr.
Подставим уравнение (12.12) в уравнение (12.11) и разделим обе части уравнения на r
1
r
2
1
2
,
получим формулу Лапласа, выражающую избыток давления со стороны вогнутой поверхности:
21
11
rr
P
.
Если поверхность сферическая, то r
1
= r
2
и лапласово давление равно
r
P
2
.
Вследствие существования лапласова давления величина давления насыщенного пара жидкости
при данной температуре зависит от формы поверхности.
12.6. Уравнение Томсона
Обозначим через r радиус сферической поверхности раздела фаз (радиус капли), через Р
0
–
давление насыщеного пара над плоской (r = ), ачерез Р – над выпуклой поверхностью. Перенесем
некоторое количество жидкости dm сплоской поверхности жидкости вкаплю радиуса r путем обратимого
изотермического испарения при давлении Р
0
, обратимого сжатия пара от Р
0
до Р и последующей обратимой
изотермической конденсации при Р. Поскольку работа испарения и конденсации равны и противоположны
по знаку, то общая работа переноса dW, совершаемая над системой, оказывается работой сжатия пара:
P
P
RT
M
dm
dW
0
1
ln
,
где М – молярная масса вещества.
С другой стороны, врезультате переноса dm вещества увеличивается масса капли за счет
увеличения ее радиуса наdr и поверхность наdS, что требует затраты энергии наработу против сил
поверхностного натяжения (работу увеличения поверхности).
В обоих случаях осуществляется перенос количества dm, поэтому работы dW
1
и dW
2
равны по
абсолютной величине и противоположны по знаку:
dS
P
P
RT
M
dm
0
ln
.
Так как m капли срадиусом r равна m = 4/3
r
3
, где
- плотность жидкости - то dm = 4
r
2
dr.
Поверхность капли S = 4
r
2
, поэтому dS = 8
rdr. Подставим эти значения dm и dS вуравнение (12.16) и
решим его относительно r. Получим:
P
P
RT
V
r
0
ln
2
(V – молярный объем жидкости
M
), что являет собой уравнение Томсона для выпуклой поверхности.
Для вогнутой поверхности кривизна отрицательна. Поэтому:
0
ln
2
P
P
RT
V
r
. (12.18)
Уравнение Томсона (Кельвина) и уравнение Лапласа являются основными уравнениями
физической химии поверхностных явлений.
Следствия из полученных уравнений.
Давление пара (насыщенного) жидкости Р
0
над плоской поверхностью (поверхность сr = )
меньше, чем давление пара над каплей радиуса r (Р
0
Р), но больше, чем давление пара Р над вогнутой
поверхностью ( r 0, Р
0
Р).
Чем меньше размер капли, тем больше равновесное давление ее насыщенного пара, и,
следовательно, тем выше значение химического потенциала жидкости, т.е. тем не менее устойчиво ее
состояние. Поэтому мелкие капли, обладая большим давлением пара, испаряются быстрее. Испарившееся
вещество может конденсироваться наповерхности более крупных частиц и наплоской поверхности. Такой
процесс роста крупных частиц за счет исчезновения (испарения) мелких носит название изотермической
перегонки (переконденсации). Таким образом, всякая полидисперсная система термодинамически
неравновесна, апоэтому неустойчива.
Равновесие твердых частиц по отношению к жидкому раствору можно выразить уравнением,
сходным суравнением Томсона. В растворе мерой интенсивности перехода вещества вдругую фазу
является концентрация насыщенного раствора, и тогда применительно к дисперсной системе твердая фаза –
раствор можно записать:
0
ln
2
CCRT
V
r
, (12.19)
где С
0
– концентрация насыщенного раствора, С– концентрация вещества врастворе, равновесном
скристалликами размером r. Поэтому при растворении высокодисперсных веществ можно получить
концентрацию раствора выше обычной растворимости.
Термодинамическая неравновесность таких систем обуславливает перекристаллизацию вещества
– рост крупных кристаллов впересыщенном растворе за счет растворения мелких. Например, для BaSO
4
найдено, что растворимость частиц сразмером r = 2 мкм равна 15,3 mмоль/л, арастворимость частиц
сразмером r = 0,3 мкм равна 18,2 mмоль/л. При подстановке этих данных вуравнение (12.19) найдем для
величины
т-ж
= 125010
-3
Дж/m
2.
Повышение давления насыщенного пара над высокодисперсными частицами по сравнению с
частицами крупных размеров обуславливает и некоторое понижение температуры их плавления. Например,
уменьшение размера частиц салола до 8 мкм понижает его температуру плавления с 42°С до 38°С.
12.7. Капиллярные явления
Особенности условий равновесия на искривленных поверхностях лежат в основе так называемых
капиллярных явлений. Если поверхность раздела фаз подвижна (поверхность жидкость-газ или жидкость-
жидкость), ее форма изменяется под влиянием поверхностного натяжения, стремясь к форме, отвечающей
минимальной поверхности. При смачивании жидкостью стенок капилляра в нем образуется вогнутый
мениск, и уменьшение давления под ним компенсируется подъемом жидкости в капилляре (всасывание).
При несмачивании образуется выпуклый мениск, и следствием является опускание жидкости в капилляре. С
описанным явлением связано также возникновение значительных перенасыщений при образовании новой
фазы. Вначале образуются зародышевые частицы весьма малых размеров. Давление пара (или
концентрация) раствора, равновесное по отношению к таким высокодисперсным агрегатам (кластерам),
заметно выше давления насыщенного пара (концентрации) насыщенного раствора. Таким образом, для
образования мелких зародышей необходимо накопление избыточной энергии, т.е. создания пересыщенных
состояний, что сильно тормозит образование новой фазы. Теория кинетики зародышеобразования
представляет собой одну из важных задач современной физической химии.
34
Лекция 13.
Адсорбция
13.1. Уравнение адсорбции Гиббса
Строгое определение понятия адсорбции по Дж.Гиббсу: адсорбцией данного компонента
награнице раздела двух фаз называется разность между фактическим количеством этого компонента
всистеме и тем его количеством, которое было бы всистеме, если бы концентрации вобеих
сосуществующих фазах были постоянны вплоть до некоторой геометрической поверхности, разделяющей
их.
Эта разность может быть положительной или отрицательной. Она обозначается символом
(гамма) и имеет размерность моль/м
2
. Эту величину называют избыточной адсорбцией по Дж.Гиббсу.
Хотя вприведенном определении адсорбция отнесена к геометрической поверхности, не
имеющей толщины (что удобно при выводе уравнений), фактически граница между фазами представляет
собой очень тонкий слой (поверхностный слой), вкотором все свойства отличаются от свойств объемных
фаз и изменяются не скачкообразно, анепрерывно.
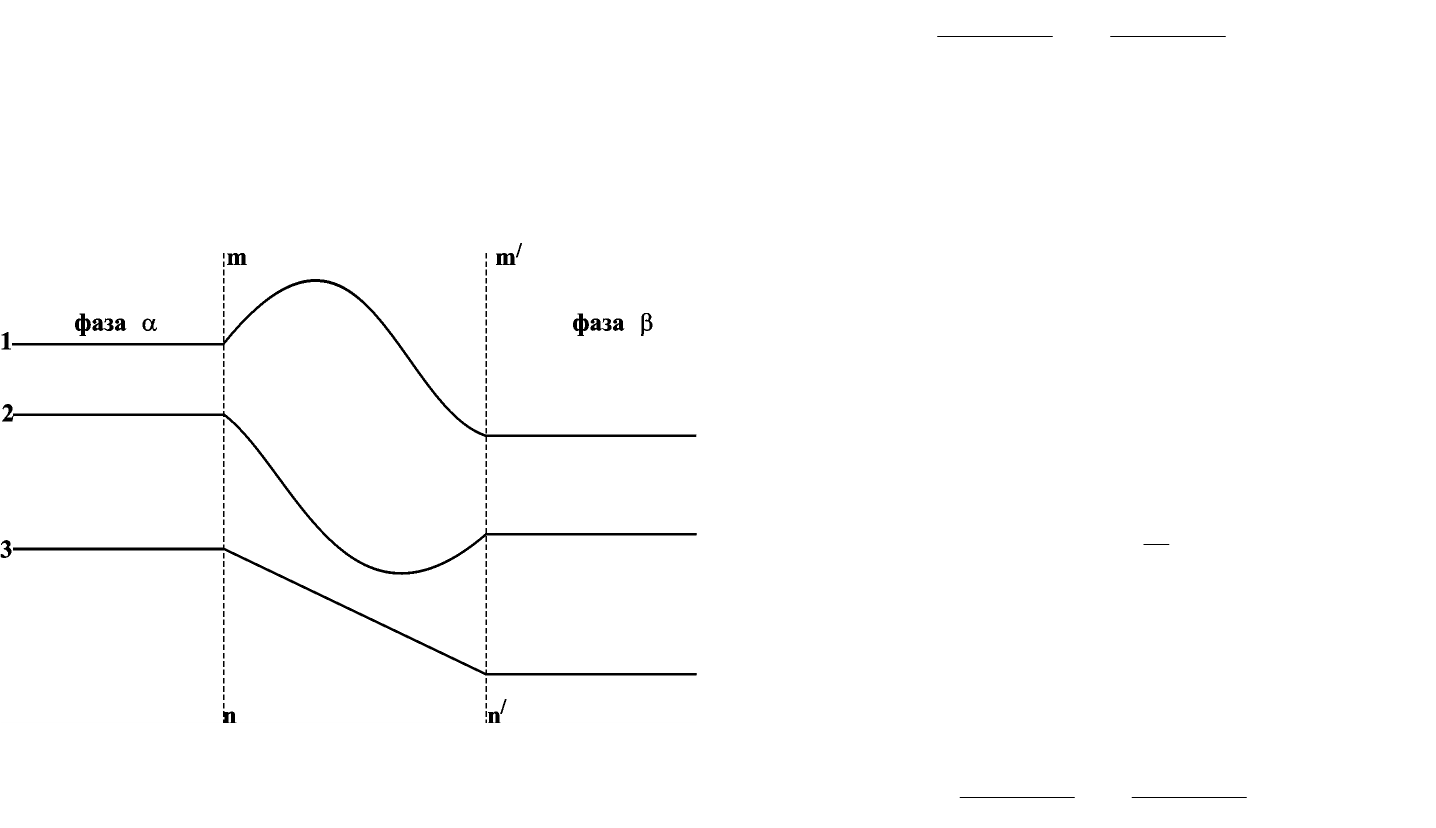
На рис. 13.1 показано возможное изменение концентрации вблизи границы раздела: концентрация
компонента может быть как выше концентраций вобеих фазах (1), так и ниже (2) или иметь промежуточное
значение. Эта область может рассматриваться как поверхностный слой. Таким образом, изучая границу
раздела фаз, нужно рассматривать состояние трех фаз: двух объемных и одной поверхностной.
Рис. 13.1. Изменение концентрации компонентов у границы раздела фаз;
поверхностный слой – mn-m’n’
Уравнение, устанавливающее связь между всеми параметрами процесса адсорбции – величиной
поверхностного натяжения
, концентрацией компонента [C] водной из фаз, его адсорбцией Г, было
выведено Дж.Гиббсом в1876г. Это уравнение является общим термодинамическим уравнением,
справедливым для любых составов и природы поверхности раздела фаз.
Рассмотрим систему, состоящую из двух компонентов 1 и 2 и двух фаз и , разделенных
поверхностью раздела сплощадью S. Общее число молей каждого компонента всистеме равно n
1
o
и n
2
o
.
Если считать, что поверхностный слой не имеет толщины, т.е. представляет собой геометрическую
поверхность, то обе объемные фазы будут иметь постоянный состав вплоть до этой геометрической
поверхности. Обозначим число молей каждого компонента вкаждой из этих фаз соответственно через n
1
,n
1
; n
2
,n
2
. Так как наповерхности имеет место адсорбция, то, очевидно, n
1
o
n
1
+ n
1
и n
2
o
n
2
+ n
2
.
По вышеприведенному определению адсорбция каждого компонента Г
1
и Г
2
, отнесенная к
единице площади поверхности, равна
S
nnn
S
nnn
22
0
2
2
11
0
1
1
;
. (13.1)
Чтобы найти Г
1
и Г
2
, напишем уравнение энергии Гиббса для двух фаз
и
вотдельности и для
всей системы вцелом. В последнем случае, очевидно, нужно включить вуравнение член
dS:
dG
= - S
dT + V
dP +
1
dn
1
+
2
dn
2
;
dG
= - S
dT + V
dP +
1
dn
1
+
2
dn
2
;
dG
o
= - S
o
dT + V
o
dP +
dS +
1
dn
1
o
+
2
dn
2
o
. (13.2)
Укажем науравнение Гиббса-Дюгема, которое устанавливает связь между химическими
потенциалами:
dG = - S dT + VdP +
i
dn
1
(P, T – постоянные). (13.3)
Тогда для бинарной системы получим
dG =
1
dn
1
+
2
dn
2
. (13.4)
Интегрируя это уравнение при постоянных значениях
1
и
2
,
получим
G =
1
n
1
+
2
n
2
. (13.5)
Следовательно,
dG =
1
dn
1
+
2
dn
2
+ n
1
d
1
+ n
2
d
2.
(13.6)
Из (13.4) и (13.6) вытекает, что
2
1
2
12211
;0
d
n
n
ddndn
. (13.7)
Это уравнение носит название уравнения Гиббса-Дюгема и связывает изменение химических
потенциалов компонентов. Тогда сучетом уравнения Гиббса-Дюгема и поверхностных явлений получаем:
n
1
d
1
+ n
2
d
2
= 0;
n
1
d
1
+ n
2
d
2
= 0; (13.8)
Sd
+n
1
o
d
1
+ n
2
o
d
2
= 0.
Сложение двух первых уравнений и вычитание полученной суммы из третьего дает
22112
22
0
2
1
11
0
1
ddd
S
nnn
d
S
nnn
d
. (13.9)
35

В качестве примера рассмотрим две конкретные системы: двухкомпонентный жидкий раствор,
находящийся вравновесии со своим двухкомпонентным насыщенным паром, и твердое тело, находящееся
вравновесии соднокомпонентным газом, совершенно не растворимым вэтом твердом теле.
Поскольку впервом случае точное положение разделяющей геометрической поверхности
несколько условно, то можно выбрать положение ее, при котором
Г
1
= 0,
тогда
d
= - Г
2
d
2
.
Во втором случае вследствие нерастворимости газа вобъеме твердого тела, объемные свойства
этого тела, вчастности его химический потенциал, не изменяются при адсорбции. Приписывая твердому
телу индекс 1, имеем:
1
= const и d
1
= 0,
поэтому
d
= - Г
2
d
2
.
В обоих случаях получено одно и то же уравнение. Поэтому можно считать, что адсорбционное
уравнение Гиббса имеет вид:
d
= Г
2
d
2
.
Оно является основным вучении о поверхностных явлениях.
Рассмотрим далее реальный раствор. Для реального раствора
=
о
(Т) + RTlna,
где а– активность, тогда:
d
= RТ d lna.
Подставив это значение вуравнение (13.12), получим:
d
= - Г RT d lna,
или
RTda
ad
.
В разбавленных растворах а С(где С – концентрация)
dC
d
RT
C
,
а для идеального или разреженного идеального газа
dP
d
RT
P
.
Уравнение (13.14) показывает, что если при адсорбции поверхностное натяжение
уменьшается
сростом концентрации С, т.е. d
/dC 0, то адсорбция Г – положительна. Это соответствует поверхностно-
активным веществам. Наоборот, если
растет сростом С, то d
/dC 0 и Г – отрицательно. Это
соответствует поверхностно-инактивным веществам. Если известна зависимость
от С(т.е. изотерма
поверхностного натяжения
= f(C) , то по уравнению Гиббса можно для каждого значения концентрации
найти d
/dC и по уравнению Гиббса вычислить значение Г, т.е. построить изотерму адсорбции.
13.2. Обзор сорбционных явлений
Адсорбция награнице раздела твердое тело/газ. В общем случае явления, связанные
сперераспределением веществ между различными частями гетерогенной системы, называются сорбцией.
Сорбция (от лат. sorbeo – сгущать) – это изменение концентрации (часто увеличение) либо у поверхности
раздела фаз (адсорбция), либо вобъеме одной из фаз (абсорбция). Например, образование раствора за счет
поглощения НСl (газа) и поглощение газа металлом (абсорбция). Поверхностная сорбция – адсорбция.
Твердое тело, у поверхности которого происходит адсорбция, называется адсорбентом,
адсорбирующийся газ или адсорбирующийся компонент жидкого раствора – адсорбтивом,
аадсорбированое вещество – адсорбат.
В строгом определении адсорбции она рассматривается как избыток вещества вблизи поверхности
по сравнению сравным объемом вдали от нее. В ряде случаев удобнее рассматривать не избыток, авсе
количество адсорбата вблизи поверхности. Это количество обозначают символом аи называют полным
содержанием, или просто адсорбцией (без указания гиббсова). Так как для пористых твердых тел бывает
затруднительно знать величину поверхности, то часто адсорбцию относят не к единице поверхности, а к
единице массы (моль/кг или моль/г).
Адсорбция самопроизвольна и протекает при Р = const со снижением энергии Гиббса, апри V =
const – со снижением энергии Гельмгольца. Однако при этом происходит не выравнивание концентраций по
всему объему системы, а увеличение разности концентраций между газовой фазой (раствором) и
поверхностью. Одновременно уменьшается подвижность сорбирующихся молекул. Оба фактора ведут к
уменьшению энтропии (S0).
По основному уравнению термодинамики находим
H = T
S +
G (13.16)
Если величины S и G – отрицательны, то значение Н – отрицательно и процесс является
экзотермическим.
Важной характеристикой адсорбции является теплота адсорбции. Она является мерой
интенсивности адсорбционных сил – сил взаимодействия молекул адсорбата споверхностью адсорбента и
между собой.
Интенсивность взаимодействия адсорбент-адсорбат зависит от состояния адсорбента и от
того, какое количество адсорбата уже адсорбировано (от заполнения поверхности). Поэтому различают
два основных понятия – интегральная и дифференциальная теплота адсорбции.
Интегральной теплотой адсорбции Q называется полное количество теплоты, выделяющейся
при адсорбции n молей адсорбата. Ее относят к единице массы адсорбента (Дж/кг). Дифференциальной
теплотой адсорбции q называют отнесенное к 1 молю адсорбата дополнительное количество теплоты,
выделяющейся при адсорбции бесконечно малого количества адсорбата:
da
dQ
q
или
2
1
a
a
qdaQ
. (13.17)
Типичные зависимости интегральной и дифференциальной теплоты адсорбции от количества
адсорбированного вещества представлены нарисунке 13.2. Прямые 1 для Q и 2 для q соответствуют
зависимости Q = ka. Как правило, такая прямая зависимость не наблюдается (она возможна лишь при q =
const). Фактически вследствие неоднородности поверхности адсорбента адсорбция происходит сначала
нанаиболее активных участках поверхности снаибольшим значением дифференциальной теплоты; при
больших заполнениях q уменьшается. Это приводит к некоторому замедлению роста Q. Возможен и третий
случай. Вследствие взаимного притяжения адсорбированных молекул уменьшается расстояние между ними
и дифференциальная теплота адсорбции повышается (кривая 3).
36
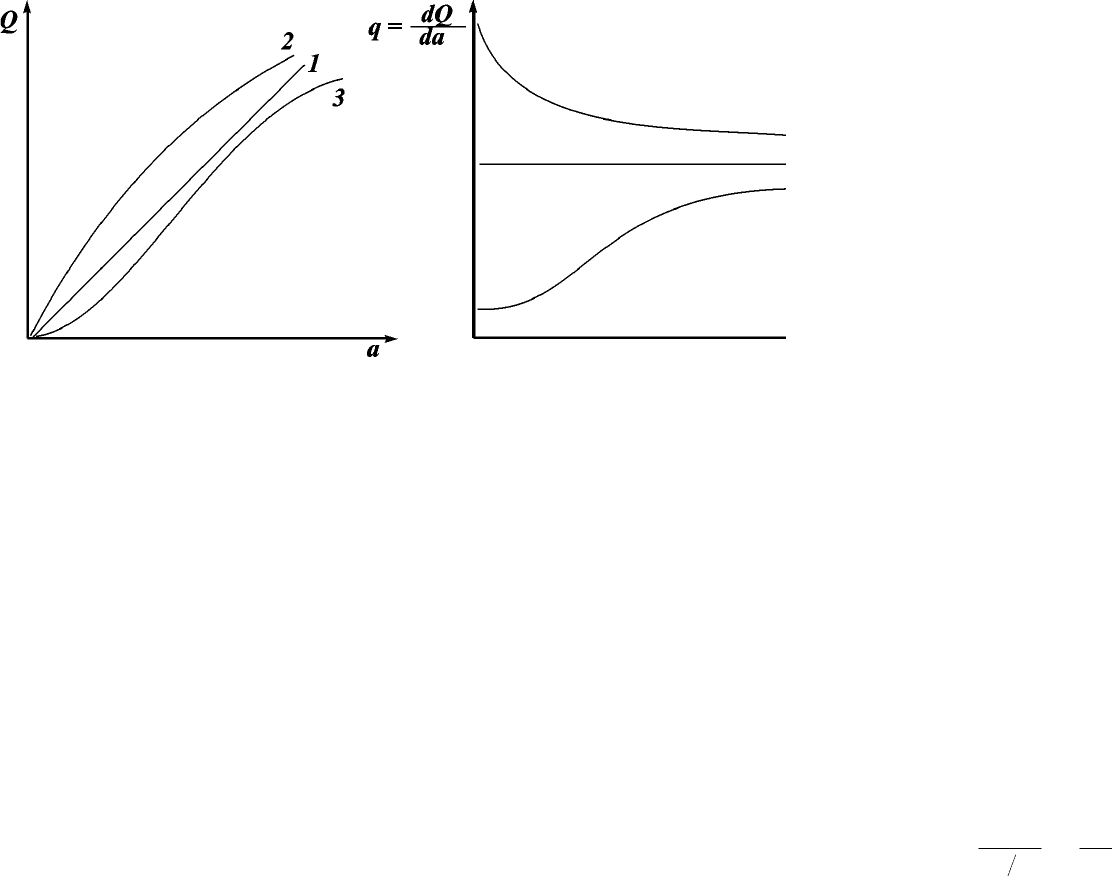
Рис. 13.2. Зависимость интегральной и дифференциальной теплоты адсорбции от количества
адсорбированного вещества
13.3. Природа адсорбционного взаимодействия
Величина адсорбции – функция природы адсорбента и адсорбата и зависит от силы
взаимодействия между ними. При адсорбции взаимодействуют молекулы, принадлежащие разным фазам,
анагранице раздела фаз неизбежно существует асимметрия сил взаимодействия. Кроме того, молекулы
адсорбата взаимодействуют не сединичной молекулой адсорбента, а сих совокупностью. Благодаря этому
силы взаимодействия взависимости от их природы могут либо возрастать, либо ослабевать.
Адсорбцию делят нафизическую и химическую (хемосорбцию). Как правило, физическая
адсорбция обусловлена межмолекулярными (ван-дер-ваальсовыми) силами. В простейшем случае
взаимодействие неспецифично, т.е. речь идет об универсальных, дисперсионных силах. Молекулы
наповерхности не теряют своей индивидуальности.
Дисперсионное взаимодействие не зависит от температуры. Важным свойством дисперсионных
сил является их аддитивность; сила взаимодействия между двумя молекулами не зависит от присутствия
других молекул. Аддитивность проявляется втом, что суммируются силы взаимодействия молекул
адсорбата со всеми близлежащими атомами поверхности адсорбента. Поэтому при адсорбции пористыми
адсорбентами вклад дисперсионных сил вобщее взаимодействие оказывается существенно бóльшим. При
адсорбции неполярных веществ наполярном адсорбенте (ионный кристалл) к дисперсионным силам
притяжения добавляются индукционные силы притяжения диполя, индуцированного электростатическим
полем адсорбента. Индукционное притяжение возникает и при адсорбции полярных молекул нанеполярном
адсорбенте.
Адсорбция полярных молекул наполярном адсорбенте вызывает ориентационное кулоновское
взаимодействие диполя адсорбата с электростатическим полем адсорбента. Энергия индукционных,
ориентационных и дисперсионных сил при парном взаимодействии обратно пропорциональна шестой
степени расстояния между центрами взаимодействующих атомов. Однако ориентационные и индукционные
взаимодействия, будучи электростатическими, не являются аддитивными. Так, появление третьей молекулы
вполе взаимодействия двух других изменяет ориентацию молекулы и ослабляет эти взаимодействия.
Поэтому энергия взаимодействия молекулы адсорбата споверхностью адсорбента может оказаться меньше,
чем энергия ее взаимодействия содним центром наповерхности. При адсорбции пористыми адсорбентами
индукционное и ориентационное взаимодействия вносят меньший вклад. Поэтому наибольшую роль чаще
всего играет дисперсионное взаимодействие. Для неполярных или слабополярных молекул его вклад может
быть стопроцентным.
Неспецифический характер взаимодействий, вызывающих физическую адсорбцию, определяет и
основные признаки этого явления. Равновесие при физической адсорбции устанавливается быстро и
обратимо. Теплота физической адсорбции превышает теплоту конденсации обычно не более чем
на~20кДж/моль.
Химическая адсорбция имеет место, когда молекулы адсорбата вступают вхимическое
взаимодействие споверхностью адсорбента собразованием
поверхностных химических соединений, но без образования новой объемной
фазы. Она гораздо более избирательна и чувствительна к химической природе адсорбата и адсорбента.
Теплоты хемосорбции обычно велики (100-200кДжмоль).
Хемосорбция может протекать довольно медленно, со скоростью, определяемой наличием
некоторого активационного барьера. Поэтому ее часто называют «активированная адсорбция». При низких
температурах скорость хемосорбции обычно мала. Хемосорбция, как правило, необратима.
Существует большое многообразие форм адсорбции, переходных между физической и
химической адсорбцией. Так, например, широко распространенным видом такого переходного
взаимодействия является образование водородной связи при адсорбции. Это характерно для адсорбентов,
содержащих наповерхности гидроксильные группы (силикагель, алюмогель и др.). Для этого пограничного
типа адсорбции теплота составляет обычно 20-40 кДж/моль.
В связи сразнообразием адсорбционных сил единая теория адсорбции, позволяющая наоснове
предположений о механизме процесса составить общее математическое описание, пока отсутствует.
13.4. Термическое уравнение адсорбции.
Изотерма адсорбции
Для данной пары адсорбент – адсорбат величина адсорбции аили Г определяется двумя
основными термодинамическими параметрами состояния: температурой Т и давлением Р для газообразного
состояния адсорбата или Т и концентрацией Спри адсорбции из растворов. Все три величины связаны
функциональной зависимостью, называемой термическим уравнением обратимой сорбции:
f = (a,Р,T) = 0 или
= (Г,С,Т) = 0. (13.18)
В теории адсорбции особенно часто рассматривают адсорбционное равновесие при условии, что
один из параметров, входящих втермическое уравнение, поддерживается постоянным. Например, а= f(P)
Т
или Г =
(С)
Т
. Адсорбия, если она выражена не как избыток, акак полное содержание, всегда возрастает
сповышением равновесного давления (концентраци). Так как адсорбция – процесс экзотермический, то при
повышении температуры величина адсорбции снижается.
Уравнение, связывающее величину адсорбции стемпературой при постоянном равновесном
давлении а= f(T)
P
или постоянной равновесной концентрации Г =
(Т)
С
, носит название соответственно
изобары или изопикны адсорбции. Уравнение вида Р = f(Т)
а
(изостера адсорбции) связывает равновесное
давление стемпературой при постоянном адсорбированном количестве.
Переход вещества из газовой фазы вадсорбированное состояние визвестном смысле аналогичен
фазовому переходу пар-жидкость. Поэтому для такого перехода может быть выведена формула, аналогичная
формуле Клаузиуса-Клапейрона. Однако вэтом случае вформулу входит частная производная давления по
температуре при постоянном значении адсорбции (Р/Т)
a
:
R
q
T
P
st
1
ln
, (13.19)
где q
st
– изостерическая теплота адсорбции, которая очень близка к выведенной ранее дифференциальной
теплоте.
Для математического описания адсорбции необходимо уравнение, которое связывает зависимость
равновесной величины адсорбции от концентрации адсорбата вобъемной фазе при различных температурах,
атакже правильно предсказывает изменение теплоты адсорбции от заполнения адсорбента.
Однако форма изотермы адсорбции натвердых телах зависит от многих параметров: свойств
адсорбента и адсорбата, взаимодействия адсорбтив/адсорбат, взаимодействия молекул адсорбата между
37
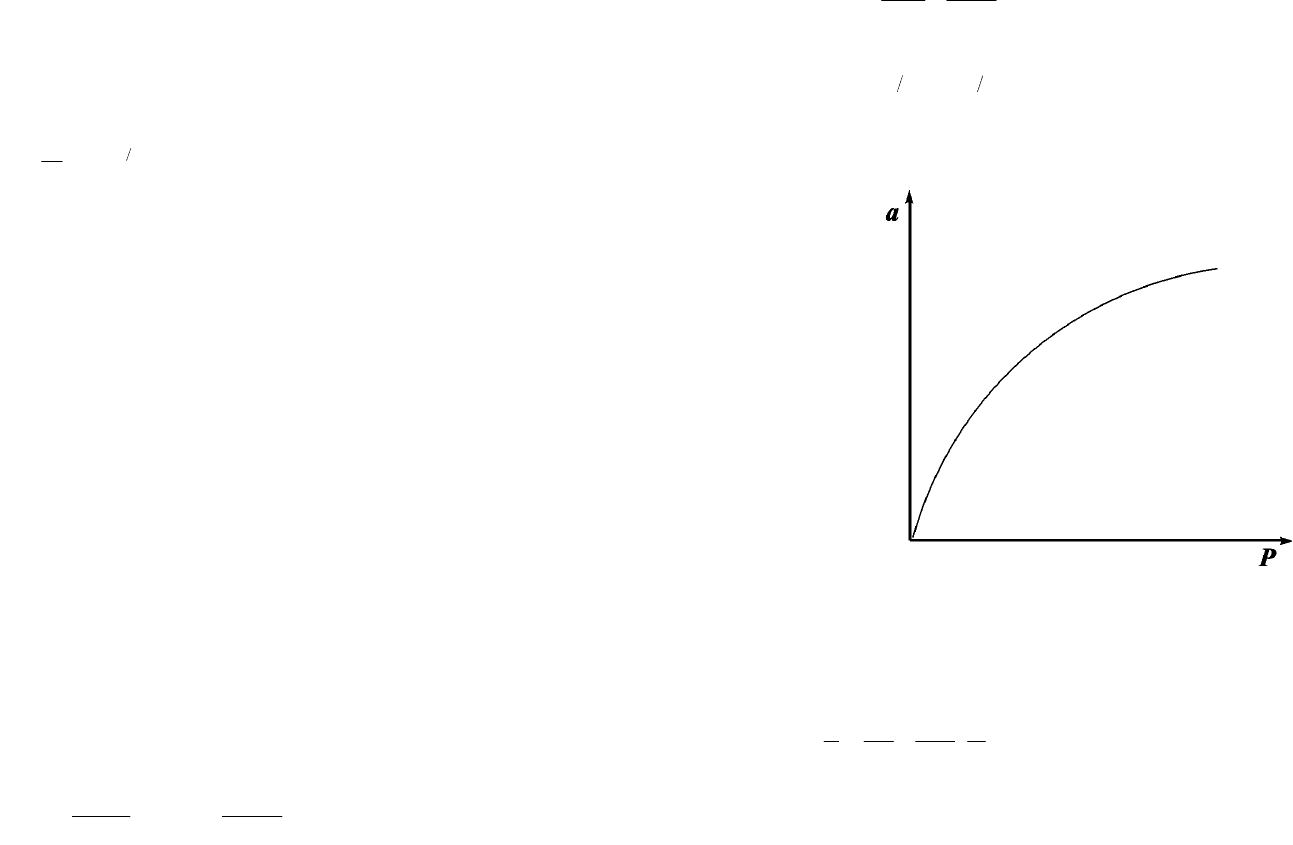
собой вгазовой фазе и вадсорбированном состоянии. В области малых давлений (концентраций) и малых
заполнений поверхности взаимодействия между молекулами адсорбата незначительны и зависимость а=
f(P)
T
сводится к простейшей форме, называемой законом Генри:
аp= kP или аp= kC.
Коэффициент пропорциональности k – коэффициент Генри – является мерой интенсивности
адсорбции. При больших давлениях (концентрациях) и больших заполнениях адсорбцию часто выражают
эмпирическим уравнением Фрейндлиха
n
C
m
x
a
1
,
где х – количество адсорбированного вещества, m – масса адсорбента,
и n – константы, характерные для
каждой адсорбционной системы. Причем 1/n всегда правильная дробь (0 1/n 1). По Г. Фрейндлиху, n не
зависит от заполнения, хотя это не вполне точно. Этим уравнением часто пользуются для ориентировочной
оценки адсорбции.
13.5. Мономолекулярная адсорбция и изотерма
Ленгмюра
Первое теоретическое уравнение изотермы адсорбции было предложено И.Ленгмюром в 1914
году. Теория Ленгмюра основана на трех основных положениях:
Адсорбция происходит надискретных адсорбционных центрах, которые могут иметь различную
природу.
При адсорбции соблюдается строгое стехиометрическое условие – наодном центре адсорбируется
одна молекула.
Адсорбционные центры энергетически однородны и независимы, т.е. адсорбция наодном центре
не влияет наадсорбцию надругих центрах.
На основании этих положений скорость адсорбции V
aдc
пропорциональна давлению газа и числу
свободных центров. Если общее число центров а
m
, то при адсорбции, равной а, число свободных центров
равно (а
m
– а).
Поэтому
V
aдc
= k
aдc
P
(a
m
– a).
Наряду садсорбцией идет процесс десорбции:
V
дес.
= k
дес.
а.
При равновесии V
aдc
= V
дес
или
k
aдc
P
(a
m
– a) = k
дес.
а.p
Обозначим k
дес.
/ k
адс.
= b, аа/а
m
= Q, где Q – относительное заполнение поверхности, получим:
bP
bP
aa
m
1
или
bP
bP
Q
1
.
Это уравнение изотермы адсорбции называется уравнением Ленгмюра. Константа b носит
название константы адсорбционного равновесия, или адсорбционного коэффициента.
Константа равновесия связана со стандартными изменениями энергии Гиббса. Если
RTlnb = –
G
o
, так как
G
o
=
H
o
+ T
S
o
,
то
RT
H
R
S
b
00
ln
. (13.26)
Следовательно
RTHRS
eeb
00
. (13.27)
Таким образом, адсорбционный коэффициент b связан со стантартной энтропией S° и со
стандартной теплотой адсорбции q = –H°.
Очень часто а
m
называют «емкость монослоя». Нарис.13.3 показана кривая, выражающая
изотерму адсорбции по Ленгмюру
Рис. 13.3. Изотерма адсорбции по Ленгмюру
При очень малых заполнениях и, следовательно, очень малых давлениях Р взнаменателе,
согласно (13.25), bР 1. Поэтому вэтой области а= а
m
bP, т.е. переходит вуравнение Генри. При очень
высоких давлениях bP 1 и а= а
m
, т.е. величина адсорбции перестает зависеть от давления, поскольку все
центры уже заняты.
Для расчета параметров a
m
и b уравнение Ленгмюра представляют ввиде
Pbaaa
mm
1111
. (13.28)
Тангенс угла наклона этой линии равен 1/a
m
b, аотрезок, отсекаемый наоси ординат, равен 1/a
m
.
Уравнение Ленгмюра, полученное на основании модели локализованной адсорбции газов на
поверхности твердого тела, часто хорошо описывает адсорбцию растворенных веществ на поверхности
жидкости (поверхность раздела раствор/газ), при которой адсорбция не локализована, так как молекулы
подвижны и образуют двумерную газо- или жидкообразную пленку.
Обусловлено это тем, что основные положения модели Ленгмюра соблюдаются при адсорбции из
растворов: поверхность жидкости идеально однородна, взаимодействие адсорбированных молекул
вадсорбционном слое мало отличается от их взаимодействия врастворе. Оно к тому же ослаблено за счет
взаимодействия молекул растворенного вещества смолекулами растворителя и практически не влияет
наадсорбцию.
38
Уравнение Ленгмюра связано суравнением состояния адсорбционной пленки – уравнением
Гиббса. Так,
dC
d
RT
C
,
а по уравнению Ленгмюра
bC
bdC
RT
1
;
тогда
bC
bC
RT
C
dC
d
1
или
bC
bdC
RTd
1
.
После интегрирования впределах от
о
до
и от 0 до С получим:
bCRT
1ln
0
,
и, наконец,
bCRT
1ln
0
,
где Г
связано с площадью, занимаемой 1 моль адсорбированного вещества вмономолекулярном слое,
следующим соотношением:
1
S
.
39
Содержание
Введение.............................................................................................................................................................................................................................
Лекция 1. Газовые законы..............................................................................................................................................................................................
1.1. Температура и нулевой закон термодинамики...........................................................................................................................................
1.2. Законы поведения идеальных газов: уравнение состояния идеального газа...........................................................................................
1.3. Кинетическое уравнение газов...................................................................................................................................................................
1.4. Уравнение состояния реальных (неидеальных) газов. Уравнение Ван-дер-Ваальса............................................................................
1.5. Закон парциальных давлений Дальтона....................................................................................................................................................
Лекция 2. Первое начало термодинамики и термохимия......................................................................................................................................
2.1. Вводная часть...............................................................................................................................................................................................
2.2. Некоторые понятия, используемые в термодинамике.............................................................................................................................
2.3. Формулировка первого начала термодинамики.......................................................................................................................................
2.4. Применение первого начала термодинамики к различным процессам..................................................................................................
2.5. Теплота химической реакции (общие положения)...................................................................................................................................
2.6. Закон Гесса...................................................................................................................................................................................................
2.7. Следствие из закона Гесса...........................................................................................................................................................................
Лекция 3. Второе начало термодинамики и его применение................................................................................................................................
3.1.Основной смысл и значение второго закона термодинамики.................................................................................................................
3.2. Обратимые и необратимые процессы........................................................................................................................................................
3.3. Формулировка и математическое выражение второго начала термодинамики....................................................................................
3.4. Изменение энтропии изолированной системы..........................................................................................................................................
3.5. Статистическая природа второго начала термодинамики.......................................................................................................................
Лекция 4. Третье начало термодинамики. Расчеты изменения энтропии при различных процессах.........................................................
4.1. Формулировка третьего начала термодинамики......................................................................................................................................
4.2. Абсолютные и стандартные значения энтропии......................................................................................................................................
4.3. Расчеты изменения энтропии в различных процессах.............................................................................................................................
4.4. Расчет изменения энтропии при протекании химического процесса.....................................................................................................
4.5. Критерии направления протекания процессов и достижения равновесных состояний воткрытых
и закрытых системах. Понятие об энергии Гиббса.........................................................................................................................................
Лекция 5. Химические реакции как открытые в термодинамическом смысле системы. Направление
протекания химических реакций. Равновесные химические реакции...............................................................................................................
5.1. Понятие о химическом потенциале............................................................................................................................................................
5.2. Экзергонические и эндергонические реакции..........................................................................................................................................
5.3. Взаимосвязь энтальпийного и энтропийного факторов в качестве критерия самопроизвольного
протекания химической реакции.......................................................................................................................................................................
5.4. Понятие о равновесии химической реакции. Обратимые и необратимые реакции..............................................................................
5.5. Уравнение изотермы химической реакции и вывод закона действующих масс...................................................................................
5.6. Зависимость константы химического равновесия от температуры........................................................................................................
Лекция 6. Химическое равновесие в гетерогенных и гомогенных
системах............................................................................................................................................................................................................................
6.1. Взаимосвязь химического потенциала с другими термодинамическими функциями..........................................................................
6.2. Летучесть......................................................................................................................................................................................................
6.3. Идеальный раствор......................................................................................................................................................................................
6.4. Фазовая диаграмма содержит зоны, линии и тройную точку.................................................................................................................
6.5. Уравнение Клаузиуса-Клапейрона.............................................................................................................................................................
6.6. Коллигативные свойства растворов...........................................................................................................................................................
6.7. Понижение точки замерзания и повышение точки кипения растворов.................................................................................................
6.8. Осмотическое давление...............................................................................................................................................................................
6.9. Растворы электролитов................................................................................................................................................................................
Лекция 7. Растворы электролитов..............................................................................................................................................................................
7.1. Общие сведения о теории электролитической диссоциации...................................................................................................................
7.2. Сильные и слабые электролиты..................................................................................................................................................................
7.3. Закон разведения..........................................................................................................................................................................................
7.4. Сильные электролиты..................................................................................................................................................................................
7.5. Ионная сила..................................................................................................................................................................................................
7.6. Произведение растворимости.....................................................................................................................................................................
7.7. Электролитическая диссоциация воды......................................................................................................................................................
7.8. Концентрация водородных ионов..............................................................................................................................................................
7.9. Буферные растворы......................................................................................................................................................................................
7.10. Механизм действия буферных растворов................................................................................................................................................
7.11. Буферная емкость.......................................................................................................................................................................................
Лекция 9. Основы кинетики и механизма ферментативных реакций. Гомогенный и гетерогенный
катализ..............................................................................................................................................................................................................................
9.1. Понятие катализа.........................................................................................................................................................................................
9.2. Основы теории гомогенного катализа.......................................................................................................................................................
9.3. Основы теории гетерогенного катализа.....................................................................................................................................................
9.4. Ферменты как биологические катализаторы.............................................................................................................................................
9.5. Кинетика реакций, катализируемых ферментами....................................................................................................................................
9.6. Физический смысл величин K
m
и V
max
........................................................................................................................................................
9.7. Уравнение Михаэлиса-Ментен и ферментативные механизмы..............................................................................................................
9.8. Общее уравнение скорости.........................................................................................................................................................................
Лекция 10. Электрохимия.............................................................................................................................................................................................
10.1. Введение в электрохимию.........................................................................................................................................................................
10.2. Термодинамика электрохимических систем.........................................................................................................................................
10.3. Электродный потенциал..........................................................................................................................................................................
10.4. Двойной электрический слой на границе между металлом и раствором электролита.....................................................................
10.5. Зависимость плотности заряда от концентрации электролита............................................................................................................
Лекция 11. Электродные и безэлектродные электрохимические
системы...........................................................................................................................................................................................................................
11.1. Правила записи ЭДС и электродных потенциалов электрохимических систем...............................................................................
11.2. Типы электродов......................................................................................................................................................................................
11.3. Диффузионный и межжидкостный потенциалы...................................................................................................................................
11.4. Электрохимические системы с химической реакцией (химические цепи)........................................................................................
11.5. Концентрационные цепи.........................................................................................................................................................................
Лекция 12. Поверхностные явления и адсорбция..................................................................................................................................................
12.1. Общая характеристика поверхностных явлений..................................................................................................................................
12.2. Поверхностные явления вдисперсных системах.................................................................................................................................
12.3. Поверхностное натяжение и природа вещества....................................................................................................................................
12.4. Термодинамика поверхностных явлений воднокомпонентных системах........................................................................................
12.5. Равновесие фаз при искривленной поверхности раздела. Капиллярность........................................................................................
12.6. Уравнение Томсона..................................................................................................................................................................................
12.7. Капиллярные явления..............................................................................................................................................................................
Лекция 13. Адсорбция..................................................................................................................................................................................................
13.1. Уравнение адсорбции Гиббса.................................................................................................................................................................
13.2. Обзор сорбционных явлений..................................................................................................................................................................
13.3. Природа адсорбционного взаимодействия............................................................................................................................................
13.4. Термическое уравнение адсорбции. Изотерма адсорбции...................................................................................................................
13.5. Мономолекулярная адсорбция и изотерма Ленгмюра.........................................................................................................................
Литература.......................................................................................................................................................................................................................
40
