Лунин Л.С., Благин А.В., Баранник А.А. Лекции по физике. Часть I. Механика, молекулярная физика и термодинамика
Подождите немного. Документ загружается.

171
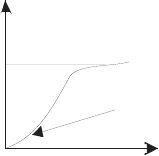
Во-первых, классическая теория теплоемкости вещества не дает за-
висимости теплоемкости от температуры, что наглядно проявляется в опы-
тах, особенно при низких температурах (рис. 15.1). Во-вторых, классиче-
ская теория теплоемкости принимает атом за материальную точку, обла-
дающую тремя степенями свободы, хотя его строго следует рассматривать
С
V
T
R
~T
3
Рис. 15.1
как ТТ, т.е. атом обладает шестью степенями свободы. При этом необхо-
димо учитывать, что при разных температурах эффективный вклад
всех степеней свободы в теплоемкость будет различным. При понижении
температуры некоторые степени свободы дают малый вклад, как бы «за-
мораживаются». С учетом этого закон равномерного распределения энер-
гии по степеням свободы требует уточнения. Внутренняя энергия молекул
может принимать лишь определенные, строго фиксированные – дискрет-
ные – значения. Например, атом при низких температурах, сколь угодно
близких к нулю Кельвина, обладает, в основном, колебательными степе-
нями свободы. Самый низкий из энергетических уровней, соответствую-
щих такому состоянию молекул, называют нулевым. Далее с повышением
температуры активизируется вращение молекул, и при высоких темпера-
турах становится справедлив закон равномерного распределения энергии
по степеням свободы.
В металлах концентрация носителей тока – электронов достаточно
велика, они слабо связаны с атомами, поэтому часто оперируют понятием
«электронного газа» в металлах. Следует отметить, что о ситуации с теп-
лоемкостью металлов долгое время говорили, как о «катастрофе с тепло-
емкостью». Это связано с тем, что помимо атомов, находящихся в узлах
кристаллической решетки, вклад в теплоемкость должны давать и носите-
ли тока. Этот вклад также дискретен, становится значительным по сравне-
нию с вкладом решетки (ионов в узлах) лишь при низких температурах.
Все вышеперечисленные факторы были учтены в новой – квантовой
теории строения вещества. К этому вопросу мы еще вернемся в третьей,
последней части курса физики.
172
15.2. Фаза. Метастабильные состояния. Диаграммы
состояния. Тройные точки. Фазовые переходы (ФП) I и II
рода.
Явление сверхтекучести (ФП II рода)
Под фазой в термодинамике понимают
равновесное состояние ве-
щества, отличающееся по своим физическим свойствам (строение, тепло-
емкость, электропроводность и т.п.) от других равновесных состояний
(других фаз) этого же вещества.
Переход вещества из одной фазы в дру-
гую (фазовый переход)
связан с качественным изменением свойств веще-
ства, например, кристаллизация расплава (жидкости). При этом, как отме-
чалось выше, может образоваться не только монокристалл (фаза), но и по-
ликристалл (также является фазой), а также аморфное ТТ (так называемая
неустойчивая – метастабильная фаза). Ясно, что
вещество, находясь в од-
ном и том же агрегатном состоянии (ТТ), может быть представлено
сразу в виде нескольких фаз
.
Любая химическая система, состоящая из некоторого числа компо-
нентов, имеет определенное число степеней свободы. В отличие от степе-
ней свободы, в молекулярной физике, химической термодинамике
под
степенями свободы понимают набор тех физических параметров, изме-
нение которых в определенном интервале не приводит к изменению фазо-
вого состава системы
. Количество степеней свободы, которыми облада-
ет многофазная система, определяется
согласно следствию из правила
фаз Гиббса
:
nfkс
+
−
=
, (15.3)
где
с – число степеней свободы; k – число независимых компонентов; f –
число фаз в данной системе;
n – число физических условий, определяющих
состояние системы (обычно
n=2 – P и Т).
В точках, где число степеней свободы оказывается отрицательным,
система является термодинамически неустойчивой.
Переход вещества из одного агрегатного состояния в другое или из одной
фазы в другую удобно описывать с помощью графического изображения –
фазовой диаграммы
, или диаграммы состояния, диаграммы равновесия,
дающей соотношение между параметрами состояния физико-химической
системы (температурой
Т, давлением Р и др.) и её составом Х. В общем
случае, когда система состоит из одного компонента, это изображение
трехмерное, но поскольку многие процессы часто протекают при постоян-
ном значении одного из параметров, то используют сечения трехмерного
изображения соответствующей постоянному параметру плоскости. На-
пример, при постоянном давлении используют сечение
Т–Х – диаграмму
Т–Х. Аналогичными соображениями обосновывается применение диа-
грамм
Р–Х и P–Т.

173
Пример P–Т диаграммы состояния однофазной системы – углекисло-
го газа
СО
2
, изучением состояния которого занимался Т.Эндрюс еще в
XIX в. (см. лекция 13, вопрос 1), приведен на рис. 15.2, где
К – точка без-
вариантности
(нонвариантности), и, согласно формуле (15.3), с=0, или
тройная точка
, в которой сосуществуют все три агрегатных состояния –
жидкое, твердое и газообразное.
Диаграмма имеет простейший вид (рис.15.2), если однокомпонентная сис-
тема характеризуется наличием только одной кристаллической (ТТ), жид-
кой и газообразной (парообразной) фазы (только в этом случае смысл по-
нятия «агрегатное состояние» и понятия «фаза» совпадают).Если же веще-
ство в одном из агрегатных состояний, например, кристаллическом, при из-
менении условий меняет свое строение (сингонию), другие свойства (харак-
теризуется несколькими фазами), то диаграмма состояния (рис.15.2) ус-
ложняется, появляется несколько критических точек – точек безвариантно-
сти.
Газ ()gas
(solid)
ТТ
(liquid)
Жид кость
K
P
T
T<0
кр
=-58,6 С°
P
кр
=534996 Па
Рис. 15.2
Пример
Т–Х диаграммы состояния двухкомпонентной системы с
неограниченной взаимной растворимостью приведен на рис. 15.3.
Рис. 15.3
174
Неограниченной растворимостью друг в друге (с образованием
полностью гомогенной – однородной среды) обладают обычно вещества
со сходными физико-химическими свойствами, например, располагаю-
щиеся в одной подгруппе Периодической таблицы Д.И. Менделеева
(золото
Au и серебро Ag).
Следует отметить тот факт, что при кристаллизации системы без особых
технических приспособлений (например, организации подпитки по како-
му-то из компонентов), в общем случае изменяется ее состав, т.е. следует
рассматривать динамическое равновесие в системе.
Ликвидусом
(от лат. liquidus – жидкий) системы называется кривая,
вдоль которой происходит полное плавление кристаллов данного вещества
с ростом температуры или начало их равновесной кристаллизации.
Солидусом (от лат. solidus – плотный, твердый) системы называется
кривая, вдоль которой происходит полная кристаллизация сплава (или
твердого раствора) или начало их равновесного плавления.
Между солидусом и ликвидусом находятся в равновесии обе фазы
(расплав и ТТ).
Если же растворение веществ друг в друге неполное или процесс
идет с образованием различных химических соединений и их модифика-
ций (по строению и прочим физико-химическим свойствам, но одинаково-
го агрегатного состояния –
,...,,
γ
β
α
), то диаграмма состояния может зна-
чительно усложняться. Естественно, диаграмма состояния усложняется и при
увеличении компонентов в системе. В этом случае она будет уже не трехмер-
ной, как в случае одного компонента, а
n-мерной, где n – число компонентов;
при этом рассматриваются вышеназванные сечения по каждому из компонен-
тов и зависимости их содержания в жидкой и твердой фазах от концентрации
других компонентов. Последние зависимости для многокомпонентных систем
получить, как правило, очень трудно из-за совместного многофакторного
влияния других компонентов с учетом изменения этого влияния при измене-
нии условий проведения технологических процессов.
Переход вещества из одной фазы в другую – фазовый переход –
всегда связан с качественными изменениями свойств вещества. При-
мерами фазовых переходов могут служить не только плавление, кристал-
лизация, испарение, т.е. изменения агрегатного состояния вещества, но и
переходы, связанные с изменениями в составе, строении и свойствах веще-
ства, например, изменение модификации кристаллического вещества (сме-
на сингонии и, следовательно, изменение свойств).
При фазовых переходах I рода скачкообразно изменяются плот-
ность, объем, концентрация, энтропия (увеличение беспорядка) и выделя-
ется или поглощается теплота –
теплота фазового перехода. Например,
при плавлении вещества должна быть затрачена энергия на разрыв связей
атомов в кристаллической решетке, а при кристаллизации, при образова-
нии этих связей излишек энергии выделяется.
175
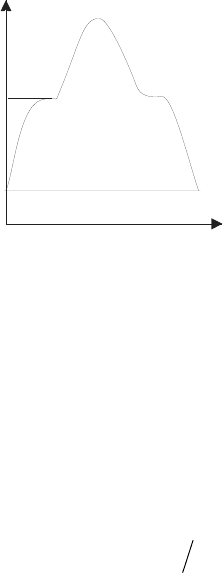
При медленном нагревании вещества выше температуры плавления
и его дальнейшем охлаждении, на графике зависимости изменения темпе-
ратуры от времени
T=f(t) появляются горизонтальные участки (рис. 15.4),
т.е. температура в системе остается в течение некоторого времени посто-
янной, хотя извне (нагревательная спираль) теплота системе сообщается.
Зависимость вида, приведённого на рис.15.4, называется
темпера-
турно-временным режимом
(ТВР).
T
t
T
пл
T
0
0
Рис. 15.4
Следует отметить, что при увеличении масштаба изображения реаль-
ных ТВР их линии будут выглядеть волнообразными, так как при проведении
технологического процесса поддержание постоянства температуры всегда
проводится с конечной точностью, в пределах которой возможны флуктуа-
ции температурного поля, а, следовательно (см. фазовые диаграммы), суще-
ственное изменение состава и свойств получаемых материалов. Поэтому при
проведении технологических процессов требуется четко выдерживать
температуру, скорость (это производная
dtdT – угол наклона кривой к
оси времени) и время (моменты) ее изменения.
К фазовым переходам I рода относятся изменение агрегатного состояния
(плавление и кристаллизация, испарение и конденсация, сублимация и обрат-
ный ей переход из газовой фазы в ТТ), переход вещества из одной кристалличе-
ской модификации в другую, переход из нормального в сверхпроводящее со-
стояние под действием сильного магнитного поля.
Выделение теплоты фазо-
вого перехода – характерный признак фазового перехода I рода.
При фазовых переходах II рода
не происходит поглощения или вы-
деления теплоты, плотность изменяется непрерывно, скачкообразно изме-
няются теплоемкость, вязкость, электропроводность, коэффициент тепло-
вого расширения (КТР). Примерами фазовых переходов II рода могут слу-
жить переходы веществ в сверхпроводящее и сверхтекучее состояния при
низких температурах, переход вещества из ферромагнитного в парамаг-
нитное состояние при нагреве до определенной температуры (температура
перехода – температура Кюри).
В квантовой теории явления сверхпро-
водимости и сверхтекучести объясняются с единой точки зрения, по-
казывается их общность
.
176
Сверхтекучесть – состояние жидкости, в котором она протекает че-
рез узкие щели и капилляры без трения. Единственным представителем
семейства сверхтекучих жидкостей долгое время считался жидкий гелий
4
Не, становящийся сверхтекучим ниже температуры Т=2,17 К. Сверхтеку-
чее состояние гелия назвали
Не–II, в отличие от обычного Не–I. Сверхте-
кучесть
Не–II была открыта П.Л.Капицей (р.1894г.) в 1938г.
При рассмотрении вопроса об ограниченности классической теории
теплопроводности говорилось о том, что при температурах сколь угодно
близких к нулю Кельвина в веществе продолжается движение – т.н. нуле-
вые колебания атомов и молекул (в квантовой теории показывается, что
энергия тепловых возбуждений может представляться в виде суммы энер-
гий
ω
h
особых квантов – фононов (h – постоянная Планка,
ω
– циклическая
частота колебаний)). Сверхтекучесть
Не–II была объяснена Л.Д.Ландау в 1941
г. в его квантовой теории двухжидкостной гидродинамики. Согласно этой тео-
рии
Не–II можно представить состоящим из двух взаимопроникающих компо-
нент: нормальной и сверхтекучей. В нормальной составляющей жидкого гелия
возможно возбуждение тепловых колебаний, с наличием которых связано су-
ществование внутреннего трения – вязкости. В сверхпроводящей же состав-
ляющей до температуры
Т=2,17 К эти колебания не возникают, при этом час-
тицы
Не–II представляют так называемый конденсат – коллектив сильно взаи-
модействующих между собой частиц.
ЛЕКЦИЯ 16. РАСТВОРЫ
1. Растворы (общие сведения).
2. Осмос и осмотическое давление. Закон Рауля.
3. Многокомпонентные твердые растворы (МТР). Применение МТР
16.1. Растворы (общие сведения)
Растворами
называют физически однородные (гомогенные) смеси
двух или нескольких веществ. Физическая однородность достигается рав-
номерным перемешиванием молекул, чем раствор отличается от механиче-
ских смесей, в которых перемешаны не молекулы, а макроскопические
частицы вещества. От химических соединений растворы отличаются тем,
что состав раствора может изменяться в широких пределах, а вещества в
химические соединения вступают в строго определенных пропорциях.
Раствор нельзя считать просто механической смесью молекул, так как
при смешивании вещества взаимодействуют между собой с рядом эффек-
тов: изменяется суммарный объем (спирт + вода), выделяется или погло-
щается теплота, образуются сольваты (непрочные соединения непостоян-
ного состава молекул компонентов раствора, если растворитель – вода, то
сольваты называют гидратами) и т.д.
177
Раствор состоит из растворителя и растворенных веществ. Раство-
рителем
считается вещество, которое до растворения находилось в том же
агрегатном состоянии, что и после растворения (вода+сахар, растворитель
– вода). Если же компоненты раствора до и после растворения находятся в
одинаковом агрегатном состоянии (вода+спирт), то растворителем счита-
ется компонент, присутствующий в большем количестве.
Растворы называются
слабыми или разбавленными, если число
молекул растворенных веществ очень мало по сравнению с числом моле-
кул растворителя, в противном случае растворы называются
крепкими.
Очень крепкие растворы называются
концентрированными. Раствор, на-
ходящийся в динамическом равновесии с растворяющимся веществом, на-
зывается
насыщенным (растворение – процесс двухстороннего перехода:
молекул из растворяемого вещества в раствор и обратно).
Относительное содержание компонентов в растворе характеризуется
их концентрациями. Различают
массовые (массовая доля), мольные
(мольная доля),
молярные (молярность), объемные концентрации.
Массовая доля есть отношение массы данного компонента к массе
всех компонентов раствора. Сумма всех массовых долей равна единице.
Мольная доля есть отношение количества компонента к сумме коли-
честв всех веществ, составляющих раствор.
Молярность есть отношение количества растворенного вещества к
массе растворителя.
Объемной концентрацией компонента называется количество его (в
граммах или молях) в единице объема раствора.
Раствор называется ненасыщенным, если концентрация растворенно-
го вещества в нем меньше, чем в насыщенном растворе. Если же она
больше, то раствор называется пересыщенным (и является метастабиль-
ным). В присутствии зародышей растворяемого вещества его избыток вы-
падает из раствора и раствор становится насыщенным.
Газы также могут растворяться в жидкостях и ТТ. При растворении
газа, например, в жидкости молекулы газа переходят из газа, где они слабо
взаимодействуют между собой, в раствор, где они подвергаются сильному
притяжению со стороны молекул растворителя (возникают связи). С этим
связан тот факт, что в подавляющем большинстве случаев тепловой эф-
фект при растворении газов положителен (выделяется теплота).
Согласно принципу Ле-Шателье с увеличением температуры раство-
римость газов должна убывать, а с увеличением давления газа над раство-
ром – возрастать.
Растворы могут быть как жидкими, так и твердыми (см. 3 вопрос).
Многие сплавы при переходе из жидкого состояния в твердое сохра-
няют свою однородность, причем соотношения между компонентами в таких
фазах могут изменяться без нарушения однородности. Такие сплавы называ-
ются
твердыми растворами (ТР). ТР представляет собой однофазную сис-

178
тему, состоит из одного вида кристаллитов, т.е. характеризуется единой кри-
сталлической решеткой. ТР существует не при строго определенном соотно-
шении компонентов, а в определенном интервале концентраций.
16.2. Осмос и осмотическое давление. Закон Рауля
Если два раствора отделены друг от друга пористой перегородкой,
через которую могут проходить молекулы растворителя и растворенного
вещества, то начнется процесс перехода молекул из одного раствора в дру-
гой до выравнивания концентраций обоих растворов и установления дина-
мического равновесия. Подобное равновесие осуществимо в случае
про-
ницаемой
перегородки.
Перегородки (ткани растительного и животного происхождения),
проницаемые для молекул растворителя, но непроницаемые для молекул
растворенного вещества, называются
полупроницаемыми. Если раствор
отделен от чистого растворителя полупроницаемой перегородкой, то через
нее молекулы чистого растворителя переходят в область, занятую раство-
ром. Это явление называется
осмосом (осмос происходит и в тех случаях,
когда полупроницаемая перегородка разделяет два раствора различной
концентрации). В результате осмоса возникает разность давлений между
раствором и чистым растворителем. Осмос прекращается при определен-
ной разности давлений, которая называется
осмотическим давлением.
Существование осмотического давления объясняется нескомпенсирован-
ными с другой стороны перегородки ударами молекул растворенного ве-
щества (удары молекул растворителя будут примерно одинаковыми с обе-
их сторон и не будут создавать давления). Его величину для разбавленных
растворов можно вычислить, как и для идеальных газов по
закону
Я.Х.Вант-Гоффа (1852–1911): осмотическое давление в слабых растворах
подчиняется тем же законам, что и давление идеальных газов:
V
RT
V
NkT
Р
осм
ν
==
, (16.1)
где
N и v – соответственно число молекул и молей растворенного вещества
в объеме раствора
V. Осмотическое давление клеток многих растений дос-
тигает 5–20 атмосфер.
Осмосом объясняется набухание и разрыв оболочек семян растений,
замоченных в воде (проницаемых для воды), оживание и насыщение кра-
сок увядших цветов, опущенных в воду, напоенность водой верхушек де-
ревьев. Осмос играет важную роль и в жизнедеятельности клеток, так как
обмен веществ в живых организмах осуществляется посредством раство-
ров – соков и крови, омывающих полупроницаемые перегородки расти-
тельных и животных клеток.

179
Механизм осмоса до конца еще не выяснен, но согласно одной из
точек зрения он объясняется различной растворимостью в материале пере-
городки соприкасающихся с ней веществ. Перегородка растворяет чистый
растворитель с одной ее стороны, образуется пересыщенный для другой
стороны раствор, тогда перегородка начинает отдавать в жидкий раствор
часть растворителя, растворяя при этом его новые порции.
Если в жидкости растворено нелетучее вещество, то свободную по-
верхность жидкости можно считать полупроницаемой перегородкой: через
нее свободно будут проходить молекулы растворителя, но не смогут прохо-
дить молекулы растворенного вещества. В результате давление насыщенно-
го пара (пара, находящегося в равновесии с жидкостью) над раствором бу-
дет при одной и той же температуре меньше, чем над растворителем. Пусть
Р
0
– давление насыщенного пара над поверхностью растворителя, а Р – дав-
ление над поверхностью раствора в трубке осмометра (рис. 16.1).
Пар
h
Раствор
Р
0
Р
Рис. 16.1
Осмометр в классическом варианте (Пфеффер (1845–1920)) представля-
ет собой глиняный сосуд, в порах которого осаждена механически непрочная
пленка железисто-синеродистой меди
62
)(CNFeCu , являющаяся проницае-
мой перегородкой для воды, но непроницаемой, например, для сахара.
В горло сосуда вставлена длинная вертикальная трубка. Если сосуд
заполнить водным раствором сахара и погрузить в чистую воду, то уровень
жидкости в трубке в результате осмоса (воды в сосуд) изменится, достигая
высоты
h. Тогда осмотическое давление ghP
раросм −
=
ρ
.
В состоянии равновесия
ghPP
пара
ρ
=
−
0
и
00
0
Р
Р
P
PP
осм
рар
пара
⋅=
−
−
ρ
ρ
.
Если раствор разбавленный, то различием между плотностью раствора и
растворителя можно пренебречь. Тогда с учетом равенства
ляр
пара
рар
пара
n
n
−−
=
ρ
ρ
(где
n
пара
– число молекул пара, а n
р-ля
– число молекул растворителя в едини-
це объема раствора) и закона Вант-Гоффа (16.1)
kTnР
осм 1
=
(n
1
– число мо-
лекул растворенного вещества в единице объема раствора) можно получить

180
лярляр
n
n
P
PP
−−
==
−
ν
ν
11
0
0
. (16.2)
Формула (16.2) выражает
закон Ф.М. Рауля (1830–1901): относи-
тельное понижение давления насыщенного пара растворителя над по-
верхностью слабого раствора нелетучего вещества равно отношению
числа молей растворенного вещества к числу молей растворителя
.
Из закона Рауля также следует, что при одном и том же давлении темпе-
ратура кипения раствора выше температуры кипения чистого растворителя.
16.3. Многокомпонентные твердые растворы (МТР)
и их диаграммы состояния. Применение МТР
(перед изучением данного вопроса следует ознакомиться с вопросом 2
лекции 15)
Рентгенографические исследования ТР (общее определение ТР дано
в вопросе 1) показывают, что
существуют три структурных типа ТР: ТР
замещения, внедрения и вычитания.
В
ТР замещения на основе химического элемента атомы растворен-
ного вещества
А замещают в кристаллической решетке атомы растворите-
ля
В, статистически (хаотически) распределяясь среди них (рис. 16.2, а). В
ТР замещения между химическими соединениями вида
АВ и АС атомы
(ионы) компонентов размещаются в соответствии с рис. 16.2,
б.
а) б) в)
A
B
C
Рис. 16.2
Многокомпонентными или сложными ТР (МТР) называются ТР с
числом компонентов
3≥n . Сложные ТР замещения обычно состоят из
атомов элементов нескольких групп (подгрупп) Периодической таблицы
Д.И.Менделеева. Как известно, в группе находятся элементы, характери-
зуемые подобными физико-химическими свойствами. Примером может
служить четырехкомпонентный ТР, состоящий из атомов двух групп (
А, В)
одной группы (и обычно одной и той же подгруппы) Периодической таб-
лицы и (
С, D) другой группы (и одинаковой подгруппы): AlGaAsSb, где
алюминий
Al и галлий Ga – элементы III группы, а мышьяк As и сурьма Sb
– V группы. Такие ТР представляют собой как бы две кристаллические
