Контрольная работа по химии №1
Подождите немного. Документ загружается.

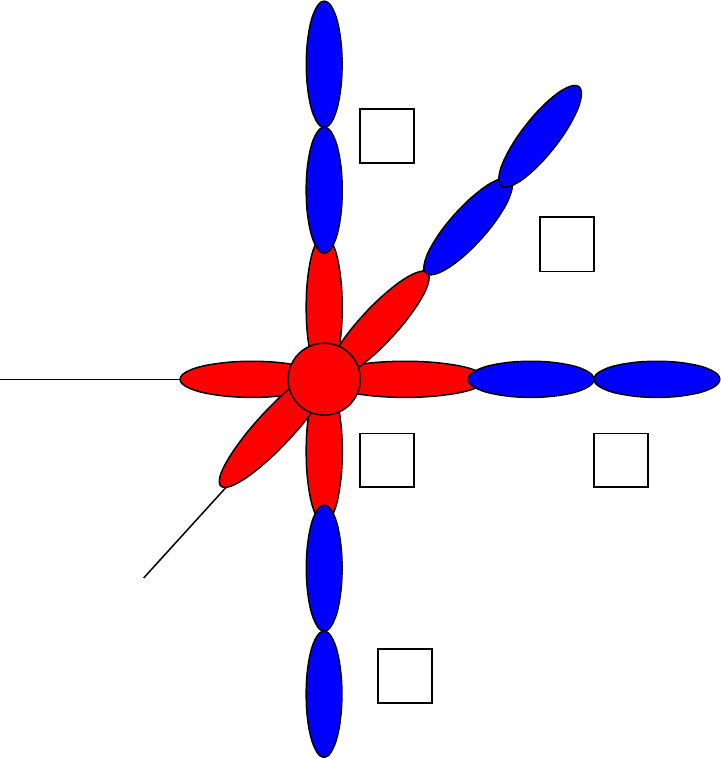
-схема перекрывания орбиталей для молекулы .............:
геометрическая форма молекулы: ................................
С
Br
Br
Br
Br
11
Задача N 4
Вычислите стандартные величины H
0
298,
S
0
298
и G
0
298
для реакции:
…HCHO
(r)
H
2(r)
+ CO
(r)
Объясните знак изменения энтальпии и энтропии. Возможно ли самопроизвольное
протекание данной реакции при стандартных условиях?
Решение
H (энтальпия), S (энтропия) и G (свободная энергия Гиббса или термодинамический
потенциал) являются термодинамическими функциями состояния и обладают общим
свойством: их изменение в ходе химической реакции не зависит от пути этой реакции, а
определяется только начальными и конечными веществами. Это позволяет вычислять H,
S, G для реакции общего вида aA + bB = cC + dD по формулам:
H
0
= (cH
0
C
+ dH
0
D
) - (aH
0
A
+ bH
0
B
)
S
0
=
(cS
0
C
+
dS
0
D
)
-
(aS
0
A
+
bS
0
B
)
G
0
= (cG
0
C
+ dG
0
D
) - (aG
0
A
+ bG
0
B
),
где
H
0
C
, H
0
D
, H
0
A
, H
0
B
- стандартные энтальпии образования веществ C, D, A, B (см.
ДОТ_Химия_2.2. Опорный конспект_Справочные материалы );
S
0
C
, S
0
D
, S
0
A
,
S
0
B
- стандартные энтропии веществ C, D, A, B (см. ДОТ_Химия_2.2. Опорный
конспект_Справочные материалы) ;
G
0
C
, G
0
D
, G
0
A
, G
0
B
- стандартные свободные энергии образования веществ C, D, A, B.
Величину G
0
можно вычислить по формуле:
G
0
= H
0
- T S
0
(при этом для стандартных условий T = 298 К).
Для реакции, указанной в условии задачи, выписываем необходимые справочные
данные:
H
0
А
.
=
.
– 115,90
.....................................
S
0
А
=
218,78
...............................................................................................
H
0
В
..
= 0
.................................................. .....
S
0
В
=
0
.........................………....................................................................
H
0
С
....
= 0,00
..................................... .....
S
0
С
= 130,52
................………................................................................
H
0
D
....
= - 110,53
......................... .... .....
S
0
D
= 197,55
..……………..................................................................
H
0
= (H
0
H
2
+ H
0
CО) - (H
0
HCHO) = (0,00 +(-110,53)) –
12

((-115,90)+ 0 ) = (-110,53) - (-115,90) = 5,37 кДж
S
0
= (S
0
H
2
+
S
0
CО
)
-
(S
0
HCHO
) = (130,52 + 197,55)- (218,78 + 0 ) =
328,07 – 218,78 = 109,29 Дж/К = 0,109 кДж/К
1
G
0
= H
0
- 298 * S
0
= - 27,112 кДж
Изменения термодинамических функций H, S, G в ходе химической реакции
позволяют судить об особенностях протекания данной реакции и ее природе.
H определяет величину теплового эффекта химической реакции. Процесс,
характеризующийся величиной H<0, происходит с выделением тепла и относится к разряду
экзотермических. H>0 говорит о том, что тепло в ходе реакции поглощается, такие
реакции называются эндотермическими.
В данной реакции величина H > 0, следовательно, тепло поглощается, и реакция
является эндотермической.
S характеризует изменение степени неупорядоченности системы.
Возрастание энтропии ( S
0
>0) говорит о возрастании неупорядоченности в расположении
и перемещении частиц в ходе химической реакции. Это происходит, например, при
превращении твердых веществ в жидкие или газообразные или при увеличении количеств
газообразных веществ. Напротив, уменьшение энтропии (S
0
<0) cвидетельствует о
возрастании упорядоченности системы в ходе реакции. Уменьшение энтропии характерно
для реакций, в ходе которых, например, газообразные или жидкие вещества превращаются
в твердые, а также для газовых реакций, сопровождающихся уменьшением количеств
газообразных веществ.
Для данной реакции рассчитанная величина изменения энтропии S
0
> 0, что
свидетельствует об увеличении (увеличении или уменьшении?) неупорядоченности в
данной системе. Действительно, из уравнения реакции видно, что в ходе реакции
из ..1........моль газообразных веществ HCHO
(r)
образуется .....2....моль газообразных
веществ… H
2(r)
и CO
(r)
, следовательно, степень неупорядоченности увеличивается
(увеличивается или уменьшается?).
Величина G
0
позволяет судить о принципиальной возможности
самопроизвольного протекания химической реакции при стандартных условиях: если G
0
<
0, данная химическая реакция принципиально осуществима при стандартных условиях, если
же G
0
> 0, то нет (в этом случае осуществима обратная реакция). Состояние химического
равновесия в системе отвечает равенству G
0
= 0.
Для рассматриваемой в задаче реакции вычисленная величина G
0
составляет
- 27,112 кДж, т.е. G
0
< 0. Следовательно, данная химическая реакция при
стандартных условиях принципиально осуществима (осуществима или не осуществима).
1
1 кДж = 1000 Дж
13
Задача N 5
Для реакции:
HCHO
(r)
H
2(r)
+ CO
(r)
составьте кинетическое уравнение;
составьте выражение для константы равновесия;
вычислите, во сколько раз изменится скорость реакции при заданных изменениях:
1. температуры,
2. общего давления (при изменении объема системы),
3. концентраций реагентов
укажите, как необходимо изменить внешние параметры (температуру, общее давление,
концентрации реагентов), чтобы сместить равновесие вправо.
Номер
задачи
Порядок
по 1-му
реагент
у
Порядок
по 2-му
реагент
у
γ Т
1
, К Т
2
, К
1
1
C
C
2
2
C
C
P
P
96 2 - 2,8 347 377 3 - 5
Решение
Химическая реакция может быть охарактеризована скоростью ее протекания.
Скорость химической реакции зависит от многих факторов, среди которых:
- природа реагирующих веществ;
- температура;
- концентрация реагирующих веществ;
- присутствие катализаторов.
Зависимость скорости реакции
aA + bB ↔ cC + dD
от концентраций реагирующих веществ может быть охарактеризовано кинетическим
уравнением:
V = k C
A
x
·C
B
y
,
где: V – скорость химической реакции, k- константа скорости химической реакции, C
A
и
C
B
- концентрации веществ А и В, x и y – порядки реакции по реагентам А и В,
соответственно (порядки реакции могут определены исключительно экспериментально).
14

Для приведенной в условии задачи реакции
HCHO
(r)
H
2(r)
+ CO
(r)
кинетическое уравнение имеет вид:
V = k C
HCHO
2
При повышении концентрации первого реагента в …3…. раз (
1
1
C
C
) скорость реакции
возрастет в…9….. раз.
При повышении концентрации второго реагента в …-…. раз (
2
2
C
C
) скорость реакции
возрастет в…-….. раз.
При повышении давления в …5…. раз (
1
1
P
P
) скорость реакции возрастет в 5
2
…*…=
…25.. раз.
Зависимость скорости реакции от температуры отображается формулой Вант-
Гоффа:
10
tt
t
t
12
1
2
γ
V
V
где V
t2
- скорость реакции при температуре t
2
,
V
t1
- скорость реакции при температуре t
1
,
- постоянная для данной реакции величина, называемая температурным
коэффициентом реакции.
Данные, приведенные в условии задачи:
= ..2,8....
t
1
= ..347K....
t
2
= ..377K...
Вычисления по формуле Вант-Гоффа дают результат:
1
2
t
t
V
V
= 2,8
377-347/10
= 21,952 ≈ 22
Таким образом, при повышении температуры на 30K скорость данной реакции
возрастет в ..22... раза.
15

Большинство химических реакций являются обратимыми: одновременно с прямой
реакций протекает обратная. В момент выравнивания скоростей прямой и обратной реакций
в системе наступает состояние химического равновесия.
Константа химического равновесия характеризует взаимосвязь равновесных
концентраций веществ, участвующих в данной реакции.
Для реакции общего вида:
a A + b B ↔ c C + d D,
где A, B, C, D - химические формулы веществ, а, b, c, d - стехиометрические
коэффициенты, выражение для константы химического равновесия выглядит
следующим образом:
ba
dc
[B][A]
[D][C]
K
где [A], [B], [C], [D] - равновесные концентрации соответствующих веществ.
В случае гомогенного равновесия (все вещества находятся в одинаковом фазовом
состоянии, реакция происходит в однородной, гомогенной среде) в правую часть данного
выражения записывают равновесные концентрации всех участников этого равновесия.
Для гетерогенных равновесий (вещества находятся в разных фазовых cостояниях,
реакция протекает в неоднородной, гетерогенной среде) концентрацию твердых веществ
считают практически неизменной и не записывают в правую часть выражения для константы
равновесия.
Равновесие, отображенное схемой, приведенной в условии задачи, относится к
разряду ........................, выражение для константы равновесия имеет вид:
К
p
= P
H
2
*
P
CO
P
HCHO
Изменение внешних условий приводит к смещению химического равновесия.
Прогнозировать направление смещения равновесия можно с помощью принципа Ле
Шателье:
если на систему, находящуюся в равновесии, оказывается воздействие
извне, то равновесие смещается в сторону той реакции, протекание
которой максимально ослабляет внешнее воздействие.
Поэтому:
нагревание благоприятствует протеканию эндотермической реакции (H>0), а
охлаждение, напротив, смещает равновесие в сторону протекание экзотермической
реакции (H<0);
повышение общего давления в системе смещает равновесие в сторону реакции с
образованием меньшего количества газообразных веществ, а понижение - большего;
добавление в реакционную систему какого-либо компонента ускоряет ту реакцию,
где этот компонент расходуется, а отвод - реакцию, в которой это вещество
образуется.
Исходя из этого, для смещения равновесия слева направо в рассматриваемой в задаче
системе обратимых химических реакций, в которой прямая реакция происходит с
поглащением... тепла (H > 0) и увеличением (увеличением или уменьшением) количеств
16

газообразных веществ (из 1 моль газов (HCHO) в результате реакции образуется 2 моль
газообразных продуктов(H
2
и CO)), НЕОБХОДИМО:
- температуру повысить (повысить или понизить),
- давление понизить (повысить или понизить)
- концентрацию исходных веществ ... HCHO.... и ...……..(формулы) повысить
(повысить или понизить),
- концентрацию продуктов прямой реакции ..... H
2
...... и ... CO.......(формулы)
понизить (повысить или понизить) (отвод).
Задача N 6
Для реакций:
1. Se + AuCl
3
+ H
2
O Au + H
2
SeO
3
+ HCl
2. MnO
2
+ NaOH MnO(OH) + Na
3
MnO
4
+ H
2
O
Составьте уравнения методом электронного баланса. Для каждой реакции укажите, какое
вещество является окислителем, а какое – восстановителем и за счет каких атомов.
Определите типы данных окислительно-восстановительных реакций.
Решение
Окислительно-восстановительные реакции характеризуются переходом электронов от
одного вещества (восстановителя) к другому (окислителю).
Для ответов на вопросы задачи вычислим степени окисления атомов, входящих в
состав приведенных в уравнении реакции веществ, руководствуясь следующими правилами:
- степени окисления атомов в простых веществах (построенных из атомов одного и
того же элемента) принимаются равными нулю;
- степень окисления атома водорода в соединениях с неметаллами равна +1;
17

- степень окисления атома кислорода в большинстве его соединениях равна -2 (к
исключениям из правила относятся, например, пероксиды типа H
2
O
2
, в которых
степень окисления атома О равна -1);
- степени окисления типичных металлов (I,II,III группы главные подгруппы
периодической системы Д. И. Менделеева, кроме бора) в их соединениях постоянны и
численно равны номеру группы, т.е. +1, +2, +3, соответственно;
- алгебраическая сумма степеней окисления атомов в молекуле равна нулю, в сложном
ионе - заряду иона.
Запишем вычисленные степени окисления над символами элементов в уравнении
реакции:
Se
O
+ Au
+3
Cl
3
-1
+ H
2
+1
O
-2
Au
O
+ H
2
+1
Se
+4
O
3
-2
+ H
+1
Cl
-1
Mn
+4
O
2
-2
+ Na
+1
O
-2
H
+1
Mn
+3
O
-2
(OH)
-1
+ Na
3
+1
Mn
+5
O
4
-2
+ H
2
+1
O
-2
Для составления электронных уравнений выпишем атомы элементов, изменившие
свои степени окисления, и укажем число электронов, отдаваемое или принимаемое атомами
для осуществления такого изменения степеней окисления:
первая реакция:
Se
O
- - 4 е = Se
+4
Au
+3
- + 3 е = Au
O
вторая реакция:
Mn
+4
- + 1 е = Mn
+3
Mn
+4
- - 1 е = Mn
+5
Восстановителями (отдают электроны) являются:
В первой реакции Se (степень окисления повышается с 0 до + 4)
……………………………………………………………………
Во второй реакции MnO
2
(за счет атома Mn, степень окисления которого
повышается с + 4 до + 5) ………………………………
Окислителями (принимают электроны) являются:
В первой реакции AuCl
3
(за счет атома Au, понижает степень окисления с + 3 до 0)
….……………………………
Во второй реакции MnO
2
(за счет атома Mn , понижает степень окисления с + 4 до
+3). ………………………………
18

Суммарное число электронов, отдаваемых в ходе реакции частицами-
восстановителями, и суммарное число электронов, принимаемых в ходе реакции частицами-
окислителями должны быть равны друг другу. На этом основан один из методов расстановки
коэффициентов в уравнениях окислительно-восстановительных реакций, называемый
методом электронного баланса.
Для обеспечения указанного электронного равенства подберем множители к
электронным уравнениям процессов окисления и восстановления, найдя наименьшее общее
кратное для числа отданных и присоединенных электронов и поделив его на каждое из
чисел.
Запишем полученные множители справа за чертой у каждого из уравнений:
Первая реакция:
Se
O
- - 4 е = Se
+4
3
Au
+3
- + 3 е = Au
O
4
Вторая реакция:
Mn
+4
- + 1 е = Mn
+3
1
Mn
+4
- - 1 е = Mn
+5
1
Расстановку коэффициентов проведем в следующей последовательности:
- перенесем полученные в электронном балансе множители в левую и правую части
уравнения реакции к формулам соответствующих веществ;
- уравняем атомы металлов;
- уравняем кислотные остатки;
- уравняем атомы водорода.
Итоговые коэффициенты в уравнениях данных реакций таковы:
Первая реакция:
3Se + 4AuCl
3
+ 9H
2
O 4Au + 3H
2
SeO
3
+ 12HCl
Вторая реакция:
19

2MnO
2
+ 3NaOH MnO(OH) + Na
3
MnO
4
+ H
2
O
Для проверки их правильности просуммируем число атомов кислорода в левой и правой
части уравнения:
..9.... = ..9...
..7.... = .7.....
Значит коэффициенты расставлены верно.
Для определения типа рассматриваемой окислительно-восстановительной реакции
воспользуемся следующей классификацией:
- межмолекулярные окислительно-восстановительные реакции (атом-окислитель и
атом-восстановитель входят в состав разных веществ);
- внутримолекулярные окислительно-восстановительные реакции (атом-окислитель
и атом-восстановитель входят в состав одного и того же вещества, являясь атомами
разных элементов);
- реакции диспропорционирования (атом-окислитель и атом-восстановитель являются
атомами одного и того же элемента в промежуточной степени окисления).
Рассматриваемые в задаче окислительно-восстановительные реакции относятся к
типам:
первая межмолекулярные, т.к. атом-окислитель и атом-восстановитель входят в
состав разных веществ ……..
…………………………………………………………………………............
………………………………………………………………………………………………………….
............
вторая диспропорционировани, т.к. атом-окислитель и атом-восстановитель являются
атомами одного и того же элемента в промежуточной степени окисления
…………………………………………………………………………………………………………
…………………………………………………..
. Задача N 7
Составьте схему гальванического элемента, напишите электронные уравнения
электродных процессов и суммарное уравнение соответствующей окислительно-
восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС.
Номер
задачи
Металл
1-го
электр
ода
Электролит 1-
го электрода
Концентр
ация
электроли
та 1-го
электрода
Металл
2-го
электр
ода
Электролит
2-го
электрода
Концентра
ция
электролит
а 2-го
электрода
ЭДС
20
