Мустафаев А.С., Корольков А.П., Смирнова Н.Н., Варшавский С.П. Общая физика. Механика. Молекулярная физика: Лабораторный практикум
Подождите немного. Документ загружается.

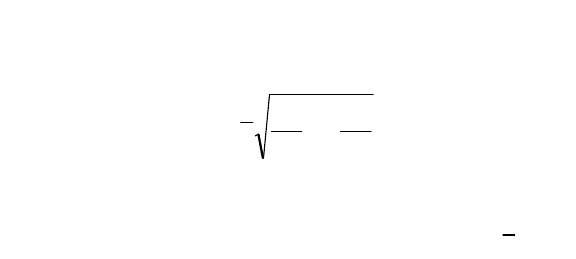
2)Eзафиксировать диски на стержне, чтобы один из них
находился вблизи конца стержня, а другой вблизи его середины;
3)Eзакрепить маятник на верхнем кронштейне на призме,
находящейся вблизи конца стержня, так чтобы конец стержня
пересекал оптическую ось фотоэлектрического датчика;
4)Eотклонить маятник примерно на 5 от положения
равновесия и придерживать его рукой;
5)Eотпустить маятник (маятник придет в движение);
6)Eизмерить время 10 колебаний маятника t;
7)Eопределить период колебаний оборотного маятника
T
1
E=Et/n;
8)Eснять маятник и закрепить его на второй призме;
9)Eизмерить период Т
2
, повторив пп.4-7;
10)Eсравнить периоды Т
2
и T
1
; если Т
2
> T
1
, вторую призму
переместить в направлении диска, находящегося в конце стержня;
если Т
2
E<ET
1
, переместить ее в направлении середины стержня
(положение дисков и первой призмы не менять);
11)Eснова измерить период Т
2
и сравнить его с величиной T
1
;
менять положение второй призмы до тех пор, пока значение периода
Т
2
не станет равным значению периода T
1
с точностью до 0,5E%;
12)Eопределить приведенную длину оборотного маятника L,
измерив расстояние между призмами (по числу нарезок, которые
нанесены через каждые 10Eмм).
13)Eобработать результаты эксперимента, вычислив
ускорение свободного падения по формуле (6) при ТE=EТ
1
E=EТ
2
,
среднюю квадратическую ошибку
n
tT
/
(здесь
t
–
погрешность измерения времени, оцениваемая исходя из точности
прибора) и среднюю квадратическую ошибку
,4
2
2
2
2
TL
g
TL
g
где
L
– погрешность измерения длины, оцениваемая по цене
деления измерительной линейки.
14)Eзаписать окончательный результат в виде
g
gg
.
61

Контрольные вопросы
1.EЧто такое математический маятник?
2.EЧто такое физический маятник?
3.EКак с помощью маятников можно измерить ускорение
свободного падения?
4.EС чем связана погрешность определения g с помощью
математического маятника?
5.EС чем связана погрешность определения g с помощью
физического маятника и как ее устранить?
6.EВ чем заключается метод оборотного маятника?
РаботаC9.CИЗУЧЕНИЕ ПРЕЦЕССИИ ГИРОСКОПА
Цель работы – экспериментально исследовать основные
свойства гироскопа, изучить законы вращательного движения
твердого тела.
Общие сведения
Гироскопом называют массивное симметричное тело,
вращающееся с большой скоростью вокруг оси симметрии.
Основное свойство гироскопа – способность сохранять неизменным
направление оси вращения при отсутствии действующего на него
момента внешних сил. Это свойство гироскопа основано на законе
сохранения момента импульса. Гироскопы широко применяются в
технике: в качестве стабилизаторов направления при движении
судов, самолетов (устройство автопилот) и т.д.
Рассмотрим гироскоп, основным элементом которого
является диск D, вращающийся со скоростью
вокруг
горизонтальной оси ОО' (см. рисунок). Ось гироскопа шарнирно
закреплена в точке C. Прибор снабжен противовесом K. Если
противовес установлен так, что точка C является центром масс
системы (m – масса гироскопа; m
0
– масса противовеса K; масса
стержня пренебрежимо мала), то без учета трения можно записать:
62

,или
0000
FllFmglglm
т.е. результирующий момент сил, действующий на систему, равен
нулю. Тогда справедлив закон сохранения момента импульса
L
:
0
dt
Ld
.
Иными словами, в этом случае
JL
const (здесь J –
момент инерции гироскопа,
– собственная угловая скорость
вращения гироскопа).
Поскольку момент инерции диска относительно его оси
симметрии есть величина постоянная, то вектор угловой скорости
также остается постоянным как по величине, так и по направлению.
Вектор
направлен по оси вращения в соответствии с правилом
правого винта. Таким образом, ось свободного гироскопа сохраняет
свое положение в пространстве неизменным.
Если к противовесу K добавить еще один с массой m
1
, то
центр масс системы сместится и возникнет вращающий момент
,
1
M
направленный перпендикулярно оси ОО' в горизонтальной
плоскости. Согласно уравнению моментов,
MdtLd
. Под
действием этого вращающего момента вектор момента импульса
получит приращение
Ld
, совпадающее по направлению с
вектором
1
M
:
63
d
1
M
1
L
L
Ld
F
B
B
D
O
О
0
F
K
С
l
l
0

010111
; glmlFMdtMLd
. (1)
Спустя время
dt
момент импульса гироскопа изменится на
величину
Ld
:
LdLL
1
.
Таким образом, вектор
L
изменяет свое направление в
пространстве, все время оставаясь в горизонтальной плоскости.
Учитывая, что вектор момента импульса гироскопа направлен вдоль
оси вращения, поворот вектора
L
на некоторый угол d за время dt
означает поворот оси вращения на тот же угол. В результате ось
симметрии гироскопа начнет вращаться вокруг неподвижной
вертикальной оси ВВ' с угловой скоростью:
dt
d
.
Такое движение называется регулярной прецессией, а величина
– угловой скоростью прецессии.
Выясним зависимость угловой скорости прецессии
гироскопа от основных параметров системы. Из формул (1) получим
.
01
dtglmdL
При малых углах поворота из геометрических соображений (см.
рисунок)
LddL
, тогда
dtlFLd
01
, и угловая скорость
прецессии
)/(
01
Jglm
. (2)
Подвижный элемент гироскопа представляет собой
массивный маховик (диск), закрепленный на оси электродвигателя.
Вдоль оси маховика закреплена планка с линейной метрической
шкалой. Вдоль планки может перемещаться противовес.
Угол поворота оси двигателя в горизонтальной плоскости и
время движения измеряются электронной схемой с
фотоэлектрическим датчиком. Кроме того, угол поворота гироскопа
можно считывать по нанесенной на основании подвижной части
угловой шкале. По окружности основания через каждые 5 нанесены
64

отверстия, которые служат для считывания угла поворота при
помощи фотоэлектрического датчика. На лицевой панели блока
управления расположены индикаторные табло угла и времени
поворота, а также кнопки «СЕТЬ», «СБРОС», «СТОП», и рукоятка
регулятора скорости вращения «РЕГ. СКОРОСТИ».
Порядок выполнения работы
1.EПеремещая противовес K вдоль планки, уравновесить
систему (ось должна принять горизонтальное положение); измерить
и записать расстояние l
0
от центра масс противовеса до оси вращения
– точки С (см. рисунок).
2.EВключить установку, двигатель и довести угловую
скорость вращения до 1000Eмин
–1
.
3.EПодвесить к противовесу перегруз m
1
и дать гироскопу
свободно прецессировать, записать значение m
1
.
4.EПосле поворота гироскопа на некоторый угол в пределах
30E<EE<E100 записать угол и время t поворота.
5.EПовторить пп.2-4 при данной угловой скорости ротора не
менее 5Eраз.
6.EПровести измерения для пяти-шести режимов вращения
ротора, меняя угловую скорость через 1000Eмин
–1
от 1000 до
6000Eмин
–1
. Перед каждым повторным измерением устанавливать
ось гироскопа горизонтально.
7.EРезультаты измерений записать в таблицу:
Номер
опыта
Номер
измерения
t t
J J
1 1
2
…
5
1
1
J
2
…
65

8.EОбработать результаты эксперимента. Вычислить угловую
скорость прецессии гироскопа E=E/t для всех значений угловой
скорости (вращение в данном случае равномерное) и вычислить
среднее значение
для каждого режима вращения двигателя.
Найти ошибку измерений по разбросу результатов и построить
график зависимости (1/). Сделать вывод относительно
выполнения зависимости (2).
Рассчитать момент инерции гироскопа в каждом случае (k –
номер измерения, и выразить в радианах в секунду)
)/(
01 kkk
glmJ
и вычислить среднее значение
J
.
Определить среднюю арифметическую ошибку результата
J (формулу вывести самостоятельно). Погрешность l
0
и
определить по цене деления измерительных приборов, погрешность
mE=E1Eг.
9.EРезультат измерений представить в виде
JJJ
.
Контрольные вопросы
1.EЧто такое гироскоп?
2.EКакими свойствами обладает гироскоп? Какими
физическими законами обусловлены эти свойства?
3.EПочему возникает регулярная прецессия гироскопа?
4.EОт каких параметров системы зависит угловая скорость
прецессии?
66

МОЛЕКУЛЯРНАЯ ФИЗИКА
РаботаC10.CОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ
ТЕПЛОЕМКОСТИ ВОЗДУХА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
К ТЕПЛОЕМКОСТИ ПРИ ПОСТОЯННОМ ОБЪЕМЕ
МЕТОДОМ АДИАБАТИЧЕСКОГО РАСШИРЕНИЯ
Цель работы – изучить законы идеального газа и основные
положения классической теории теплоемкости; определить
коэффициент Пуассона
методом адиабатического расширения
(методом Клемана – Дезорма).
Общие сведения
Количество тепла, которое необходимо сообщить одному
молю вещества, чтобы повысить его температуру на 1EК, называют
молярной теплоемкостью.
M
dT
dQ
C
,
где Q – количество тепла, подводимого к системе; Т – абсолютная
температура системы; M – масса газа; – масса одного моля газа.
Как показывают теория и опыт, теплоемкость зависит от
условий, при которых нагревается газ, т.е. от характера
термодинамического процесса.
Теплоемкость газа при постоянном давлении С
p
больше
теплоемкости при постоянном объеме C
V
. Это легко показать
качественно на основании первого начала термодинамики:
количество тепла Q, подводимого к системе, идет на увеличение
внутренней энергии системы U и на совершение этой системой
работы A над внешними телами:
Q7=7UE+EA.
Если газ нагревается при постоянном объеме, то работа не
совершается и все подводимое тепло идет на увеличение запаса его
внутренней энергии U, т.е. только на повышение температуры газа.
EКоэффициент Пуассона – отношение теплоемкости воздуха при
постоянном давлении С
р
к теплоемкости при постоянном объеме C
V
.
67
Если же газ нагревается при постоянном давлении, он расширяется
и производит работу, требующую дополнительного расхода тепла.
Таким образом, для повышения температуры газа на определенную
величину в изобарном процессе требуется большее количество
теплоты, чем при изохорном.
Как следует из теории,
C
p
E=EC
V
E+ER, (1)
где R – универсальная газовая постоянная.
Выражение (1) носит название соотношения Майера.
Отношение E=EС
р
/C
V
входит в уравнение Пуассона,
описывающее адиабатический процесс, т.е. процесс, идущий без
теплообмена с окружающей средой (QE=E0):
2211
;const VpVppV
. (2)
Здесь p
1
и V
1
– давление и объем газа в первом состоянии; p
2
и V
2
–
давление и объем газа во втором состоянии.
Полную теплоизоляцию газа от внешней среды
осуществить невозможно. Однако, если параметры состояния газа
изменяются очень быстро, процесс можно приближенно считать
адиабатическим. На практике адиабатический процесс совершается
в некоторых тепловых двигателях (например, в двигателе Дизеля);
распространение звука в газах (быстрое периодическое изменение
давления в малых областях
пространства) также протекает
адиабатически.
68
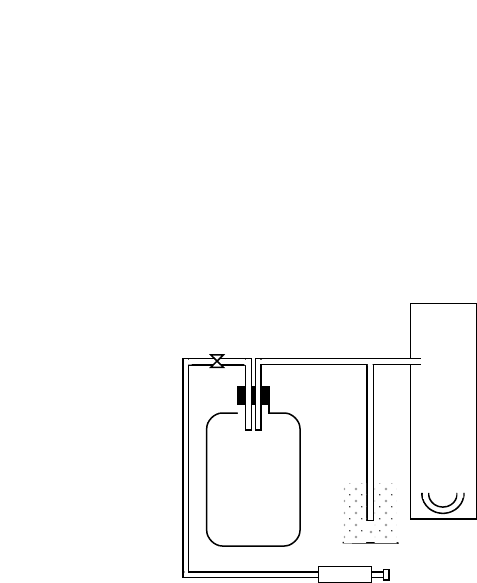
В
K
U-образный
манометр
Насос

Рассмотрим метод Клемана – Дезорма. Накачаем насосом
воздух в большой стеклянный баллон В (см. рисунок) и закроем
кран K. При быстром сжатии температура воздуха повышается.
Поэтому после прекращения нагнетания разность уровней жидкости
в манометре будет постепенно уменьшаться, пока температура
воздуха внутри баллона не сравняется с температурой окружающего
воздуха. Назовем состояние воздуха в баллоне после выравнивания
температур состоянием 1. Параметры состояния 1 следующие: V
1
–
объем единицы массы воздуха; t
1
– температура воздуха; HE+Eh
1
–
давление в баллоне, выраженное в единицах разности уровней
жидкости в манометре
; Н – атмосферное давление; h
1
– избыточное
давление, созданное накачиванием.
Откроем кран K и, как только давление в баллоне В
сравняется с атмосферным (это можно определить по прекращению
характерного шипения), закроем его. Так как расширение
происходит очень быстро, то процесс близок к адиабатическому и,
следовательно, температура понизится до t
2
. Объем единицы массы
воздуха станет равным V
2
. Воздух, оставшийся в баллоне, перейдет в
состояние 2 с параметрами V
2
, t
2
, Н. Так как температура t
2
меньше
наружной, то воздух в баллоне будет постепенно нагреваться (вслед-
ствие теплообмена с окружающей средой) до температуры
окружающего воздуха t
1
. Это нагревание происходит изохорически,
так как кран закрыт. Давление воздуха в баллоне увеличивается по
сравнению с атмосферным, и в манометре возникает разность
уровней h
2
, т.е. воздух переходит в состояние 3 с параметрами V
2
, t
1
,
НE+Eh
2
.
Таким образом, мы имеем три состояния газа со
следующими параметрами:
Состояние 1 2 3
Объем V
1
V
2
V
2
Температура t
1
t
2
t
1
Давление НE+Eh
1
Н НE+Eh
2
EГидростатическое давление выражается через разность уровней:
p7=7gh, где – плотность жидкости. В итоговую формулу давления войдут в виде
отношения, поэтому сомножитель g можно опустить с самого начала.
69

В состояниях 1 и 3 воздух имеет одинаковую температуру,
следовательно, параметры этих состояний можно связать
уравнением изотермического процесса (уравнением Бойля –
Мариотта):
.
2211
hHVhHV
. (3)
Переход от состояния 1 к состоянию 2 происходит
адиабатически, поэтому параметры их связаны уравнением
Пуассона (2), которое примет вид
.
211
HVhHV
(4)
Преобразуем уравнение (3). Возведем обе его части в
степень :
2211
hHVhHV
.
Разделим почленно полученное равенство на выражение (4),
2
112
1
1
или
hH
hH
H
hH
H
hH
hH
hH
.
Прологарифмируем последнее равенство:
2
11
lglg
hH
hH
H
H+h
,
откуда
.
+1lg
1lg
;
lg
lg
2
21
1
2
1
1
hH
hh
H
h
hH
hH
H
hH
Так как величины h
1
и h
2
, выраженные в миллиметрах
ртутного столба, очень малы по сравнению с Н и, следовательно,
70
