Сборник докладов Энергетика, надежность, безопасность
Подождите немного. Документ загружается.


Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
геологической среды при ее освоении, позволяет обосновывать конкретные меры борьбы с
негативными инженерно-геологическими процессами, а также принимать оптимальные проектные
решения с учетом границ конкретного типа строения геологической среды и ее устойчивости.
Такая оценка необходима для более грамотных и конкретных рекомендаций по рациональному
использованию и охране геологической среды городской территории. Поэтому
геолого-
экологические задачи необходимо включать в систему текущих и перспективных задач решения
перманентной экологической проблемы города в рамках его социально-экономического развития.
Приведенные суждения позволяют сформулировать ключевые направления
экологических исследований и охраны геологической среды городской территории:
•
исследование изменений физико-механических и химических свойств грунтов и подземных
вод, залегающих в основании зданий и сооружений для объективной оценки их несущей
способности и предотвращения разрушений фундаментов и подземных коммуникаций;
•
обоснование, выделение и пространственное обособление зон реального или потенциального
социального дискомфорта для человека, обусловленных геодинамическими и другими
неоднородностями литосферы;
•
количественная оценка риска, опасности и ущерба, развитых на территории инженерно-
геологических процессов и явлений;
Такая экологически ориентированная геологическая информация поможет принимать
объективные управляющие решения, направленные на сохранение или улучшение экологической
обстановки, которая формируется под воздействием города и геологической среды.
Список литературы:
1. Голодковская Г.А., Зеенгофер Ю.О., Лебедева Н.И. Вопросы и методика комплексного
картографирования городской территории для прогнозной оценки изменений геологической
среды // Новые типы карт. М.: Изд-во МГУ,1983.– С. 39 – 48.
2.
Дзекцер Е.С., Казеннов С.М. Принципы районирования территорий городов по их
потенциальной подтопляемости грунтовыми водами //Методы типизации и картирования
геологической среды городских агломераций для решения задач планирования инженерно-
хозяйственной деятельности. - М.: Изд-во МосТИСИЗ ПО Стройизыскания, 1981. – С.72 – 76.
3.
Крепша Н.В. Типизация инженерно-геологических условий территории города Томска как
основа прогноза их изменений при освоении: Автореф. дис….канд. г. - м. наук. – Томск,
1990.– 21с.
4.
Крепша Н.В. Прогнозирование изменения геологической среды в условиях техногенного
воздействия города на основе картографического метода // Геоэкология. – 1993. – № 3. – С. 44
– 57.
5.
Сулакшина Г.А., Рождественская Л.А., Рогова Н.С.. Крепша Н.В. Характер и прогноз
изменчивости инженерно-геологических условий городских территорий Западной Сибири при
застройке / Проблемы инженерной геологии Сибири. – Новосибирск: Наука, 1985. – С. 47–50.
6.
Опыт крупномасштабного инженерно-геологического картографирования геологической
среды г. Томска // Материалы региональной конференции геологов Сибири, Дальнего Востока
и северо-востока России в г. Томске 18-23 сент. 2000 г. Томск – т.1.– С.350–352.
УДК 665
Увеличение выхода дистиллятных фракций из тяжёлых нефтяных остатков
И.А. Кузнецов, *М.А. Копытов, *А.К. Головко, **А.Г. Аншиц
Томский государственный университет, г. Томск, Россия
*Институт химии нефти СО РАН, г. Томск, Россия
**Институт химии и химической технологии СО РАН, г. Красноярск, Россия
kma@ipc.tsc.ru
Исследования в области нефтепереработки ведутся довольно давно, в основном это
термические и термокаталитические процессы. В результате этих исследований разработано и
функционируют множество нефтеперерабатывающих процессов.
Среди всех применяемых методов переработки тяжелых нефтяных остатков наиболее
эффективным является гидрокрекинг, но в то же время и наиболее дорогостоящим.
В связи с увеличением потребности в моторных
топливах и уменьшением количества
легких нефтей становится актуальной проблема переработки тяжелых нефтяных остатков и в
частности мазутов альтернативными методами. Поэтому цель нашей работы был поиск и
171
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
исследование методов позволяющих увеличивать выход дистиллятных моторных топлив из
тяжелых нефтей и остатков нефтепереработки.
В данной работе была проведена серия экспериментов по термической обработке
тяжелого углеводородного сырья (мазут Зуунбаянского месторождения – Монголия). С целью
увеличения выхода дистиллятных фракций мазут предварительно подвергали механоактивации
(МА)[1] в шаровой мельнице (с ускорением 60
g). Термолиз проводили в близких к
сверхкритическим условиях при температуре 450
°С в течении 2 часов в присутствии добавки –
микросфер (микросферы зол ТЭЦ содержащие до 85% Fe
2
O
3
), а также в присутствии
протонодонорной добавки тетралина. Опробованы следующие схемы экспериментов: термолиз
без МА и микросфер (МС) (образец №1), предварительная МА и последующий термолиз без МС
(образец №2), предварительная МА и последующий термолиз в присутствии МС (образец №3), без
предварительной механоактивации и последующий термолиз с протонодонорной добавкой
тетралином (Т) (образец
№4)
Образцы нефти массой 7,5
г загружали в реактор объемом 12 мл (в инертной среде – азот).
Микросферы зол ТЭЦ добавляли в реакционную смесь в количестве 2
% масс. от навески нефти
(0,15
г). Нагрев до заданной температуры осуществлялся со скоростью 10 °С / мин. Условия
синтеза приведены в таблице 1.
Таблица 1
Условия синтеза
Термолиз (450 °С, 2 ч.)
Каталитические системы Добавки
Образец №
Предварительная обработка
мазута
Наименование Кол-во, % мас. Тетралин, % мас.
1 Мазут без предварительной
обработки
- - -
2 Механоактивация (10 мин) - - -
3 Механоактивация (10 мин) МС 2,0 -
4 Мазут без предварительной
обработки
- - 5
Для оценки выхода светлых фракций в продуктах термолиза нефти использовали
термогравиметрический метод анализа. Термогравиметрический анализ (ТГА) [2] мазута
проводили на дериватографе «Paulik-Paulik-Erdey» Q-1000 фирмы «МОМ» (Венгрия). Пробы
мазута массой 100 мг вносили в тигли и нагревали от комнатной температуры до 600
°С со
скоростью 10
°С / мин. Результаты термогравиметрического анализа представлены в таблице 2 и
на рисунке 1.
Таблица 2.
Результаты термогравиметрического анализа исходного мазута и образцов после термолиза
(номера образцов соответствуют шифру образцов из таб. 1)
Потеря массы образца, %
Исходный мазут Образец № 1 Образец № 2
Пределы выкипания,
º
С
Отд. фр-й Сум. Отд. фр-й Сум. Отд. фр-й Сум.
0 - 100 0,0 0,0 0,0 0,0 0,0 0,0
100 - 150 0,0 0,0 0,0 0,0 0,5 0,5
150 - 200 0,5 0,5 1,5 1,5 0,5 1,0
200 - 250 1,0 1,5 3,5 5,0 2,0 3,0
250 - 300 6,0 7,5 6,5 11,5 19,2 21,2
300 - 350 13,0 20,5 12,0 23,5 18,8 40,0
350 - 400 16,0 36,5 16,0 39,5 36,0 76,0
400 - 450 34,5 71,0 20,5 60,0 3,0 79,0
450-500 11,5 82,5 22,5 82,5 3,5 82,5
172
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
Продолжение таблицы 2.
Исходный мазут Образец № 3 Образец № 4
Пределы выкипания,
0
С
Отд. фр-й Сум. Отд. фр-й Сум. Отд. фр-й Сум.
0 - 100 0,0 0,0 0,0 0,0 0,0 0,0
100 - 150 0,0 0,0 0,0 0,0 0,0 0,0
150 - 200 0,5 0,5 1,0 1,0 1,0 1,0
200 - 250 1,0 1,5 4,0 5,0 4,0 5,0
250 - 300 6,0 7,5 13,0 18,0 13,0 18,0
300 - 350 13,0 20,5 14,0 32,0 14,0 32,0
350 - 400 16,0 36,5 16,0 48,0 16,0 48,0
400 - 450 34,5 71,0 25,0 73,0 25,0 73,0
450-500 11,5 82,5 7,0 80,0 7,0 80,0
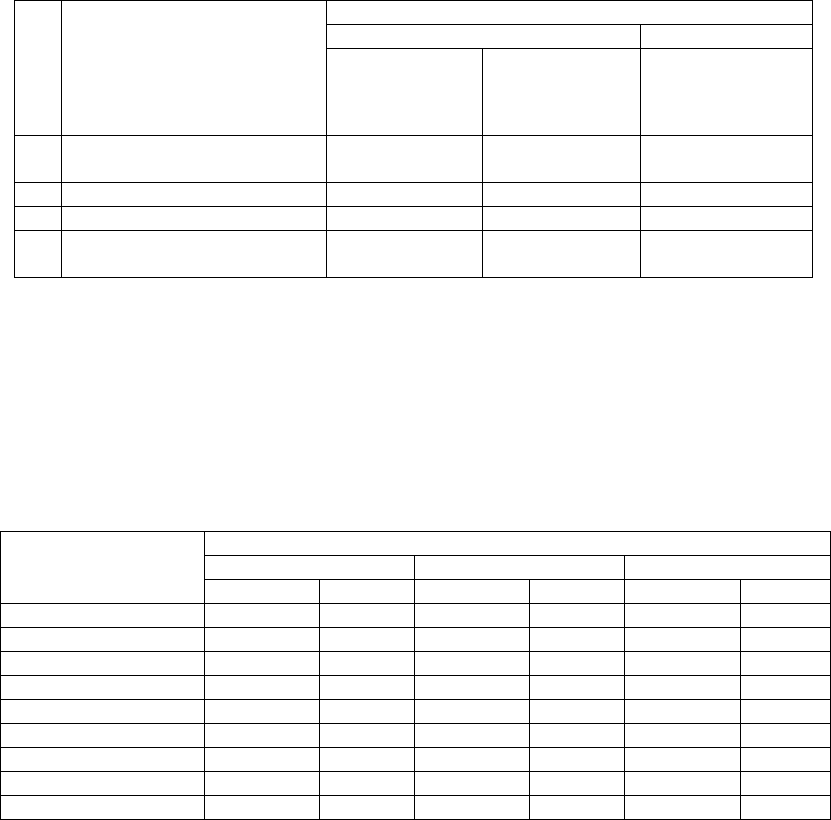
Рис.1 Диаграмма дифференциального изменения массы относительно увеличения температуры
Из данных представленных на рисунках 1 и в таблице 2 видно, что предварительная
обработка приводит к увеличению выхода фракции 250-400
°С. Образец 3 на 12% при 250-300 °С,
образец 2 на 23% при 350 и 400
°С.
Таким образом, сочетание термолиза в присутствии МС и предварительной МА приводит
к увеличению выхода легких фракций из тяжелого нефтяного остатка.
Среднюю молекулярную массу определяли криоскопическим методом в нафталине[3] на
установке “Крион”. Результаты приведены на рисунке 2.
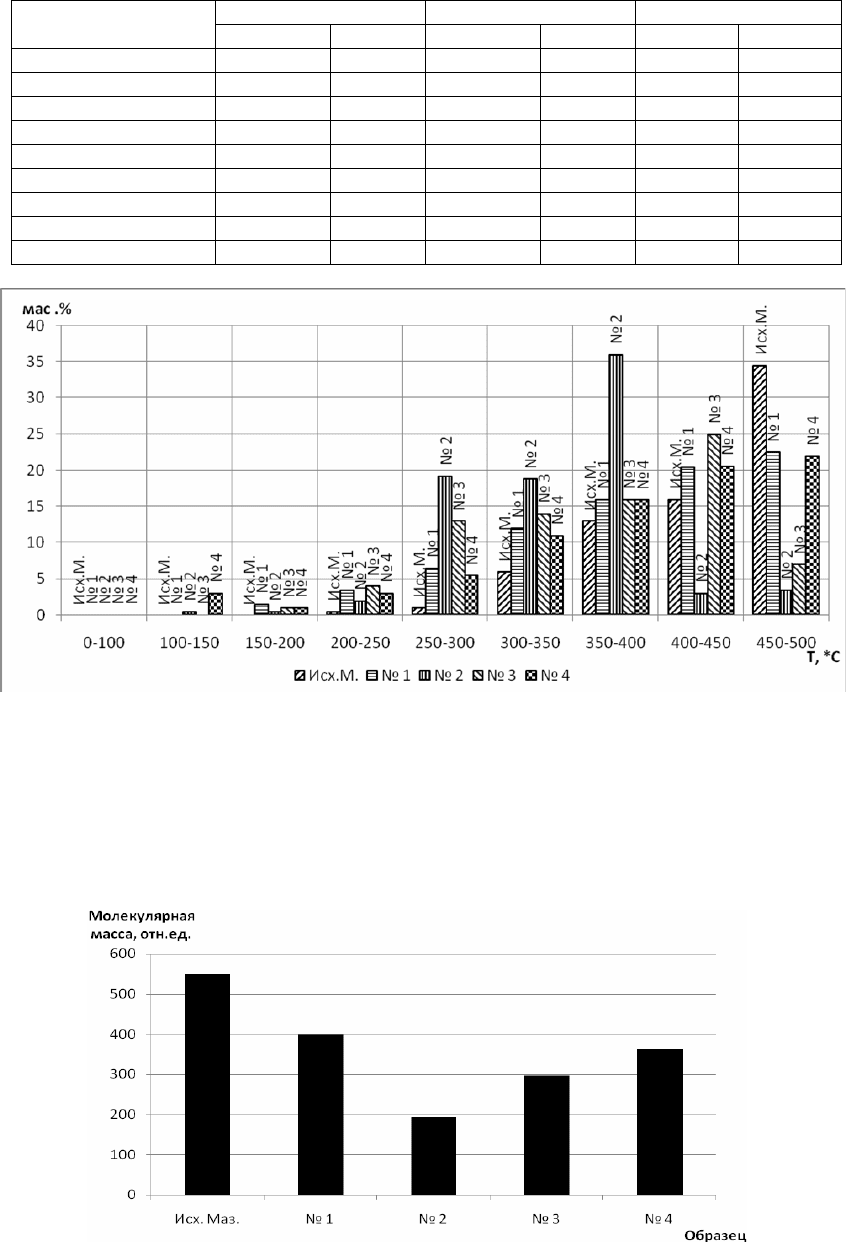
Рис.2 Средние молекулярные массы образцов
173

Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
Из данных приведенных на рисунке 2 видно, что механоактивация снижает среднюю
молекулярную массу более чем в 2 раза.
Содержание углерода и водорода в исследуемых образцах определяли по методике
ВНИИНП, содержание азота – методом Кьельдаля. Общее содержание серы в образцах
устанавливали методом двойного сожжения. Содержание кислорода определяли по разности.
Результаты приведены в таблице 3.
Таблица 3.
Элементный
состав образцов
Содержание элементов, %масс.
Образец
C H N S
О
№ 1
82,34 12,67 0,78 0,16
4,05
№ 2
85,00 13,00 0,58 0,09
1,33
№ 3
85,50 12,00 0,58 0,11
1,81
№ 4
84,60 12,50 0,77 0,15
1,98
Выводы.
1. Механоактивацией исходного образца мазута возможно уменьшить среднюю молекулярную
массу образца почти в 2 раза, что в комплексе с дальнейшей термической обработкой
позволяет увеличить выход легких фракций (выкипающих до 300
º
С) до 13,7% масс, что
объясняется деструкцией высокомолекулярных компонентов образца.
2. До 43% уменьшается количество содержания серы в получаемых продуктах. Данный эффект
достигается за счёт связывания серы оксидом кальция, содержащимся в микросферах зол
ТЭЦ.
Список литературы:
1. Днепровский К.С.. Дисс. Механохимические превращения углеводородов нефти канд. хим.
наук. Томск: Институт химии нефти СО РАН, 2003г., 103с.
2.
Уэндландт У. Термические методы анализа. М.: Мир1987г. 526с.
3.
Богомолов А.И., Темьянко М.Б., Хотынцева Л.И. Современные методы исследования нефтей.
Ленинград: Недра, 1984г. 432с.
УДК 551.510.42
Совершенствование отношений по природопользованию
Л.И. Молодежникова, Ю.А. Чащина
Томский политехнический университет, г. Томск
dekanat@sibmail.com
Проблема совершенствования отношений по природопользованию обусловлена
экологическими трудностями экономического роста, а также ухудшением природных условий
воспроизводства рабочей силы. Суть в том, что, во-первых, растут затраты совокупного труда на
получение элементов природной среды, используемых в производстве; во-вторых, происходят
большие потери общественного труда в результате
нерационального использования сырья,
материалов, топлива, составляющих элементы природной среды; в-третьих, возникает
необходимость выделения значительного количества совокупного труда для ликвидации
негативных последствий воздействия производства на природную среду; в-четвертых, возрастает
дефицит природных условий производства.
Все это ставит на повестку дня вопрос о необходимости совершенствования
экономического механизма защиты окружающей среды.
Одним
из наиболее эффективных инструментов экономико-экологического контроля в
процессе становления рыночной экономики должен стать экологический аудит.
Экологический аудит (ЭА) – инструмент, включающий в себя организационно-
экономические факторы защиты окружающей среды. Он позволяет выбрать оптимальный вариант
природоохранных сооружений, организовать информационно-аналитический контроль за
состоянием и степенью эксплуатации природоохранной техники, дать экономическую оценку
намечаемых
технических и технологических усовершенствований.
174

Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
На ряде тепловых электрических станций был проведен ЭА системы управления в области
охраны окружающей среды на соответствие стандарту ГОСТ Р ИСО 14001-98. Настоящий анализ
проводился в качестве первого этапа программы внедрения системы управления окружающей
средой (СУОС) на станции.
Область применения данного аудита включала в себя определение возможности
интеграции СУОС с существующей на
станциях системой управления в области охраны
окружающей среды, а также возможности использования ряда механизмов управления, как
основы для разработки элементов системы.
В ходе ЭА были выявлены следующие несоответствия:
1. Для исследуемых станций не разработана действующая экологическая политика;
2. Отсутствует процедура по систематической идентификации и оценке экологических
аспектов. Существенные экологические аспекты деятельности станций не
идентифицированы;
•
Не установлены цели и задачи которые основывались бы на приоритетных значимых
экологических аспектах;
3. Нет четкого определения кто, как и какими средствами должен идентифицировать,
устанавливать, контролировать и корректировать цели и задачи;
4. Станциями не разработана(ы) программа(ы) по достижению поставленных целевых и
плановых показателей;
5. Не определены и не документированы роли, ответственность и полномочия работников
станций с учетом их положения в системе управления окружающей средой;
6. Не осуществляется систематическое обучение персонала по значимым экологическим
воздействиям, осведомленность об экологической политике, экологических выгодах и т.д.;
7. В настоящее время на станциях не существует описания СУОС;
8. Не разработана процедура по выявлению потенциальных аварийных ситуаций и
инцидентов, которые могут иметь негативное влияние на окружающую среду;
9. Не соблюдаются в полном объеме требования законодательства по вопросам ГО и ЧС, по
порядку эксплуатации опасных объектов, которые могут потенциально являться
источниками негативного воздействия на окружающую среду в случае аварийной
ситуации;
10. Не определена ответственность конкретных должностных лиц в действующем плане
мероприятий по ликвидации аварийных ситуаций и предотвращению вредных последствий
аварий.
Проведенный на ряде тепловых электрических станций аудит показал, что руководство
станций заинтересовано во внедрении системы управления окружающей средой, соответствующей
стандарту ГОСТ Р ИСО 14001-98. Коллективы станций уже достаточно хорошо используют
механизмы, предлагаемые многими элементами стандарта, но не всеми из этих элементов
занимались с требуемой тщательностью. Для облегчения эффективного внедрения СУОС
рекомендуется предпринять следующие шаги:
1. Основываясь на результатах предварительного анализа (после выявления значимых
экологических аспектов), провести всестороннее обучение сотрудников предприятий в
области экологических аспектов и воздействий. Это обучение должно быть
дифференцированным для каждого подразделения предприятий и пройти его должны все
сотрудники, которые могут стать причиной возникновения или способствовать уменьшению
экологических воздействий.
2. Предполагается использовать результаты данной проверки и сделанные рекомендации, для
исследования всех других областей, где они могут быть с пользой применены. Необходимо
обеспечить, чтобы были определены процедуры для эффективного управления операциями,
связанными с воздействиями на окружающую среду во всех важных областях при поддержке
обученного персонала на различных уровнях организации.
3. При документировании и внедрении СУОС необходимо использовать в качестве основы уже
существующие на станциях структуры и механизмы. Это может включать элементы системы
управления, существующую организационную структуру и разграничение ответственности,
существующие операционные процедуры, инструкции и т.д.
4. Подготовить экологических аудиторов и проводить внутренние экологические аудиты для
создания и повышения осведомленности о СУОС во всех подразделениях станций.
Обеспечьте, чтобы линейное руководство своевременно предпринимало корректирующие
действия, направленные на устранение основных причин возникновения несоответствий.
175

Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
5. Необходимо широко использовать механизмы улучшения системы (регистрация и устранение
несоответствий, корректирующие и предупреждающие действия, внутренние экологические
аудиты и анализ со стороны руководства) для демонстрации преимуществ и
жизнеспособности СУОС.
6. При документировании СУОС нужно точно следовать духу и букве положений стандарта, а
также руководства по использованию требований стандарта, приведенном в приложении к
стандарту ГОСТ Р ИСО 14001.
7. Последнее, и также очень важное: обеспечить обязательство и поддержку руководителей
высшего звена внедрению системы УОС! Демонстрация финансовых выгод, которые эта
система может принести предприятию, является наилучшим способом достижения этой цели.
Таким образом, если следовать вышеприведенным рекомендациям можно не только
содействовать улучшению экологических параметров большого числа субъектов
производственной деятельности и снижению непосильной для окружающей среды техногенной
нагрузки, но и общему оздоровлению экономики предприятий.
Список литературы:
1. ГОСТ 24525.4-80. Управление охраной окружающей среды. Управление производственным
объединением и промышленным предприятием. Основные положения.
2.
ГОСТ Р ИСО 14001-98 Системы управления окружающей средой. Требования и руководство
по применению.
3.
ГОСТ Р ИСО 14004-98 Системы управления окружающей средой. Общие руководящие
указания по принципам, системам и средствам обеспечения функционирования.
4.
Охрана труда и социальное обеспечение. №№1-10, 2000.
УДК 628.5
Исследование физико-химических характеристик сахаптинского цеолита
П.А. Дуданова , О.Б. Назаренко, Р.Ф. Зарубина
Томский политехнический университет, г. Томск
obnaz@mail.ru
В последние десятилетия наблюдается ухудшение качественных показателей состояния
водных объектов, используемых для хозяйственной деятельности. Это связано с увеличением
объемов сброса в них сточных вод, содержащих большое количество вредных веществ, в том
числе и аммонийный азот [1, 2].
Аммонийный азот, являясь первичным загрязнителем, окисляется до нитратов и нитритов,
неблагоприятно влияющих на здоровье человека
и окружающую среду. Сброс соединений азота с
хозяйственно-бытовыми, промышленными, сельскохозяйственными стоками приводит к
эвтрофикации природных водоемов, к уменьшению содержания растворенного кислорода,
оказывает токсическое влияние на рыб, способствует усиленной коррозии распределительных
систем водоснабжения. Поиск эффективных методов удаления иона аммония является одной из
важнейших проблем водоочистки.
Традиционные методы очистки воды от
аммонийного азота имеют ряд недостатков [3] и
могут эффективно использоваться при определенных концентрациях аммония: менее 10 мг/л –
хлорирование, более 100 мг/л – метод отдувки воздухом, химическое осаждение. Если в 70-е г.г.
XX в. концентрация аммиака в городских сточных водах составляла 1,9–13 мг/л, иона аммония –
до 2,2 мг/л [4], то в настоящее время содержание
аммонийного азота (NH
4
+
+ NH
3
) значительно
выше – 20–50 мг/л [1]. В основе технологической схемы большинства очистных сооружений
лежит биологический метод очистки. Биологическая очистка не обеспечивает эффективного
удаления азотсодержащих веществ в современных условиях – снижение концентрации
аммонийного азота составляет не более 20–40 %. Это объясняется изменением качественных и
количественных характеристик сточных вод, поступающих на очистку, и изношенностью
технологического оборудования, которое
было построено по типовым проектам 40–45 лет назад и
соответствует природоохранным нормативам того времени.
В данной работе представлены результаты исследования физико-химических
характеристик природного цеолита Сахаптинского месторождения Красноярского края, показана
возможность его использования для очистки воды от аммонийного азота.
Природные цеолиты являются широко распространенным и дешевым минеральным
сырьем, обладают уникальным спектром физико
-химических, адсорбционных и ионообменных
176
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
свойств, благодаря чему они нашли широкое применение во многих отраслях народного
хозяйства, в том числе и в практике очистки сточных вод [5–7].
Цеолиты представляют собой группу природных минералов, кристаллический
трехмерный каркас которых состоит из алюмокремнекислородных тетраэдров (Si,Al)О
4
.
Поскольку часть четырехвалентных ионов кремния замещена трехвалентными ионами алюминия,
каркас имеет отрицательный заряд, который нейтрализуется присутствием на стенках полостей
катионов натрия, калия, кальция, магния и других металлов. Кроме того, внутренние полости и
соединяющие их каналы заполнены молекулами так называемой цеолитной воды. Суммарный
объем полостей и соединяющих их каналов в цеолитах
составляет около 50 % объема кристалла, а
диаметр этих каналов на поверхности кристалла варьирует от 0,26 до 0,80 нм. Катионы металлов и
молекулы воды способны свободно удаляться и поглощаться структурой, благодаря чему
происходит ионный обмен.
Структурная формула цеолита может быть представлена следующим образом [7]:
М
m/n
[(AlO
2
)
x
(SiO
2
)
y
] · zH
2
O,
где x+y – сумма тетраэдров в элементарной ячейке, m – число катионов М (калия, натрия, кальция,
магния), n – валентность катиона.
Группа природных цеолитов включает около 30 минералов. По литературным данным
[5, 6] наибольшей избирательностью к ионам больших размеров, в частности, к иону аммония,
обладает клиноптилолит: (К
2
, Na
2
, Ca) [Al
2
Si
7,5-11,0
O
19,0-26,0
] (6-8)H
2
O. Обменные катионы Na
+
,
расположенные в больших полостях клиноптилолита, легко замещаются в водных растворах солей
на ион аммония [6]. Поэтому, чем больше фазы клиноптилолита содержится в цеолите, тем лучше
он очищает воду от аммонийного азота.
Цеолитовые породы широко распространены и используются в водоочистке во многих
странах мира [6]. Каждое цеолитовое месторождение характеризуется своими, присущими только
ему,
минералогическим coставом и физико-химическими свойствами. Поэтому перед
применением цеолитового сырья требуется подробное исследование его физико-химических
свойств и адсорбционных характеристик.
Для исследований свойств сахаптинского цеолита использовались следующие методы
анализа: рентгенофазовый анализ (РФА), термический анализ, инфракрасная (ИК) спектроскопия,
химический анализ.
Минералогический состав сахаптинского цеолита определялся по рентгенограмме, снятой
на дифрактометре ДРОН
-3 с использованием рентгеновской трубки БСВ-9 с CuK
α
-излучением.
Термический анализ проводился на ТГА/ДСК/ДТА анализаторе SDT Q600 при скорости нагрева
на воздухе до 1000 °C около 10 °C/мин. Спектры поглощения образца цеолита в инфракрасной
области спектра (4000–400 см
-1
) были сняты на ИК-Фурье спектрометре Nicolet 5700.
Концентрацию ионов аммония в воде определяли фотометрическим методом с реактивом
Несслера. Интенсивность окраски раствора измеряли с помощью фотоэлектроколориметра КФК-2
при длине волны 400 нм в кювете с толщиной слоя 2 см.
Согласно данным РФА исследуемый образец содержит в своем составе 45–50 %
клиноптилолита, гейландит, а также примесные породы –
кварц, монтмориллонит, полевой шпат и
кристобалит.
В ходе термического анализа в структуре природного цеолита не обнаружено
существенных изменений. Установлено, что кривая дегидратации как функция температуры
является плавной, что характерно для фазы клиноптилолита [8]. Исследуемый цеолит содержит в
своем составе связанную и сорбированную воду. Потеря веса при нагревании образца природного
цеолита до 1000 °С
составляет 9,22 %, причем максимальная потеря массы ~6 % наблюдается в
температурном диапазоне от 80 до 300 ˚С. Изменение структуры цеолита начинается с 750 ˚С, а
свою устойчивость образец теряет при температуре выше 1000 ˚С. Результаты термического
анализа и литературные данные позволяют предположить, что для улучшения ионообменных
свойств сахаптинского цеолита можно проводить термическое модифицирование в температурном
диапазоне
250–350 ˚С.
Наличие характерных для фазы клиноптилолита [8] структурных групп в образце
сахаптинского цеолита установлено методом инфракрасной спектроскопии. Наиболее
интенсивный пик наблюдается для полосы поглощения 1046 см
−1
, отвечающей колебанию связи
Si–O–Si. Пики поглощения 800,5 и 780, 5 см
−1
связаны с валентными колебаниями связи Al–O, а
473,2 см
−1
– с деформационными колебаниями Al–O
4
. С наличием цеолитной воды связаны
следующие полосы поглощения: 3638,6 см
−1
– полоса связанных водородной связью с кислородом
каркаса ОН-групп, 3406,1, 3249,2 и 3184,6 см
−1
– полосы антисимметричных и симметричных
177
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
валентных колебаний изолированных ОН-групп, 1612,4 см
−1
– полоса деформационных
колебаний молекул воды.
Эксперименты по очистке модельного раствора от аммонийного азота на фильтре с
цеолитовой загрузкой проведены с помощью исходного сахаптинского цеолита и цеолита,
переведенного в Na-форму обработкой раствором хлорида натрия. В экспериментах
использовалась предварительно отсеянная на сите фракция цеолита размером 1–2 мм. Объем
цеолита в фильтре составлял 80 мл.
Для первого эксперимента был приготовлен раствор хлористого аммония на
водопроводной воде с концентрацией аммония 20 мг/л. Для анализа производили отбор каждых
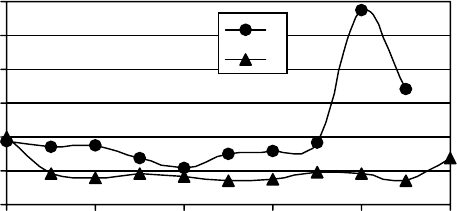
последовательных 100 мл отфильтрованной воды. Результаты измерения концентрации ионов
аммония в фильтрате представлены на рис. 1. Концентрация ионов аммония в растворе снижается
на 42,5 %. Дальнейшее увеличение ионов аммония может быть связано с их
выносом быстрым
потоком воды из относительно малого объем цеолита в фильтре. Для второго эксперимента цеолит
был переведен в Na-форму пропусканием через фильтр раствора хлорида натрия. Модельный
раствор хлористого аммония был приготовлен на дистиллированной воде с концентрацией ионов
аммония 5 мг/л. Результатом модифицирования цеолита раствором хлорида натрия является
улучшение его ионообменных
свойств. Концентрация ионов аммония в этом случае снизилась на
69,4 %.
0
0,5
1
1,5
2
2,5
3
0 200 400 600 800 1000
V, мл
С/С
0
1
2
Рис. 1. Зависимость концентрации ионов аммония в фильтрате от объема модельного раствора,
прошедшего через фильтр с цеолитом: 1 – природным (исходная концентрация NH
4
+
– 20 мг/л); 2 –
модифицированным хлоридом натрия (исходная концентрация NH
4
+
– 5 мг/л)
Таким образом, в ходе проведенных исследований была показана возможность
использования природного цеолита Сахаптинского месторождения Красноярского края для
очистки воды от аммонийного азота. На основании изучения физико-химических свойств данного
минерала можно предложить для увеличения эффективности процесса очистки провести
химическое и термическое модифицирование.
Список литературы:
1. Хенце М., Армоэс П., Ля-Кур-Янсен И., Арван Э. Очистка сточных вод. М.: Мир, 2004. 480 с.
2. Иевлева О.С., Гончарук В.В. Методы удаления нитратов из природных и питьевых вод // Химия и
технология воды. 2006. Т. 28. № 3. С. 256–273.
3. Яковлев С.В. Водоотведение и очистка сточных вод. М: Стройиздат, 1996. 591с.
4. Грушко
Я.М. Вредные неорганические соединения в промышленных сточных водах:
Справочник. Л.: Химия, 1979. 160 с.
5. Тарасевич Ю.И. Природные сорбенты в процессах очистки воды. Киев: Наукова думка, 1981.
207 с.
6. Челищев Н.Ф., Володин В.Ф., Крюков В.Л.. Ионообменные свойства природных
высококремнистых цеолитов. М.: Наука, 1988. 128 с.
7. Минералогическая энциклопедия / Под ред. К.
Фрея. Л.: Недра, 1985. 512 с.
8. Брек Д. Цеолитовые молекулярные сита. М.: Мир, 1976. 781 с.
178
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
Экономическая оценка ущербов здоровью человека на производстве
Л.Т. Рязанцева, В.И. Федянин, Е.А. Ушакова
Воронежский государственный технический университет, г. Воронеж
RyazancevaLT@mail.ru
Под оценкой ущерба (вреда) здоровью понимается всесторонняя характеристика влияния
как конкретных потенциально вредных воздействий, так и различных политических, научно-
технических и технологических программ или проектов на состояние здоровья людей с
использованием комплекса количественных методов установления ожидаемой частоты нарушений
состояния здоровья, ухудшений условий и
качества жизни человека [1].
Одним из основных положений оценки ущерба (вреда) здоровью населения при
чрезвычайных ситуациях является необходимость относительно точного установления числа
атрибутивных (т. е. обусловленных анализируемым воздействием) случаев тех или иных
нарушений состояния здоровья.
Многими зарубежными странами и международными организациями для оценки
эффективности государственных программ по охране атмосферного воздуха, планирования
мероприятий
по снижению загрязнения атмосферного воздуха автотранспортом и др. широко
используется методология оценки риска, рассматриваемая сегодня как один из наиболее
эффективных инструментов научного обеспечения принятия управленческих решений.
Оценка ущерба основывается исключительно на критериях, отражающих
непосредственное влияние химических веществ на здоровье различных групп населения (факторы
канцерогенного потенциала, параметры зависимости экспозиция-ответ, полученные
в
эпидемиологических исследованиях).
Ущерб здоровью населения непосредственно выражается в дополнительной
заболеваемости и смертности, связанной с воздействием факторов окружающей среды.
Принципиальный вопрос оценки ущерба здоровью – это перевод натуральных показателей ущерба
здоровью в стоимостные. В связи с этим получили развитие две основные концепции
экономической оценки ущерба: концепция стоимости человеческой жизни и концепция стоимости
груза болезней [2].
Существует несколько методологических подходов к оценке стоимости статистической
жизни человека и широкого спектра различных вредных эффектов. Вместе с тем использование
каждого из подходов в целях такой оценки связано с рядом условностей и ограничений. Оценка
стоимости статистической жизни (года жизни) на основе потерь индивидуального дохода дает
весьма низкие значения,
не отражающие реальные масштабы ущерба здоровью. Это связано,
главным образом, с низким уровнем денежных доходов населения. Сходные проблемы возникают
и при оценке стоимости статистической жизни на основе тех потерь, которые несет общество в
результате дополнительной заболеваемости и смертности. Общество недополучает из-за
дополнительной заболеваемости и смертности часть общественного продукта и, кроме
того, несет
затраты на лечение. Однако, во-первых, размер таких потерь в денежном выражении зависит от
уровня развития экономики; во-вторых, потери индивида и общества могут не совпадать.
Еще одним способом оценки стоимости статистической жизни является использование
размеров оплаты труда за профессиональный риск. Поскольку лица опасных профессий получают
более высокую
оплату, то стоимость статистической жизни исчисляется на основе
дополнительной оплаты за дополнительный риск. Этот метод весьма широко используется в
развитых странах, однако с учетом экономических реалий России он опять же оказывается мало
применим для целей оценки ущерба здоровью.
В международных проектах широко используются оценки стоимости статистической
жизни, основанные на готовности населения
платить за снижение риска развития опасных
заболеваний, сохраненный год жизни и т. д. Метод, называемый “benefer transfer”, позволяет на
этой основе перевести значения готовности платить, полученные для какой-либо страны, на
условия другой страны. Обычно предполагается, что в развитых странах готовность платить за год
сохраненной жизни составляет 100 000 долларов [3].
В России, по данным The Vienna Institute for International Economic Studies,
годовой ВВП
на душу населения составил в 2001 г. 8320 долларов по паритету покупательной способности.
Исходя из сравнения ВВП на душу населения и стоимости статистической жизни в США и ЕС
(соответственно 4 800 000 и 3 100 000 долларов), стоимость статистической жизни в России
составляет 1 444 800 долларов. Стоимость одного потерянного года жизни в результате острой
смерти или смерти от
хронического заболевания соответственно равна 54 172 и 39 298 долларов.
179
Секция 4
ЭНЕРГЕТИКА: ЭКОЛОГИЯ, НАДЕЖНОСТЬ, БЕЗОПАСНОСТЬ
Разработка методических подходов к оценке ущербов осуществляется также путем
проведения характеристики реальных ситуаций. В частности, при оценке возможных
экономических потерь осуществлялся с использованием трех способов оценки стоимости
человеческой жизни:
1-й способ: 54 000 долларов (по обменному курсу и предположению о сокращении
продолжительности жизни на 30 лет);
2-ой способ: 204 000 долларов (по ППС и предложению
о сокращении продолжительности
жизни на 30 лет);
3-й способ: 1 444 800 долларов (по ППС, общее население).
Данные методические подходы оценки ущербов здоровью населения от воздействия
факторов окружающей среды позволяют создать основу для разработки подходов к сравнительной
оценке медико-социальной и экономической значимости спектра эффектов, вызываемых
воздействием факторов окружающей среды, что чрезвычайно важно при
формировании
правильной экономической политики в области охраны окружающей среды и здоровья населения.
Весьма перспективным в целях прогнозирования риска развития патологии является
подход, основанный на оценке состояния основных систем иммунитета человека. В настоящее
время уже общепризнанным является тезис о чрезвычайно выраженной чувствительности
иммунной системы к разнообразным неблагоприятным воздействиям, что позволяет выявить
ранние признаки таких влияний. При этом истинное состояние иммунной системы отражают не
только и не столько количественные и качественные дефекты конкретных показателей, сколько
взаимосвязи между различными компонентами. Поэтому актуален поиск неких интегральных
показателей, которые окажутся информативными для оценки состояния иммунного статуса при
прогнозировании течения заболевания и возможности его развития.
Прогнозирование нарушений
состояния здоровья у работающих в условиях воздействия
химических веществ наряду с оценкой условий труда возможно лишь на основе
целенаправленного изучения как анамнестических данных, так и ряд клиническо-функциональных
и лабораторных показателей при проведении периодических медицинских осмотров. При этом
должны учитываться уровень фактических концентраций химических веществ и кратность
превышения ПДК.
В
качестве прогностических критериев риска развития нарушений здоровья у работающих
можно использовать 4 градации уровней загрязнения воздушной среды: группа KR0 – воздействие
факторов малой интенсивности (не выходящий за пределы гигиенических нормативов), группа
KR1 – воздействие факторов средней интенсивности (превышение ПДК в пределах одного
порядка), группа KR2 – воздействие факторов высокой интенсивности (превышение ПДК в 10-100
раз), группа
KR3 – воздействие факторов экстремального уровня (в 100 раз и более выше ПДК).
Для прогнозирования ожидаемой частоты случаев профессиональных заболеваний среди
работающих в контакте с нейротропными веществами со стажем работы более 3 лет
целесообразно учитывать уровень средних концентраций этих веществ в воздухе рабочей зоны и
коэффициент (1,83), рассчитанный на основе корреляционно-регрессионного анализа зависимости
частоты выявленной профпатологии от уровня средних концентраций веществ в воздухе. При
возрастании воздействующих на работающих концентраций химических веществ в воздухе в n-ое
количество раз по отношению к ПДК риск развития профессионального заболевания будет
определяться по формуле:
KR = n – 1,83 ,
где n – кратность превышения ПДК.
Прогностическим критерием риска возникновения заболевания в условиях воздействия
антропогенных факторов химического происхождения может служить интегральный
иммунологический параметр (ИП). Он основан на оценке функционирования иммунной системы
лиц, подвергающихся воздействию вредных веществ производственной среды, с помощью
большого числа показателей, характеризующих различные стороны иммунного ответа.
Использование при вычислении ИП математического подхода позволяет осуществлять
автоматизированный отбор диагностически значимых показателей для выявления
неблагоприятного влияния
факторов химической природы, определять количественные значения
ИП на основе минимального набора иммунологических показателей для различных
нозологических форм патологии и устанавливать граничные (пороговые) его величины,
превышение которых является аргументом для отнесения обследованных к группе риска развития
соответствующей патологии.
180
