Стась Н.Ф. Введение в химию. Учебное пособие
Подождите немного. Документ загружается.

2.6. Взаимосвязь между классами веществ
Между классами веществ существует возможность их взаимного
превращения: из простых веществ получают оксиды, из оксидов – осно-
вания или кислоты, из кислот – соли. Возможен и обратный переход от
солей к основаниям или кислотам, от оснований или кислот к оксидам, а
от оксидов к простым веществам.
Пример 2.1. Напишите уравнения реакций для осуществления цепочки пр
вращений:
Решение.
авнения реакций для осуществления цепочки пре-
вращений:
Решение.
тво из дру-
гого
меди (II).
с ым
о и:
е-
Ca
→ CaO → Ca(OH)
2
→ CaSO
4
1. 2Ca + O = 2CaO.
2
2. CaO + H
2
O = Ca(OH)
2
.
3. Ca(OH)
2
+ H
2
SO
4
= CaSO
4
↓ + H
2
O.
Пример 2.2. Напишите уравнения реакций для осуществления цепочки пре-
вращений:
P
→ P
4
O
10
→ H
3
PO
4
→ KН
2
PO
4
→ K
2
НPO
4
→ K
3
PO
4
Решение.
1. P
4
+ 5O
2
= P
4
O
10
.
2. P
4
O
10
+ 6H
2
O = 4H
3
PO
4
.
3. H
3
PO
4
+ KOH = KН
2
PO
4
.
4. KН
2
PO
4
+ KOH = K
2
НPO
4
.
5. K
2
НPO
4
+ KOH = K
3
PO
4
.
Пример 2.3. Напишите ур
CuSO
4
→ Cu(OH)
2
→ CuO → Cu
1. CuSO
4
+ 2NaOH = Cu(OH)
2
↓ + Na
2
SO
4
.
2. Cu(OH)
2
= CuO + H
2
O.
3. CuO + H
2
= Cu + H
2
O.
Подобная связь классами соединений, позволяющая получать ве-
щество одного класса из вещества другого класса, называется генетиче-
ской. Но необходимо иметь в виду, что не всегда одно вещес
можно получить напрямую. Например, гидроксид меди Cu(OH)
2
нельзя получить взаимодействием оксида меди (II) с водой. Тогда при-
меняют косвенный путь: на оксид меди (II) действуют кислотой и полу-
чают соль, а из соли действием щелочи получают гидроксид
Генетическую
сое но п
вязь между основн
каз еск
и классами неорганических
динений мож
ать схематич
59
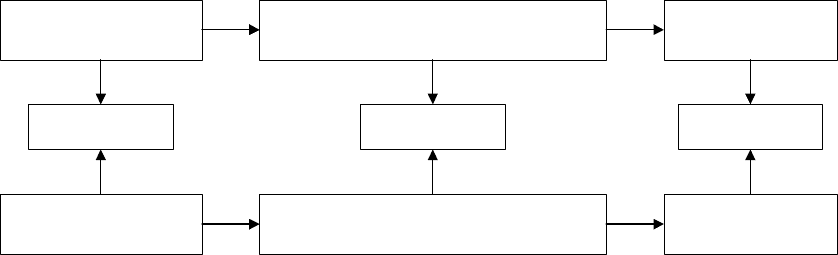
Основной или амфотерный
Металл Основание
оксид
Соль Соль Соль
Неметалл К сидислотный ок Кислота
овремен-
но связаны с атомами формула простей-
ших гидроксидов Э
Деление гидр еделяется их дис-
соци
+ –
оснований,
О си
рво -
шой полярно-
ки-
лот ни
ют одновременно
.
Тип ди и (степени
–О упрочняет-
силиваю
O
4
HClO
4
о с
2.7. Современный подход
к классификации оснований и кислот
Химия, как и вся наука, быстро развивается. По мере её развития
пересматриваются многие понятия. Пересматриваются взгляды и на
классификацию неорганических соединений.
В настоящее время основания и кислоты рассматриваются как со-
единения одного класса – гидроксиды, т.е. продукты присоединения во-
ды к оксидам (дословно: водные оксиды). Все гидроксиды имеют в сво-
ём составе один или несколько атомов кислорода, которые одн
водорода и емента. Общая
.
эл
ОН
оксидов на основания и кислоты опр
ацией при растворении в воде. Характер диссоциации зависит от
сравнительной прочности и полярности связей Э–О и О–Н и может
протекать по двум типам:
1) ЭОН = Э + ОН - по типу
2) ЭОН = Н
+
+ ЭО
–
- по типу кислот.
-Гидроксиды, в которых связь Э– льно полярна и имеет неболь
прочность, диссоциируют по пе му типу – это типичные осношую
вания. Гидроксиды, в которых связь Э–О обладает неболь
стью, но большей, чем связь О–Н, прочностью, диссоциируют как
ы. Но у многих гидроксидов обе связи мало отличаются по степес
полярности и по прочности, поэтому они диссоцииру
по обоим типам – это амфотерные основания или амфолиты
ссоциации гидроксида зависит от валентност
окисления) элемента. С увеличением валентности связь Э
ся, а связь О–Н ослабевает. Поэтому кислотные свойства гидроксидов
тся в периодах периодической системы: у
NaOH Mg(OH)
2
Al(OH)
3
Si(OH)
4
H
3
PO
4
H
2
S
н о в а н и я а м ф о л и т ы к и с л о т ы,
60
ослабевают в группах:
ы основание,
его ва-
лентн
о с .
ений
На пра и у ебно меняются ис-
торически м все при-
жении 8 приведены наиболее часто встречающиеся тривиаль-
ные в, в
приложении
названия см
1. Ка
идроксомеди (II) 4. Дигидрокарбонат меди (II)
2. Ка
1. C O
4
основные соли?
3
, CO
2
3. CO
2
, BaO, SiO
2
Н
3
ВО
3
Al(OH)
3
Ga(OH)
3
In(OH)
3
Tl(OH)
3
кислота а м ф о л и т
а у гидроксидов одного элемента у иливас ются при увеличении
ости:
Mn(OH)
2
Mn(OH)
3
Mn(OH)
4
H
2
MnO
4
HMnO
4
н о в а н и я амфолит к и с л о т ы
2.8. Тривиальные названия неорганических соедин
ктике, в технической ч й литературе при
сложившиеся названия (тривиальные), к которы
выкли, и от которых пока нет смысла отказываться, например: углекис-
лый газ (CO
2
), бертолетова соль (KClO
3
), поваренная соль (NaCl) и т.д.
В прило
названия наиболее распространённых неорганических вещест
9 – названия минерало а в приложении 10 – тривиальные
есей, часто используемых в химической практике.
в,
2.9. Тест для самоконтроля
(ответы можно сверить с приложением 2)
Из приведённых после каждого вопроса ответов необходимо найти
только один правильный ответ. Составленную таблицу ответов можно
сверить с ответами в приложении 2.
кое название соответствует соли (CuOH)
2
CO
3
?
1. Гидрокарбонат меди (II) 2. Карбонат гидроксомеди (II)
3. Карбонат диг
кое вещество имеет название гидрофосфат кальция?
a
3
(PO
4
)
2
2. Ca(H
2
PO
4
)
2
3. (CaOH)
3
PO
4
4. CaHP
3. Ка
1. HCl 2. HNO
3
3. H
2
S 4. HClO
4
4. Какие основания могут образовывать
кая из кислот может образовывать кислые соли?
1. NaOH 2. KOH 3. Ca(OH)
2
4. Cu(OH)
2
5. В каком списке содержатся только кислотные оксиды?
1. K
2
O, MnO
2
, SO
2
2. P
2
O
5
, SO
61
6. Какое основание обладает ам и свойствами?
1. La(OH 4. LiOH
7. Какое
9. Ка
собо
та.
фотерным
) 2. Mg(OH) 3. Al(OH)
3 2 3
основание относится к щелочам?
1. Al(OH)
3
2. Mg(OH)
2
3. Zn(OH)
2
4. Ca(OH)
2
8. С каким веществом будет взаимодействовать гидроксид натрия?
1. CaO 2. Na
2
O 3. CO
2
4. CaCO
3
кое взаимодействие является реакцией нейтрализации?
1. BaCl
2
+ H
2
SO
4
→ 2. Na + H
2
SO
4
→
3. NaOH + CO
2
→ 4. KOH + H
2
SO
4
→
10. В какой паре вещества могут химически взаимодействовать между
й?
1. SO
3
и HNO
3
2. CO
2
и NO
2
3. CaO и P
2
O
5
4.CaO и BaO
2.10. Упражнения для самостоятельной работы
(выполненные решения можно сверить с приложением 2)
Для закрепления знаний по данной теме рекомендуется самостоя-
тельно выполнить пять упражнений.
1. Распределите по классам и группам и напишите названия соеди-
нений: CaSO
4
, MgO, CaCl
2
, Na
2
HPO
4
, H
2
SO
3
, H
2
S, Pb(OH)
2
, N
2
O
5
,
Mg(OH)Cl, Fe(OH)
3
, KHCO
3
.
2. Какие из 10 оксидов непосредственно взаимодействуют с водой:
BaO, SO
3
, CaO, SiO
2
, P
2
O
5
, Fe
2
O
3
, Al
2
O
3
, Na
2
O, NO
2
, ZnO? Напишите
уравнения реакций.
3. Напишите уравнения реакций для цепочки превращений:
K → K
2
O
2
→ K
2
O → KOH → KHSO
4
→ K
2
SO
4
→ BaSO
4
.
4. Напишите уравнения реакций для цепочки превращений:
железо → нитрат железа (III) → гидроксид железа (III) → оксид
железа (III) → железо → сульфат железа (II) → гидроксид железа (II) →
гидроксид железа(III) → феррит калия.
5. Концентрированная серная кислота, гидроксид натрия, гидро-
ксид калия и фосфорный ангидрид применяются для осушки газов. Ка-
кие из них можно, а какие нельзя использовать для осушки углекислого
газа? Приведите обоснование отве
62
Глава 3
ПЕРИОДИЧЕСКАЯ СИСТЕМА
ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д.И. МЕНДЕЛЕЕВА
ия периодического зако-
на и соз чности
свойств эл ы од-
ной
Ответы и строения
атомов. В 19 . Мозли) и
было
нципиально не измени-
лась
Периодическая система – это естественная систематизация и клас-
сификация химических элементов, разработанная выдающимся русским
химиком Д.И. Менделеевым на основе открытого им периодического
закона. Периодическая система является графическим отображением
периодического закона, его наглядным выражением.
Периодический закон был открыт Д.И. Менделеевым (1869) в ре-
зультате анализа и сопоставления химических и физических свойств 63-х
известных в то время элементов. Его первоначальная формулировка:
свойства элементов и образованных ими простых и сложных веществ
находятся в периодической зависимости от атомной массы элементов.
Разрабатывая свою систему, Д.И. Менделеев уточнил или исправил
валентность и атомные массы некоторых известных, но плохо изучен-
ных элементов, предсказал существование девяти еще не открытых
элементов, а для трёх из них (галлий, германий, скандий) описал ожи-
даемые свойства. С открытием этих элементов (1875–1886 г.г.) перио-
дический закон и периодическая система получили всеобщее признание
и легли в основу всего последующего развития химии.
На протяжении почти 50 лет после открыт
дания периодической системы сама причина периоди
ементов была неизвестна. Было неясно, почему элемент
группы имеют одинаковую валентность и образуют соединения с
кислородом и водородом одинакового состава, почему число элементов
в периодах не одинаковое, почему в некоторых местах периодической
системы расположение элементов не соответствует возрастанию атом-
ной массы (Аr – К, Co – Ni, Te – I).
на все эти вопросы были получены при изучени
14 г. были определены заряды атомных ядер (Г
установлено, что свойства элементов находятся в периодической
зависимости не от атомной массы элементов, а от положительного за-
ряда ядер их атомов. Но после изменения формулировки периодиче-
ского закона форма периодической системы при
, так как атомные массы элементов увеличиваются в той же после-
довательности, что и заряды их атомов.
В этом пособии мы не рассматриваем строение атомов (оно изуча-
ется по программе университетского курса химии), поэтому закономер-
ности изменения свойств атомов, элементов и соединений приводятся
без теоретического обоснования.
63
3.1. Основные формы периодической системы
Существует около 500 вариантов периодической системы, но наи-
более распространены две: 18-клеточная и 8-клеточная
В 18-клеточной периодической системе элементы размещены со-
гласно строению электронных оболочек их атомов, но часть элементов
вынесена из таблицы и приведены внизу в виде приложения, а их место
в системе обозначено звездочками. Эта форма периодической системы
приведена в приложении 4 и в рекомендуемом справочнике (стр. 5). Она
рекомендуется для повсеместного использования.
В 8-клеточной форме большие периоды (4-й, 5-й, 6-й и 7-й), содер-
жащие по 18 элементов, разделены в соотношении 10 : 8, и вторая часть
размещена под первой. Таким образом, большие периоды состоят из
двух рядов (строк) каждый. В этом варианте в периодической системе
имеется восемь групп, и каждая из них состоит из главной и побочной
подгруппы. Главные подгруппы содержат по 5-6 элементов, а побочные
– п 3–4 элемента, кром ой побочная подгруп-
па состои иодиче-
ской сист . 4. Она
комп
3.2. Периодические свойства химических элементов
С и ха-
рактери зации,
в ле элек риц ост ал э
законом со ся свойств
п ты ств мичес един й.
.2.1 мны ные иус ент
Ра атом ионо риод мен я, т лект
о оч а и на к посл ующе мент пери
сравнени предшествующ тняется из чения заряда
ра и
строения
о е восьмой группы, в котор
т из девяти элементов – трех «триад». Эта форма пер
емы приведена в приложении 5 и в справочнике на стр
актна и потому более удобна для пользования, но в ней нет того
однозначного соответствия между формой и электронным строением
атомов, которое присуще 18-клеточной форме.
периодическим законом лучше всего согласуются свойства
стики атомов: атомные и ионные радиусы, энергия иони
сродст
тов. Но
о к э
с периоди
ктрону,
ческим
троот ательн
гласуют
ь и в
также
ентность
многие
лемен-
а
рос х веще и хи ких со ени
3 . Ато е и ион рад ы элем ов
диусы ов и в в пе ах у ьшаютс .к. э ронная
бол ка атом
ю с
ли ио аждого
им упло
ед го эле
-за увели
а в оде по
яд-
увеличения притяжения электронов к ядру.
Радиусы в группах увеличиваются, т.к. атом (ион) каждого элемен-
та отличается от вышестоящего появлением нового электронного слоя.
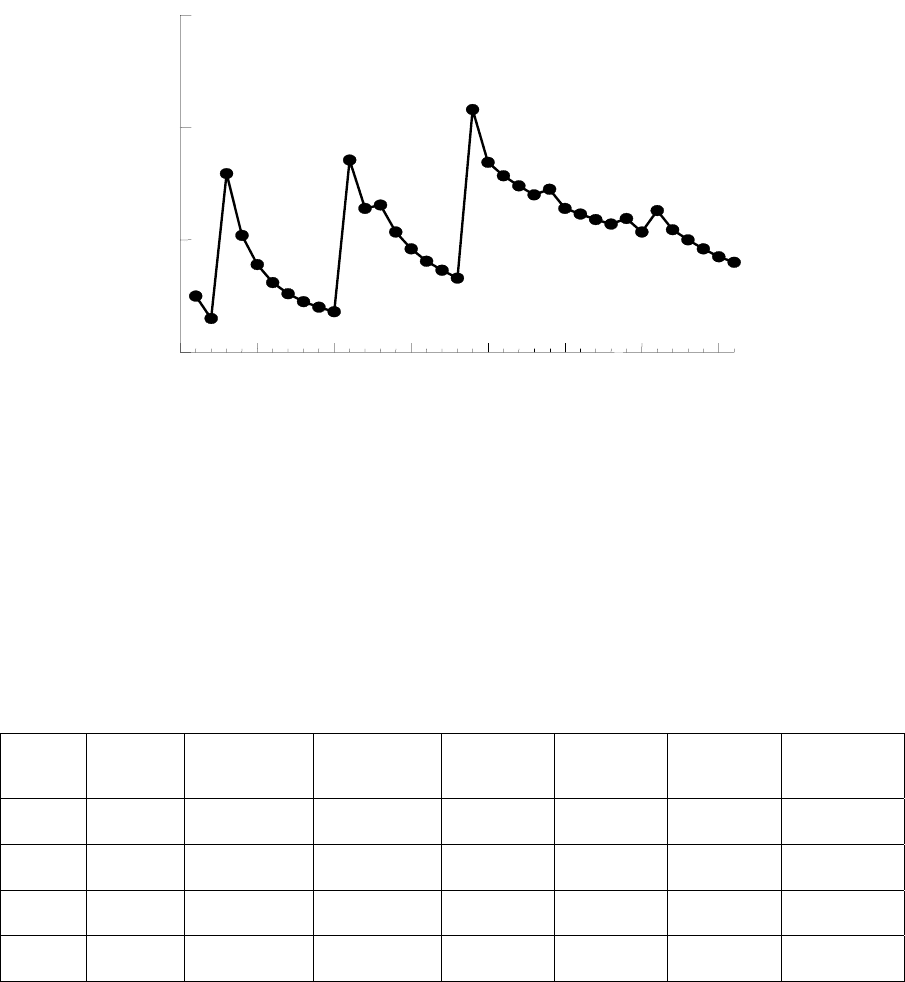
Изменение атомных радиусов показано на рис. 3.1, из которого
видно, что зависимость имеет характерный для периодического закона
«пилообразный» вид. Но в периодах уменьшение размеров атомов и ио-
нов происходит не монотонно, что объясняется особенностями
64
электронны в универ-
сит
х оболочек некоторых атомов, которые изучаются
етском курсе химии.
0 5 1 0 15 20 25 30 3 5
Ζ
0 . 0 0
0 . 1 0
0 . 2 0
0 . 3 0
R
,
н
м
L i
Na
K
H
H e
Ne
Ar
K r
Рис. 3.1. Зависимость радиуса
от атомного номера элементов первого-четвёртого периодов
Простые положительно заряженные ионы (катионы) возникают
отрыве электронов от атомов, а простые отрицательно
(анионы) – при радиусы ато-
мов и ионов щелоч
лица 1
адиус ом о елоч х элементов галогенов
м ио r r, нм атио r,
при
заряженные
их присоединении. В табл. 3.1 приведены
ных элементов и галогенов.
Таб 3.
Р ы ат ов и и нов щ ны и
АтомАтом r, н Кат н , нм К н нм
Li 0,157
+
0 39
F
–
0,040 Li ,019 F 0,0
Na 0,180
+
0 73
–
0,074 Na ,028 Cl 0,0
Cl
K 0,216
+
0 87 0K ,059 Br 0,0
Br
–
,089
Rb 0,229
+
0 07
I
–
0Rb ,073 I 0,1
,109
Из табл. ет пр е то катионы сопровожда-
етс
следу , что евращ ние а мов в
я резким уменьшением радиуса, тогда как превращение в анионы
почти не изменяет орбитального радиуса. Объясняется это тем, что об-
разование анионов не связано с образованием новых электронных слоев
и оболочек, а образование катионов сопровождается, как правило, ис-
чезновением всего внешнего энергетического уровня.
65

3.2.2. Энергия и потенциал ионизации атомов
Энергия, затрачиваемая на отрыв электрона от атома и превраще-
ние атома в положительно заряженный ион, называется энергией иони-
зации (Е
ион
). Экспериментально ионизацию атомов проводят в электри-
ческом поле, измеряя разность потенциалов, при которой происходит
ионизация. Эта разность потенциалов называется ионизационным по-
тенциалом (J). Единицей измерения ионизационного потенциала явля-
ется эВ/атом, а энергии ионизации – кДж/моль; переход от одной вели-
чины к другой осуществляется по соотношению: Е
ион
= 96,5·J.
Отрыв от атома первого электрона характеризуется первым иони-
зационным потенциалом (J
1
), второго – вторым (J
2
) и т.д. Последова-
тельные потенциалы ионизации возрастают (табл. 3.2), т.к. каждый сле-
дующий электрон необходимо отрывать от иона с возрастающим на
единицу положительным зарядом. Из табл. 3.2 видно, что у лития рез-
кое увеличение ионизационного потенциала наблюдается для J
2
, у бе-
риллия – для J
3
, у бора – для J
4
и т.д. Резкое увеличение J происходит
тогда, когда заканчивается отрыв внешних электронов и следующий
электрон находится на предвнешнем энергетическом уровне.
Таблица 3.2
Потенциалы ионизации атомов (эВ/атом)
элементов второго периода
Элемент J
1
J
2
J
3
J
4
J
5
J
6
J
7
J
8
Литий 5,39 75,6 122,4 – – – – –
Бериллий – 9,32 18,2 158,3 217,7 – – –
Бор 8,30 25,1 37,9 259,3 340,1 – – –
Углерод 11,26 24,4 47,9 64,5 392,0 489,8 – –
Азот 66,8 – 14,53 29,6 47,5 77,4 97,9 551,9 6
Кислород 13,60 35,1 54,9 77,4 113,9 138,1 739,1 871,1
Фтор 17,40 3 157,1 185,1 953,6 5,0 62,7 87,2 114,2
Неон 21,60 41,1 63,0 97,0 126,3 157,9
Ионизационный потенциал – физическая характеристика, но явля-
ется показателем металлических свойств элемента: чем он меньше, тем
легче отрывается электрон от атома и тем сильнее выражены металли-
ческие (восстановительные) свойства элемента. Для элементов, с кото-
рых начинаются периоды (литий, натрий, калий и др.), первый иониза-
66
ционный потенциал равен 4–5 эВ/атом, и эти элементы я
пичными металлами – си ми. У других металлов
значения J
1
низацион-
н тенц но 10 азо ,53 -
слорода 1 и т
н т
группах ), д уе
талличес вой периодах и лли х – уп Поэ
не ал од правой ве час ой
ней Периодической тем аниц жду тал и
таллами проходит во втором периоде м е ор
третьем между алюминие кре и т прил ени .
вляются ти-
льными восстановителя
больше, но не выше 10 эВ/атом. У неметаллов ио
ые по
Пе
иалы обыч больше
.д.
ые по
эВ/атом: у та 14
ах ве
эВ/атом, ки
3,60 эВ/атом
рвые ио
ш
низацион
аю рис
енциал
ч и
ы в период
ет в
у личиваю
усилении
тся, а в
умень
ких с
тся (
ств в
. 3.2 то св
мета
ельст
чески
т об
в гр
неме-
томупах.
мет лы нах ятся в рхней ти, а металлы – в лев ниж-
части сис ы. Гр а ме ме лами неме-
ежду берилли м и б ом, в
– м и мнием .д. ( ож е 10)
0 5 1 0
1
5
2
0
2
5
3
0
3 5
Ζ
0 . 0 0
1 0 . 0 0
2 0 . 0 0
3 0 . 0 0
J
H e
Ne
H
L i
Na
Ar
K
K
r
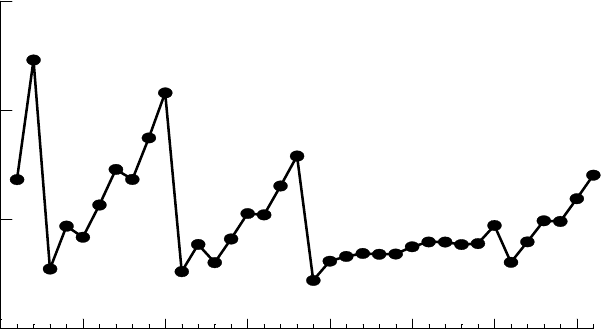
Рис. 3.2. Зависимость ионизационного потенциала
от атомного периодов
Пример 3.1. Ионизационный потенциал натрия равен 5,14 эВ/атом, а углерода
11,26
оединение элек-
трон
табл. 3.3.
номера элементов первого-четвёртого
эВ/атом. Чему равна их энергия ионизации?
Решение. 1. Е
ион
(Na) = 5,14·96,5 = 496,0 кДж/моль.
2. Е
ион
(С) = 11,26·96,5 = 1086,6 кДж/моль.
3.2.3. Сродство к электрону
(этот вопрос можно не изучать)
Сродство к электрону – это энергия, выделяющаяся при захвате
электрона атомом, или энергия, затрачиваемая на прис
а к атому. Эта характеристика обозначается символом F. Методика
определения сродства к электрону пока не совершенна, поэтому данные
об этой величине противоречивы. Наиболее достоверные значения
сродства к электрону для элементов трех первых периодов приведены в
67
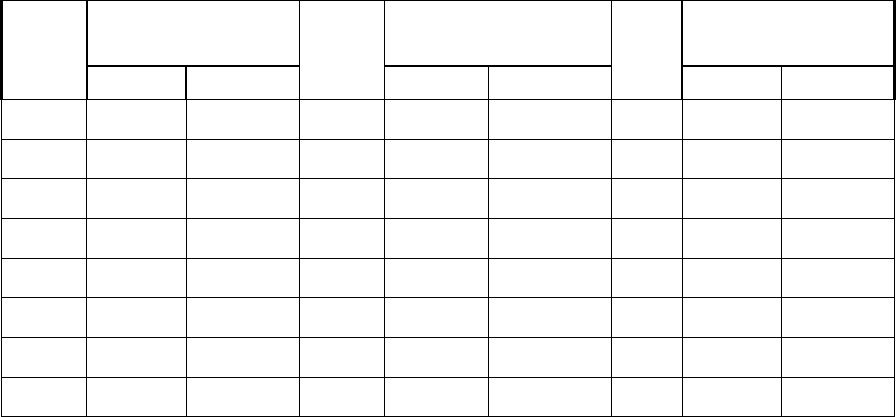
Таблица 3.3
Сродство к электрону
элементов первого, второго и третьего периодов
Эле-
мент
Сродство
к электрону
Эле-
мент
Сродство
к электрону
Эле-
мент
Сродство
к электрону
эВ/атом кДж/моль
эВ/атом кДж/моль
эВ/атом кДж/моль
H 0,75 72,4 Li 0,59 59,8 Na 0,34 32,8
He –0,22 –21,2 Be –0,19 –18,3 Mg –0,32 –30,9
B 0,33 31,8 Al 0,46 44,4
4 119,6 C 1,24 119,7 Si 1,2
0,77 74,3 N 0,05 4,8 P
O 1,47 141,8 S 8 200,7 2,0
F 3,50 Cl 1 348,3 337,8 3,6
0,30 –28 7 Ne – ,9 rA –0,36 –34,
табл. 3.3 видно, трицате ые зна я сродс элек-
тро меют ородны (He, Ne, Ar) а та бериллий гний,
поэтому отрицательно заряженные ионы этих омов неустойчивы.
При динен лектрон омам других элементов сопровождается
выделением гии. Это етельств т о том имеющ ней-
тральных ато электро компенсируют полностью си тяже-
ния отивоположно заряженного ядр что анионы Н
–
, F
–
,
–
ус-
тойч
3.2.4. Электроотрицательность
Электроотрицательностью называется свойство химического
элемента притягивать к своему атому электроны от атомов других эле-
ментов, с которыми данный элемент образует химическую связь в со-
единениях.
При образовании химической связи между атомами разных эле-
ментов общее электронное облако смещается к более электроотрица-
тельному атому, из-за чего связь становится коваленто-полярной, а при
большой разности электроотрицательностей – ионной.
Электроотрицательность учитывается при написании химических
формул: в бинарных соединениях первым записывается символ менее
электроотрицательного, а вторым – более электроотрицательного эле-
мента нное
Из что о льн чени тва к
ну и благ е газы кже и ма
ат
сое ие э а к ат
энер свид уе , что иеся у
мов ны не л при
пр а и Cl
–
, O
ивы. Но присоединение двух и более электронов никаким атомом
невозможно и, следовательно, ионы O
2–
, S
2–
, N
3–
и т.п. не существуют.
. Знак степени окисления элемента в соединении (но не числе
68
