Морозов В.П. Практикум по неорганической химии
Подождите немного. Документ загружается.

81
остывания сосуда налить в него немного воды и взболтать. Каков
цвет раствора? Написать уравнение реакции.
б) В железной ложечке сильно нагреть небольшое количество
порошка железа и понемногу высыпать в сосуд с хлором, на дне
которого насыпан небольшой слой песка. Наблюдать взаимодейст-
вие железа с хлором. Написать уравнение реакции.
3. Взаимодействие хлора с неметаллами (опыт проводится
под тягой)
Положить в ложечку для сжигания немного красного фосфора
и внести в сосуд с хлором. Наблюдать происходящее явление. На-
писать уравнение реакции. Указать окислитель и восстановитель.
4. Хлорная вода и ее свойства (опыт проводится под тягой)
а) Налить в пробирку (на 2/3) холодной воды и насытить ее
хлором (пропуская хлор в течение 2-4 минут). Отметить цвет и за-
пах полученной хлорной воды (осторожно!). Полученную хлорную
воду сохранить для опытов.
б) К небольшой порции полученной хлорной воды прилить
раствор лакмуса. Что наблюдается? К другой порции добавить не-
сколько капель раствора нитрата серебра. Объяснить результаты
опыта и написать уравнения реакций в молекулярной и ионной
формах.
в) В пробирку с раствором сульфата хрома(III) прилить избы-
ток раствора гидроксида калия и добавить хлорной воды. Отметить
изменения окраски раствора. Написать уравнения реакций, имея в
виду, что ионы Cr
+3
переходят в ионы CrO
4
-2
.
5. Получение брома и йода (работать под тягой!)
а) Смешать немного кристаллов KBr с небольшим количеством
порошка MnO
2
, всыпать в пробирку, прилить несколько капель
концентрированной H
2
SO
4
и слабо подогреть. Отметить цвет и за-
пах (осторожно!) выделяющихся паров брома. Написать уравнение
реакции.
б) Проделать аналогичный опыт с KI. Какое вещество выделя-
ется в виде паров? Каков их цвет и запах? Написать уравнение ре-
акции. Какую роль выполняет MnO
2
в проведенных реакциях?
82
в) К раствору KI прилить по каплям свежеприготовленную
хлорную воду. Наличием, какого вещества, обусловлена окраска
раствора? Добавить к раствору 1 мл бензола. Энергично встрях-
нуть содержимое пробирки. Отметить цвет раствора и слоя бензо-
ла. Сделать вывод о растворимости брома в воде и органическом
растворителе. Написать уравнение реакции взаимодействия KBr с
хлорной водой. Составить электронное равенство.
г) В 2 пробирки налить по 2-3 мл раствора KI, в одну из них
прибавить по каплям свежеприготовленную хлорную воду, в дру-
гую – бромную воду. Наблюдать за происходящими явлениями.
Составить уравнения реакций. Сравнить окислительную актив-
ность Cl
2
и Br
2
и проверить свои наблюдения, пользуясь таблицей
окислительно-восстановительных потенциалов.
6. Получение хлороводорода и его свойства
Собрать прибор. В колбу Вюрца поместить 15-20 г хлорида на-
трия. В капельную воронку влить концентрированную серную ки-
слоту. Конец газоотводной трубки ввести в сухой сосуд для соби-
рания хлороводорода так, чтобы трубка доходила почти до дна. За-
крыть отверстие сосуда. Рядом с прибором – кристаллизатор с во-
дой. Из капельной воронки вливать серную кислоту. Наблюдать за
происходящими изменениями реагирующих веществ. Для ускоре-
ния реакции колбу слегка можно подогреть. Закрыть отверстие со-
суда с хлороводородом. Повернув сосуд отверстием вниз, погру-
зить его в кристаллизатор с водой и открыть сосуд с хлороводоро-
дом. Объяснить наблюдаемые явления. Какова растворимость хло-
роводорода в воде? Затем вынуть сосуд из кристаллизатора, закрыв
его предварительно под водой.
Разделить полученный раствор на 4 пробирки. Одну часть рас-
твора испытать лакмусовой бумагой. Доказать опытным путем, что
полученный раствор хлороводорода является соляной кислотой. Во
вторую порцию раствора внести гранулу цинка, в третью – не-
большое количество оксида магния, в четвертую – несколько кри-
сталлов карбоната кальция. Наблюдать происходящие процессы.
Написать уравнения реакций получения соляной кислоты и взаи-
модействия соляной кислоты с этими веществами.
83
Контрольные задания
1. Дописать уравнения следующих окислительно-
восстановительных реакций:
HCl + PbO
2
=
HCl + KClO
3
=
Cl
2
+ KOH =
KI + H
2
O
2
+ H
2
SO
4
=
KClO
3
+ H
2
C
2
O
4
= ClO
2
+…
KClO
3
+ MnO
2
+ KOH =
NaIO
3
+ SO
3
+ H
2
O =
2. Написать уравнения реакции гидролиза Cl
2
в молекулярной
и ионной формах. Как влияет на равновесие гидролиза добавление
к хлорной воде: а) раствора кислоты, б) раствора щелочи, в) NaCl.
3. Сколько литров Cl
2
(измеренного при н.у.) образуется при
взаимодействии 100 мл 36 %-й соляной кислоты с 50 г KMnO
4
?
(Ответ: 8,15 л.)
4. Сколько миллилитров 30 %-го раствора HCl нужно для по-
лучения из нее действием MnO
2
11,2 г Cl
2
измеренного при н.у.?
(Ответ: 211 мл.)
5. К раствору NaCl был прилит избыток раствора AgNO
3
. В ре-
зультате реакции выпал осадок массой 10 г. Сколько граммов NaCl
было в растворе?
(Ответ: 4,1 г.)
6. В замкнутом сосуде было смешано 2 моль газообразного Cl
2
с 3 моль водорода. В результате взаимодействия газов (при повы-
шенной температуре и в присутствии катализатора) устанавливает-
ся равновесие: H
2
+ Cl
2
⇔ 2HCl.
Концентрация Cl
2
в момент равновесия оказалась 0,6 моль.
Определить К
равн
.
(Ответ: 8,1.)
7. Сколько хлороводорода (н.у.) содержится в 3 л 20 %-го рас-
твора соляной кислоты.
(Ответ: 405 л.)
8. Определить валентность и степень окисления брома и йода в
следующих соединениях: HBr, HBrO, HBrO
3
, I
2
O
5
, HIO
4
, HIO.
84
9. Написать уравнения реакций брома с водой. В каком на-
правлении сместится химическое равновесие при добавлении в
систему:
а) кислоты,
б) йодида калия?
10. В раствор иодида калия было добавлено небольшое коли-
чество бромной воды, затем избыток хлорной воды. Какие реакции
произошли в растворе?
11. Написать уравнения реакций получения йодноватой кисло-
ты тремя способами.
12. Закончить уравнения реакций и подобрать коэффициенты:
KBr + KClO + HCl =
I
2
+ HNO
3
(kонц.) =
KBrO
3
+ KBr + H
2
SO
4
=
Br
2
+ KOH =
Br
2
+ Cl
2
+ H
2
O = HCl +…
Ba(BrO
3
)
2
+ H
2
SO
4
=
13. Сравнить силу кислот и окислительные свойства в ряду:
HClO
3
, HBrO
3
, HIO
3
.
14. Определить процентную и молярную концентрации рас-
твора бромоводородной кислоты, полученной разбавлением 50 мл
14 %-го раствора HBr (ρ = 1,10) до 700 мл водой (ρ = 1,0).
(Ответ: 1,1 %; 0,136 М.)
15. Сколько миллилитров, 6 %-го раствора KBrO
3
(ρ = 1,04)
надо взять для того, чтобы в присутствии H
2
SO
4
окислить FeSO
4
,
содержащийся в 50 мл его 0,75 М раствора?
(Ответ: 16,7 мл.)
16. Определить степень окисления реагирующих веществ и ко-
эффициенты в следующих реакциях окисления-восстановления:
а) KI + H
2
O
2
+ HCl = I
2
+ KCl + H
2
O;
б) Na
2
SO
3
+ I
2
+ H
2
O = Na
2
SO
4
+ HI.
17. Сколько миллилитров хлора (при н.у.) можно получить,
если подействовать кислотой на 2 кг хлорной извести, содержащей
80 % Ca(ClO)
2
?
(Ответ: 500 мл.)
85
18. Какой объем хлора при 27
0
С и 101,325 кПа получится при
взаимодействии 20 г HCl с эквивалентным количеством перманга-
ната калия?
(Ответ: 3,49 л.)
19. Вычислите, сколько перманганата калия, хлорида натрия и
80 %-ой серной кислоты надо взять, чтобы полученным хлором
окислить иодид – ионы из 1 кг иодида калия?
(Ответ: 190,4 г KMnO
4
; 352,6 г NaCl; 590,3 г 80 % H
2
SO
4
.)
20. Дописать следующие уравнения и проставить соответст-
вующие коэффициенты:
I
2
+ Cl
2
+ H
2
O = HIO
3
+ …
KCl + HNO
3
= NO + …
K
2
Cr
2
O
7
+ KI + H
2
SO
4
= Cr
2
(SO
4
)
3
+ …
KIO
3
+ KI + H
2
SO
4
= I
2
+ …
KClO
3
+ MnO
2
+ KOH = K
2
MnO
4
+ …
CaClO
2
+ H
2
O
2
= CaCl
2
+ …
21. Проставить соответствующие коэффициенты и написать
уравнения в молекулярной форме:
IO
3
-
+ SO
3
2-
+ H
+
= I
2
+ SO
4
2-
+ H
2
O;
Br
-
+ MnO
4
-
+ H
+
= Br
2
+ Mn
2+
+ H
2
O;
ClO
-
+ MnO
4
-
+ H
2
O = Cl
-
+ MnO
4
-
+ OH
-
.
КИСЛОРОД И СЕРА
Общая характеристика подгруппы кислорода.
В подгруппу кислорода входят пять элементов: кислород, сера,
селен, теллур и полоний (полоний – радиоактивный элемент). Это
р-элементы VI группы периодической системы Менделеева. Они
имеют групповое название – халькогены, что означает «образую-
щие руды».
У атомов халькогенов одинаковое строение внешнего энерге-
тического уровня (см. п.2, табл.7). Этим объясняется сходство их
химических свойств. Все халькогены в соединениях с водородом и
металлами проявляют степень окисления –2, а в соединениях с ки-
слородом и другими активными неметаллами – обычно +4 и +6
(
п.5, табл.7).
86
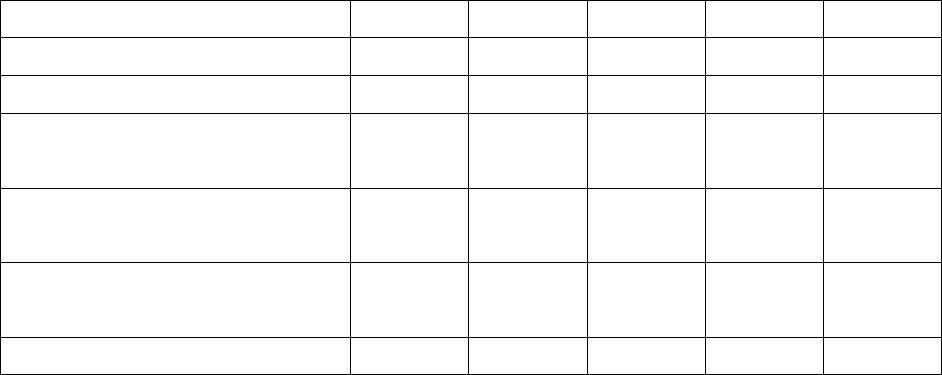
Таблица 7
Свойства элементов подгруппы кислорода
Свойства O S Se Te Po
1.Порядковый номер 8 16 34 52 84
2.Валентные электроны
2s
2
2p
4
3s
2
3p
4
4s
2
4p
4
5s
2
5p
4
6s
2
6p
4
3.Энергия ионизации
атома, эВ
13,62
10,36
9,75
9,01
8,43
4.Относительная элек-
троотрицательность
3,50
2,6
2,48
2,01
1,76
5.Степень окисления в
соединениях
-1, -2,
+2
-2, +2,
+4, +6
-2, +4,
+6
-2, +4,
+6
-2, +2
6.Радиус атома, нм 0,066 0,104 0,117 0,137 0,164
Для кислорода, как и для фтора, нетипична степень окисления,
равная номеру группы. Он проявляет степень окисления обычно –2
и в соединении со фтором +2. Значения степеней окисления сле-
дуют из электронного строения халькогенов.
У атома кислорода на 2р-подуровне два неспаренных элек-
трона. Его электроны не могут разъединяться, поскольку отсутст-
вует d-подуровень на внешнем уровне, т. е. отсутствуют свобод-
ные орбитали. Поэтому валентность кислорода всегда равна двум,
а степень окисления –2 и +2 (например, в H
2
O и OF
2
). Таковы же
валентность и степень окисления у атома серы в невозбужденном
состояние. При переходе в возбужденное состояние (что имеет
место при подводе энергии, например при нагревании) у атома се-
ры сначала разъединяются 3р-, а затем 3s-электроны. Число не-
спаренных электронов, а, следовательно, и валентность в первом
случае равны четырем (например в SO
2
), а во втором – шести (на-
пример в SO
3
). Очевидно, четные валентности 2, 4, 6 свойственны
аналогам серы – селену, теллуру и полонию, а их степени окисле-
ния могут быть равны –2, +2, +4, +6.
Водородные соединения элементов подгруппы кислорода от-
вечают формуле H
2
R (R- символ элемента): H
2
O, H
2
S, H
2
Se, H
2
Te.
Они называются хальководородами. При растворении их в воде
образуются кислоты. Сила этих кислот возрастает с ростом поряд-
кового номера элемента, что объясняется уменьшением энергии
87
связи в ряду соединений H
2
R. Вода, диссоциирующая на ионы H
+
,
OH
-
, является амфотерным электролитом.
Сера, селен, теллур образуют одинаковые формы соединений с
кислородом типа RO
2
и RO
3
. Им соответствуют кислоты типа
H
2
RO
3
и H
2
RO
4
. С ростом порядкового номера элемента сила этих
кислот убывает. Все они проявляют окислительные свойства, а ки-
слоты типа H
2
RO
3
также восстановительные.
Закономерно изменяются свойства простых веществ: с увели-
чением заряда ядра ослабевают неметаллические и возрастают ме-
таллические свойства. Так, кислород, сера и теллур – неметаллы,
но последний обладает металлическим блеском и проводит элек-
тричество.
Вопросы допуска к лабораторной работе
1. Электронная формула внешнего энергетического уровня
2s
2
2p
4
соответствует атому:
а) серы; б) углерода;
в) кремния; в) кислорода.
2. Электронная формула внешнего энергетического уровня
атома серы:
a) 3s
2
3p
4
; б) 2s
2
2p
4
;
в) 2s
2
3p
6
; г) 2s
2
2p
6
.
3. Валентность серы в соединениях SO
3
, H
2
S, Al
2
S
3
, соответст-
венно равна:
а) VI, II, II; б) III, II, III;
в) III, II, VI; г) II, II, II.
4. Химический знак элемента, электронная формула атома ко-
торого 1s
2
2s
2
2p
6
3s
2
3p
4
:
а) Se; б) Fe;
в) S; г) Si.
5. Электронную формулу 1s
2
2s
2
2p
4
имеет атом:
а) кремния;
б) серы;
в) углерода;
г) кислорода.
6.
В лаборатории кислород получают:
а) разложением воздуха;
88
б) разложением KMnO
4
;
в) взаимодействием метана с водой;
г) взаимодействием натрия с водой.
7. Массовая доля кислорода в серной кислоте равна приблизи-
тельно:
а) 16 %; б) 33 %;
в) 65 %; г) 2 %.
8. Элемент «Э» в схеме превращений Э = ЭО
2
= Н
2
ЭО
3
может
быть:
а) S; б) Ca;
в) P; г) Al.
9. Сумма коэффициентов в уравнении реакции, схема которой
H
2
S + O
2
= S + H
2
O, равна:
а) 4; б) 5;
в) 6; г) 7.
10. Оксиды серы (VI) не реагируют с:
а)NaOH; б) CaO;
в) H
2
O; г) CO
2
.
11. Кислород нельзя получить разложением:
а) KClO
3
; б) H
2
O;
в) KMnO
4
; г) CaCO
3
.
12. Массовая доля серы в оксиде серы (VI) SO
3
равна:
а) 40 %; б) 60 %;
в) 20 %; г) 10 %.
13. Масса серы необходимая для получения 4 моль SO
2
равна:
а) 32 г; б) 64 г;
в) 128 г; г) 4 моль.
14. Высшую и низшую валентность сера проявляет соответст-
венно в соединениях:
а) SO
3
, ZnS; б) SO
2
, H
2
S;
в) SO
3
, SO
2
; г) H
2
S, SO
3
.
15. Оксид серы (IV) реагирует с:
а) кислотами;
б) щелочами;
в) кислотными оксидами;
г) сульфатом натрия.
89
16. Соляная кислота может взаимодействовать со всеми веще-
ствами группы:
а)Fe, F
2
O
3
, Cu(OH)
2
; б) Zn, SiO
2
, Ag;
в) Cu, CuO, Cu(OH)
2
; г) S, SO
2
, SO
3
.
17. В уравнении реакции избытка гидроксида натрия с серной
кислотой сумма коэффициентов перед формулами продуктов реак-
ции равна:
а) 2; б) 3;
в) 4; г) 5.
18. Разбавленная серная кислота может реагировать с:
а) Mg, Cu(OH)
2
; б) CO
2
, NaOH;
в) FeO, H
2
S; г) P, CuCl
2
.
19. Молекулярную кристаллическую решетку имеет:
а) Al; б) SO
2
;
в) KCl; г) графит.
20. Коэффициент перед формулой H
2
O в уравнении реакции,
схема которой H
2
S + O
2
= H
2
O + SO
2
равен:
а) 1; б) 2;
в) 3; г) 4.
21. Кислород не реагирует с веществами пары:
а) Na, S; б) MgO, H
2
O;
в) H
2
, P; г) CH
4
, Fe.
22. Кислород можно распознать:
а) лакмусом; б) тлеющей лучиной;
в) известковой водой; г) по запаху.
23. К растворам данных солей прилили кислоту. В каких слу-
чаях наблюдается выделение газа?
а) Na
2
SO
4
; б) CuSO
4
;
в) Na
2
S; г) Na
2
SO
3
;
д) Na
2
S
2
O
3
.
24. Какие из приведенных сульфидов растворимы в воде?
а) CaS; б) CuS;
в) ZnS; г) CoS;
д) NiS.
25. Какие продукты получаются при взаимодействии цинка с
разбавленной серной кислотой?
а)ZnSO
4
+ H
2
O + SO
2
; б) ZnSO
4
+ H
2
;
90
в) ZnSO
4
+ S + H
2
O; г) ZnSO
4
+ H
2
O + H
2
S;
д) ZnSO
3
+ H
2
O.
26.Чему равна молярная масса эквивалента серы в соединении,
содержащем 50 % серы и 50 % кислорода?
а) 32; б) 8;
в) 164; г) 4;
д) 5,33 г.
1. Получение кислорода
а) Для опыта берут хорошо измельченный KClO
3
и порошок
MnO
2
. С бертолетовой солью надо обращаться осторожно, так как
в присутствии малейших примесей горючих веществ (бумаги, угля
и т. д.) она при трении или нагревании может дать сильный взрыв.
Следует также иметь в виду, что MnO
2
иногда загрязнен, поэтому
его предварительно прокаливают.
Поместить в чистую сухую пробирку около 0,03 г KClO
3
и ук-
репить ее в зажиме штатива. Нагревать дно пробирки сначала сла-
бо и осторожно, затем сильнее. Когда соль расплавится, испытать,
загорится ли внесенная в пробирку тлеющая лучинка. Сделать вы-
вод, интенсивно ли идет разложение KClO
3
. Оставить горелку, тот-
час же всыпать в пробирку немного заранее приготовленного по-
рошка MnO
2
. Снова опустить в пробирку, не касаясь, соли, тлею-
щую лучинку. Составить уравнение реакции разложения бертоле-
товой соли. Какую роль в этой реакции выполняет диоксид мар-
ганца?
б) В пробирку насыпать небольшое количество кристалличе-
ского перманганата калия и осторожно нагреть. Доказать наличие
кислорода.
2. Обнаружение пероксида водорода
Налить в пробирку 1 мл 3 %-го раствора перекиси водорода,
добавить 1-2 капли раствора иодида калия и несколько капель раз-
бавленной серной кислоты. Добавить к смеси 1-2 мл крахмального
клейстера. Наблюдать изменение окраски. Написать уравнение ре-
акции.
