Ушакова В.Г. (сост.) Химия окружающей среды
Подождите немного. Документ загружается.

81
ЛИТОСФЕРА [lithosphere].
Верхняя твердая оболочка Земли, включающая земную кору и верхнюю ман-
тию планеты. Мощность литосфеы 60-200 км, в том числе земной коры до 50-70
км на континентах и 5-10 км на дне океана. Земная кора более чем на 99,5% со-
стоит всего лишь из 13 химических элементов ( табл).
В результате антропогенной деятельности наибольшему загрязнению и раз-
рушению подвергается почва - самый верхний слой литосферы.
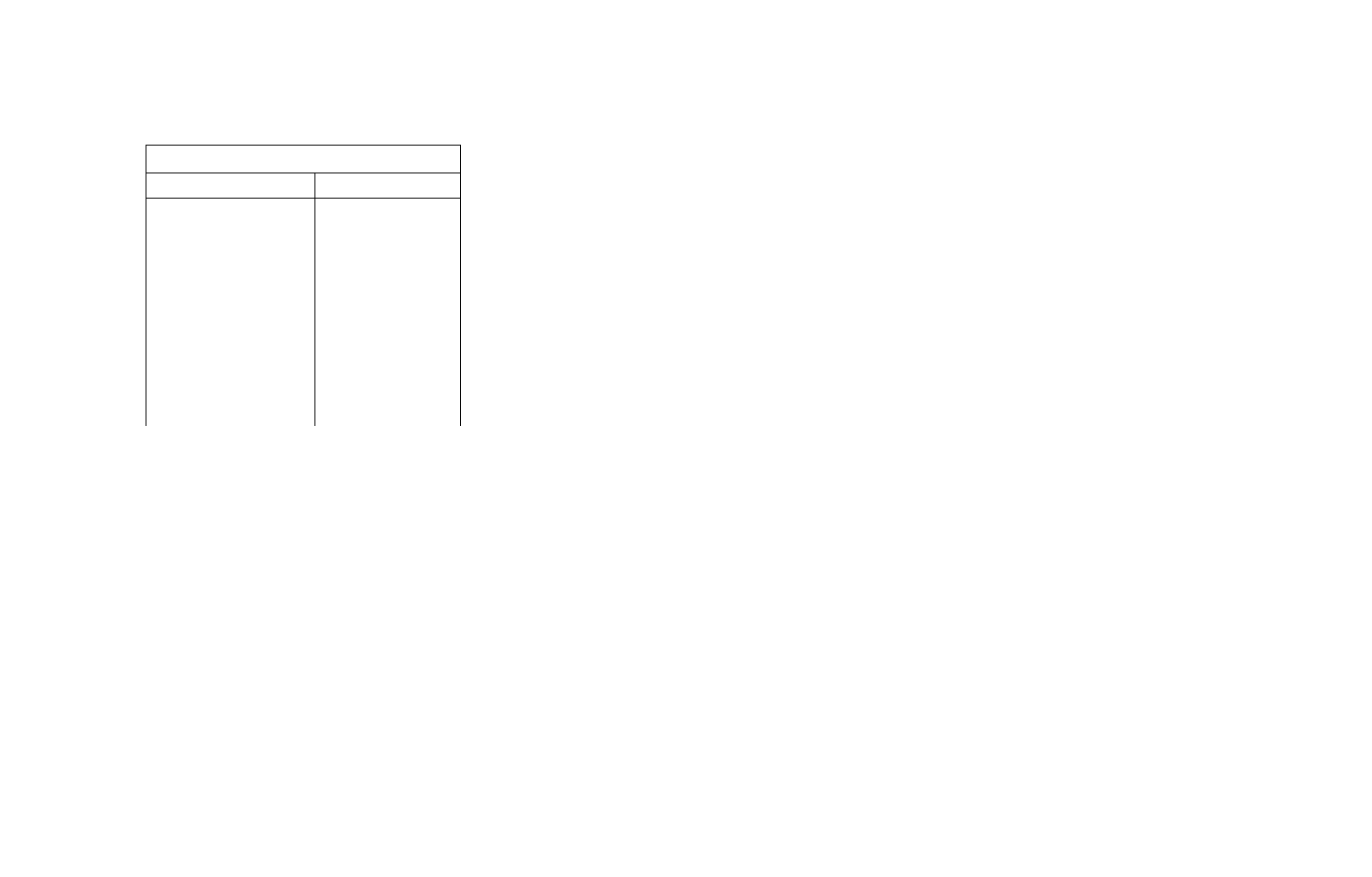
Состав земной коры
Элемент Содержание
Кислород
Кремний
Алюминий
Железо
Кальций
Натрий
Калий
Магний
Водород
Титан
Углерод
Хлор
Фосфор
49,13
26,00
7,45
4,20
3,25
2,40
2,35
2,35
1,00
0,61
0,35
0,20
0,10
МАГНИЙ (M
g
) [Magnesium].
Химический элемент II группы третьего периода периодической системы
элементов. Атомный номер 12, атомная масса 24,312. Впервые выделен Г. Дэви
в 1808 г. Относится к классу s-элементов. Серебристо-белый щелочноземель-
ный металл, t
пл
650°C, t
кип
1095°C, плотность 1,74 г/см
3
. Восстановитель, в со-
единениях проявляет степень окисления +2. В природе встречаются три ста-
бильных изотопа
24
Mg (78,60%),
25
Mg (10,11%) и
26
Mg (11,29%). На воздухе по-
крывается защитной пленкой оксида магния. Растворяется в растворах боль-
шинства кислот. Разрушается в морской и минеральной воде. Химически стоек
в растворах соды, щелочей, а также в бензине, керосине. В больших количест-
вах растворяет водород. Содержание в земной коре 2,1% по массе, в морской
воде 0,12%. В свободном виде в природе не встречается, находится в виде си-
ликатов, хлоридов, карбонатов, сульфатов. Например: доломит - MgCO
3
· Са-
СО
3
, магнезит - MgCO
3
. Мировое производство 325 000 т/ год. Применяется
при получении легких сплавов, в порошкообразном виде для обезвоживания
органических веществ, в пиротехнике, при производстве сигнальных ракет, за-
жигательных бомб, в антикоррозийных системах защиты металлов.
Существенно важен для всех форм жизни. Содержание в организме человека
(масса тела 70 кг) - 19 г, в крови 37,8 мг/л, в костной ткани 7-5-18 • 10
-2
%, в
мышечной ткани 9 · 10~
2
%. Ежедневный прием с пищей - 250-380 мг. Нетокси-
чен.
82
МАССОВАЯ ДОЛЯ (w) [mass fraction].
Безразмерная величина, равная отношению массы растворенного вещества
(m) к массе всего раствора (m
p
): w =m/ m
p
. Массовую долю. Обычно выражают
в долях от единицы или в процентах. Например, пусть массовая доля хлорида
натрия в растворе составляет 0,1 или 10%. Это означает, что в 100 г данного
раствора содержится 10 г хлорида натрия и 90 г воды. Процентный способ вы-
ражения массовой доли во многих отраслях науки и техники называют массо-
вым процентом или процентом по массе.
МАССОВАЯ КОНЦЕНТРАЦИЯ [mass concentration].
Отношение массы компонента к объему раствора (системы). Выражается в
кг/м
3
. Рекомендована для использования в рамках Международной системы
единиц. МАССОВОЕ ЧИСЛО [mass number].
Сумма протонов и нейтронов (нуклонов) в ядре атома конкретного элемента.
Обозначается цифрой вверху слева у символа химического элемента. Напри-
мер,
16
О,
32
S. Используется для характеристики изотопов и радиоактивных эле-
ментов. Имеет целочисленные значения. Практически полностью совпадает с
атомной массой. Иногда обозначается буквой А.
МАССОВЫЙ ПРОЦЕНТ, ПРОЦЕНТ ПО МАССЕ [MASS PERСENT].
Процентная доля массы вещества в общей массе раствора. Характеризует
количество граммов вещества в 100 г раствора. То же, что процентное выраже-
ние массовой доли. Часто используется для характеристики содержания тех или
иных элементов и соединений в земной коре и других оболочках планеты. См.
массовая доля.
МГНОВЕННЫЕ ДИПОЛИ [momentary dipoles].
Диполи, имеющие очень малое время жизни. Обусловливают дисперсионное
взаимодействие между нейтральными химическими частицами при низких
температурах
МЕДЬ (Сu) [Cuprum].
Химический элемент I группы четвертого периода периодической системы
элементов. Атомный номер 29, атомная масса 63,546. Известна древним циви-
лизациям. Относится к классу d-элементов. Пластичный металл красного цвета,
t
пл
1084
°
C, t
кип.
2540° С, плотность 8,94 г/см
3
. Восстановитель, в соединениях
проявляет степень окисления +1, +2, редко +3. В природе встречаются два ста-
бильных изотопа
63
Сu (69,1%) и
65
Сu (30,9%). Химически малоактивна. В сухом
воздухе при комнатной температуре почти не окисляется, при нагревании окис-
ляется до оксидов. При наличии в воздухе влаги и углекислого газа медленно
покрывается зеленой пленкой состава [Сu(ОН)]
2
СО
3
, называемой патиной. Рас-
творяется в азотной и концентрированной серной кислотах, образует комплекс-
ные соединения с аммиаком и другими веществами.
Содержание в земной коре 4,7 · 10
-3
% по массе, в морской воде 8 • 10
-9
%. Из-
вестно более 250 минералов, содержащих медь. В свободном состоянии встре-
чается редко. Мировое производство 7 · 10
6
т/год. Применяется при произ-
водстве латуни бронзы, медно-никелевых сплавов, для изготовления проводов,

83
кабелей, контактов, при получении сплавов с золотом. Соли меди используются
в сельском хозяйстве для борьбы с вредителями, в качестве микроудобрений.
Медь важна для всех форм жизни. Содержание в организме человека (масса
тела 70 кг) - 72 мг, в крови 1,01 мг/л, в мышечной ткани
1 · 10
-3
%. Ежедневный прием с пищей - 0,50-6,0 мг. Токсическая доза более
250 мг.
МЕЖДУНАРОДНАЯ НОМЕНКЛАТУРА, полусистематическая но-
менклатура [international nomenclature, semisystematic nomenclature].
Система составления названий химических соединений, в основу которой
положено использование слов иноязычного происхождения. Разновидность ра-
циональной номенклатуры. Чаще всего используются корни слов латинских на-
званий химических элементов. При записи названий оксидов, гидроксидов и
солей химических элементов после слов оксид, гидроксид или группового на-
звания кислотного остатка в рамках международной номенклатуры. Обычно
пишут символ химического элемента и численное значение его степени окис-
ления римскими цифрами. Но широко используется и другой подход, когда за-
писывается русскоязычное название химического элемента. Например: NO
2
-
оксид N (IV), оксид азота (IV) или диоксид азота, CuSO
4
- сульфат Си (II) или
сульфат меди (II). Международная номенклатура до сих пор широко применя-
ется в учебной, научной и технической литературе. Однако Международным
союзом теоретической и прикладной химии в настоящее время рекомендуется
использование систематической номенклатуры.
МЕТАЛЛЫ, [metals].
Простые вещества, характеризующиеся в обычных условиях высокими зна-
чениями электро- и теплопроводности, отрицательным температурным коэф-
фициентом электропроводности, ковкостью, блеском, пластичностью. В газо-
образном состоянии, как правило, одноатомны. В твердом состоянии образуют
кристаллы с плотно упакованными решетками. Обладают металлической хими-
ческой связью, обусловливающей их характерные свойства. Особенностью ме-
таллов. является низкая энергия ионизации и малое сродство к электрону. Из
110 элементов периодической системы 83 являются металлами За исключением
благородных металлов. в природе в чистом виде не встречаются.
Антропогенная деятельность вызывает увеличение содержания металлов в
окружающей среде. Это является негативным фактором, так как чистые метал-
лы. - чуждые, незнакомые биосфере вещества, от которых у нее нет эффектив-
ных способов защиты.
МЕТАН (СН
4
) [methane].
Простейший предельный углеводород, газ без цвета и запаха. Главная со-
ставляющая часть природного газа. Один из газов, вызывающих парниковый
эффект.
МЕХАНИЗМ ФОТОХИМИЧЕСКОЙ РЕАКЦИИ [mechanism of
photochemical reaction].
Совокупность превращений химических частиц под действием излучения.
Превращения делятся на две группы: первичные и вторичные. К первичным
процессам относятся:
84
1. Возбуждение фотоном химической частицы (М):
М + hν → М*
частица фотон возбужденная частица
2. Диссоциация молекулы АВ на атомы, радикалы (фотолиз):
АВ + hv → А + В;
3. Ионизация химических частиц с выделением электрона (е) (фотоэф-
фект):
М + hν → М
+
+ е. Активные частицы, образовавшиеся в первичных процес-
сах, могут вступать в химическое взаимодействие с обычными молекулами, а
также могут дезактивироваться путем излучения и теплового обмена. Эти про-
цессы, протекающие в отсутствие излучения, называются вторичными или
темновыми. Фотохимические реакции характерны для различных слоев атмо-
сферы, например при образовании фотохимического смога в тропосфере.
МИЛЛИОННАЯ ДОЛЯ (млн
-1
), количество частей на миллион [parts
per million, ppm].
Единица концентрации для растворов с очень небольшим содержанием рас-
творенного вещества или для оценки следовых количеств веществ в окружаю-
щей среде. Используется, например, для выражения биологической потребно-
сти в кислороде (БПК), концентрации микропримесей. Для примера рассмот-
рим, какова будет концентрация 5% раствора, выраженная в миллионных до-
лях. Так как 5% от 1 миллиона составляет 50000, то концентрация 5% раствора
вещества в миллионных долях составит 50000 млн
-1
(1 млн
-1
=10
-4
%).
МИНЕРАЛЫ, [minerals].
Общее название природных химических соединений или их смесей, пред-
ставляющих собой результирующие продукты химических реакций и физиче-
ских процессов, происходящих или происходивших на Земле.
К минералам относятся: различные соли (силикаты, сульфиды, карбонаты);
вода; кислород; нефть; уголь; элементарное золото; серебро и др. Возраст ми-
нералов составляет от 4,6 млрд. лет и меньше года (лед). Минералы - основа
земной коры. Среди них большую часть составляют (в мас. %): силикаты (75%),
оксиды и гидроксиды (17%), карбонаты (1,7%), сульфиды (1,15%), фосфаты
(0,7%), галогениды (0,5%). Содержание органических соединений вместе с нит-
ратами, хроматами и другими солями составляет 3,35% по массе (мас. %). Из-
вестны минералы биологического происхождения, к которым относятся по-
чечные камни, жемчуг и другие. К настоящему времени определено более 2500
минералов..
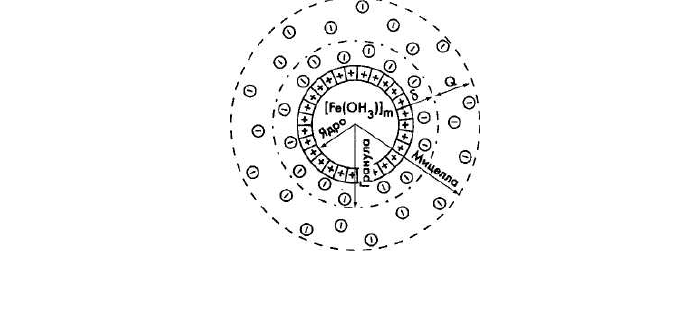
МИЦЕЛЛА [micelle].
Система, состоящая из коллоидной частицы и противоположно заряженных
ионов. На рисунке представлена схема строения мицеллы гидроксида железа
(III), где m - число молекул Fe(OH)
3
(обычно 400-600), δ - адсорбционный слой
противоионов, относительно прочно связанных с коллоидной частицей, Q -
диффузионный слой противоионов. Совокупность ядра, слоя положительно за-
ряженных ионов железа и адсорбционного слоя составляют гранулу.
85
+ - Fe
+3
- Cl
-
противоионы.
МОЛЬ, [Mole].
Количество вещества, содержащее столько химических частиц или других
структурных единиц (молекул, атомов, ионов, электронов), сколько содержится
атомов в 12 граммах изотопа углерода
12
С. В одном моле любого вещества со-
держится одинаковое число химических частиц, равное 6,02 • 10
23
. Эта величи-
на называется постоянной Авогадро. Слово «моль» после числа не склоняется.
Например, масса моля атомов, но 2 моль атомов.
МОЛЬНАЯ ДОЛЯ, [mole fraction].
Отношение числа молей растворенного вещества к общему числу молей рас-
творителя и растворенного вещества. Этот способ выражения концентрации
широко применяется в физической химии. См. концентрация
МОЛЬНЫЙ ОБЪЕМ, молярный объем [mole volume, molar volume].
Объем, занимаемый одним молем любого газа или смеси газов при давлении
101,325 кПа (760 мм рт.ст.) и температуре 0°С. Численно равен 22,4 л. См.
следствие закона Авогадро.
МОЛЬНЫЙ ПРОЦЕНТ [mole percent].
Процентная доля числа молей вещества в растворе:
C
моль%
= n/ n
раст
· 100% ,
где n, n
раст
- число молей вещества и раствора соответственно. См. мольная
доля.
МОЛЯЛЬНОСТЬ, [Molality].
Число молей растворенного вещества, приходящееся на 1 кг (1000 г) раство-
рителя. Разновидность массовой концентрации. Используется при изучении за-
мерзания и кипения растворов.
МОЛЯРНАЯ КОНЦЕНТРАЦИЯ, молярность, [molar concentration,
molarity].
Отношение количества молей растворенного вещества к объему раствора
(сплава). Выражается в кмоль/м3, на практике чаще всего в моль/л. Обычно
обозначается буквой М после численного выражения молярной концентрации.
Так, 0,4 М раствор КСl означает, что в одном литре раствора содержится 0,4
86
моль хлорида калия. Рекомендована для использования в рамках Международ-
ной системы единиц.
МОЛЯРНАЯ МАССА (М) [molar mass].
Масса моля вещества, равна частному от деления массы вещества в кило-
граммах на его количество в молях: М = m/v, кг/моль. На практике часто поль-
зуются кратной единицей - г/моль. В этом случае молярная масса численно
равна относительной молекулярной массе данного вещества (Мг). Например,
Mr (N
2
) = 28, М (N
2
) = 28 г/моль. Значение молярной массы атомов вещества
численно равно относительной атомной массе Аr. Например, Mr (N) = 14, М (N)
= 14 г/моль.
МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА [molar mass of equivalent].
Масса моля эквивалента. Численно совпадает с прежним значением грамм-
эквивалента. Например, Молярная масса эквивалента серной кислоты равна 98 :
2 = 49.
НАТРИЙ (Na) [Natrium].
Химический элемент I группы третьего периода периодической системы
элементов. Атомный номер 11, атомная масса 22,98977. Выделен Г. Дэви в 1807
г. Относится к классу s-элементов, группа щелочных металлов. Мягкий сереб-
ристо-белый металл, t
пл
97,83°C, t
кип.
882,9°С, плотность 0,968 г/см . Сильный
восстановитель, в соединениях проявляет степень окисления +1. В природе
встречается один стабильный изотоп
23
Na. Как и все щелочные металлы натрий
обладает очень высокой химической активностью. На воздухе быстро окисля-
ется, образуя в конечном итоге гидроксид и карбонат. Натрий. бурно взаимо-
действует с водой (иногда со взрывом) с образованием гидроксида натрия и во-
дорода. Энергично взаимодействует с кислородом, фтором, хлором, серой. При
температуре более 200°С с водородом образует гидрид натрия. В отличие от
других щелочных металлов при взаимодействии с кислородом образует перок-
сид натрия: Na + О
2
= Na
2
O
2
. Гидроксид натрия относится к сильным основани-
ям (щёлочь). Хранить натрий следует под слоем керосина или в инертной атмо-
сфере.
Содержание в земной коре 2,64% по массе, в морской воде - 1,05%. Из
всех других металлов натрий является наиболее распространенным элементом
в морской воде. Основные минералы: галит (каменная соль) - NaCl, мирабилит
(глауберова соль) - Na
2
SO
4
• 10Н
2
О, чилийская селитра - NaNO
3
, криолит —
Na
3
AlF
6
и другие. Мировое производство металлического Н. 200 000 т/год, кар-
боната Н. - 29 • 10
6
т/год. Применяется как теплоноситель в ядерных реакторах,
для получения тугоплавких металлов, при производстве газоразрядных ламп,
при получении синтетического каучука. Хлорид натрия является одним из ос-
новных базовых веществ в химической промышленности.
Важен для большинства форм жизни, включая человека. Хлорид натрия
служит одним из главных источников образования соляной кислоты - состав-
ной части желудочного сока человека и животных. Содержание в организме че-
ловека (масса тела 70 кг) - 100 г, в костной ткани - 1,0%, в мышечной ткани -
0,26+0,78%, в крови - 1970 мг/л. Ежедневный прием с пищей – 2 - 15 г, в усло-

87
виях жаркого климата до 25 - -70 г, так как соединения натрия. выводятся из
организма вместе с потом. Не токсичен.
НЕГАШЁНАЯ ИЗВЕСТЬ (СаО) [quick lime].
Оксид кальция, получаемый термическим разложением карбоната кальция
СаСО
3
:
>900°С
СаСО
3
→ СаО + СО
2
Негашёная известь реагирует с водой с обраованием гашеной извести и вы-
делением большого количества тепла:
СаО + Н
2
О = Са(ОН)
2
+ Q
НЕЖИВАЯ ПРИРОДА [dead nature].
Совокупность объектов окружающего нас мира: вода, воздух, скалы, кусок
гранита, песок, минералы и т. д. Составляет среду обитания для живых орга-
низмов, источник различного рода химических веществ для обеспечения их
жизнедеятельности. Часто к неживой природе относят объекты созданные че-
ловеком: дома, заводы, машины, плотины, города, дороги и т. д.
НЕЙТРАЛЬНАЯ РЕАКЦИЯ РАСТВОРА (НЕЙТРАЛЬНАЯ РЕАКЦИЯ)
[neutral reaction of solution, neutal reaction].
Свойство раствора, в котором концентрации ионов водорода и гидроксид-
ионов равны или примерно одинаковы. Характерна для чистой воды, растворов
солей, образованных сильными основаниями и сильными кислотами. Наблюда-
ется также при гидролизе солей, образованных слабыми кислотами и слабыми
основаниями.
НЕЙТРАЛЬНАЯ СРЕДА [neutral medium].,
Чистая вода или водные растворы, для которых концентрация гидроксид-
ионов и ионов водорода одинаковы: [ОН
-
] = [Н
+
], рН - 7.
Нейтральную среду имеют растворы солей, образованных сильной кислотой
и сильным основанием, например NaCl, K
2
SO
4
, NаNO
3
.
НЕЙТРОН, (n) [neutron].
Фундаментальная электрически нейтральная частица со спином 1/2 и массой
немного больше массы протона. Составная часть ядра атома. Часто нейтроны
относят к элементарным частицам.
НЕМЕТАЛЛЫ, [non-metals].
Вещества, не обладающие характерными свойствами металлов. Как правило,
к ним относятся вещества, состоящие из элементов, лежащих выше диагонали
бор-астат в периодической системе элементов Д. И. Менделеева.
НИТРАТЫ, [nitrates].
Соли азотной кислоты, содержащие кислотный остаток NO
з
-
. Получаются
при действии азотной кислоты на металлы, оксиды металлов и гидроксиды.
Хорошо
растворимы в воде, при нагревании разлагаются с выделением кислорода.
Наибольшее практическое значение имеют нитрат. калия, натрия, кальция и
аммония, называемые также селитрами. Применяются в качестве удобрений,
при производстве стекла. Нитрат калия с XIII в. используется при изготовлении
88
черного пороха (74-78% KNO
3
, 16-20% древесный уголь, 10% сера). Содержат-
ся в овощах и других продуктах. С повышением температуры и интенсивности
солнечного освещения нитраты в овощах при участии ферментов переходят в
более токсичные нитриты и далее в аммиак. Поэтому, например, овощи лучше
собирать во второй половине дня и в более холодное время суток. Это может
уменьшить содержание нитратов и нитритов в них на 30-40%. Ср. нитриты.
НИТРИТЫ, [nitrites].
Соли азотистой кислоты, содержащие кислотный остаток NO
2
-
. Нитриты ще-
лочных металлов образуются при взаимодействии щелочей с оксидом азота
(III). За исключением AgNO
2,
хорошо растворимы в воде. Некоторые нитриты
используются в качестве пищевых добавок. В почве под действием бактерий
нитрит-ион образуется из аммиака по схеме:
2NH
3
+ 2О
2
-> 2HNO
2
+ 2Н
2
. Более токсичны, чем нитраты. Ср. нитраты.
НОМЕНКЛАТУРА [nomenclature].
Система правил обозначения и составления названий химических элементов
и химических соединений. Различают номенклатуру для неорганических со-
единений для органических соединений
НООСФЕРА [noosphere].
Высшая стадия развития биосферы, сфера разума. При ноосфере. разумная
коллективная деятельность человечества должна стать главным, определяющим
фактором взаимоотношений общества и природы, обеспечивая гармоничное и
устойчивое их развитие. В эпоху ноосферы люди планеты должны научиться
жить в согласии с природой и ее законами, ибо в это время разум человека бу-
дет играть доминирующую роль в развитии системы человек - природа.
НООСФЕРНОЕ ОБРАЗОВАНИЕ [noospherical education].
Высшая ступень экологического образования.
НОРМА ВЫБРОСА, [discharge norm].
Суммарное количество газообразных и (или) жидких отходов, разрешаемое
предприятию для сброса в окружающую среду. Норма выброса определяется из
расчета, чтобы кумуляция вредных выбросов от всех предприятий данного ре-
гиона не создала бы в атмосфере и (или) гидросфере концентраций загрязняю-
щих веществ, превышающих ПДК.
НОРМА ЗАГРЯЗНЕНИЯ,[contamination norm].
Предельное количество какого-либо вещества, поступающего или содержа-
щегося в окружающей среде. Определяется ПДК и другими нормативными до-
кументами.
НОРМАЛЬНОСТЬ, [normality]. Число моль-эквивалентов вещества в 1 л
раствора. Обозначается н или N после численного выражения нормальности.
Так, 1 н раствора НС1 означает, что в одном литре раствора содержится один
моль-эквивалент соляной кислоты. Используется для характеристики жестко-
сти воды.

89
НОРМАЛЬНЫЕ УСЛОВИЯ [normal conditions].
Температура 273°К (0°С), давление 101,325 кПа (1 атм, 760 мм рт. ст.). На
практике иногда под термином нормальные условия понимают стандартные
условия, что неправильно.
НУКЛИД, [nuclide].
Конкретное атомное ядро с данными атомным номером и массовым чис-
лом А.
НУКЛОНЫ, [nucleons].
Общее название для протонов и нейтронов, основных частиц, составляющих
ядра атомов химических элементов.
ОБЩАЯ ЖЁСТКОСТЬ ВОДЫ [total water hardness].
Совокупность свойств природной воды, обусловленная содержанием в ней
растворимых солей кальция и магния. Общая жёсткость воды (Ж
общ
) складыва-
ется из временной и постоянной жесткости воды. Количественно общая жёст-
кость воды характеризуется количеством миллимоль-эквивалентов или милли-
молей ионов Са
2+
и/или Mg
2+
в 1 л или 1 кг воды (ммоль-экв/л, ммоль/л). Один
миллимоль-эквивалент жесткости воды отвечает содержанию в ней 20,04 мг/л
Са
2+
или 12,15 мг/л Mg
2+
, один миллимоль - 40,08 мг/л Са
2+
или 24,30 мг/л Mg
2+.
По величине общей жёсткости воды различают мягкую воду (Ж
общ
. не более 2
ммоль/л), воду средней жесткости (Ж
общ
от 2 до 6 ммоль/л), жесткую воду
(Ж
общ
. от 6 до 10 ммоль/л) и очень жесткую воду (Ж
общ
больше 10 ммоль/л). В
зависимости от места и происхождения природные воды имеют разную Ж
общ
..
Например, Ж
общ
в озерах и реках тундры составляет 0,1 - 0,2 ммоль/л, а в мо-
рях, океанах, подземных водах достигает 80-1000 ммоль/л и даже больше
(Мертвое море).
ОЗОН [ozone].
Химическое соединение из трех атомов кислорода. Газ синего цвета с резким
запахом, t
кип
- 111,9'С. Аллотропная модификация кислорода. Сильнейший
окислитель, хорошо растворяется в воде (100 объемов воды растворяет 49 объ-
емов О
3
). Образуется в атмосфере при электрических разрядах, в приземном
слое его содержится 10
-7
-10
-6
%. Озоновый слой в стратосфере поглощает ульт-
рафиолетовое излучение, опасное для всех живых организмов. Химическая ак-
тивность О
3
объясняется тем, что его молекула легко распадается на молекулу
кислорода и атомарный кислород. Образовавшийся атомарный кислород более
активно реагирует с веществами, чем молекулярный.
Применяют О
3
для обеззараживания промышленных сточных вод, в ме-
дицине в качестве дезинфицирующего средства. Следует отметить, что несмот-
ря на большую эффективность применения О
3
при обеззараживании воды огра-
ничено по двум причинам: 1) он должен вырабатываться в месте его примене-
ния; 2) в отличие от хлора О
3
быстро разлагается в водопроводных сетях. При
повышенном содержании в приповерхностном атмосферном воздухе О
3
пора-
жает органы дыхания, раздражает слизистые глаз, вызывает головную боль.
ПДК в воздухе рабочей зоны составляет 0,1 мг/м
3
. Токсичность О
3
. резко воз-
растает при одновременном воздействии оксидов азота.
90
ОЗОННАЯ «ДЫРА», [ozone hole].
Значительная область в озоносфере Земли с заметно пониженным содержа-
нием озона. Например, Озонная дыра над Антарктидой. Причины возникнове-
ния озонной дыры пока до конца не ясны. Считают, что одной из возможных
причин возникновения озонной дыры являются хлорсодержащие соединения.
ОЗОНОСФЕРА, [ozonosphere].
Область атмосферы на высоте 20-40 км, характеризующаяся максимальным
содержанием озона. Играет важнейшую роль в защите живых существ от высо-
коэнергетического воздействия ультрафиолетового излучения, избыток которо-
го вызывает рост числа заболеваний раком кожи.
ОКИСЛЕНИЕ, [oxidation].
То же, что реакция окисления
ОКИСЛИТЕЛИ [oxidizing agents].
Вещества, атомные или молекулярные частицы, присоединяющие электроны
в ходе окислительно-восстановительных реакций и понижающие при этом сте-
пень окисления входящих в них атомов. Например: Na
0
+ С1
2
0
= 2Na
+
Сl
-
.
В этой реакции окислителем будет хлор, который понизил (уменьшил) сте-
пень окисления от нуля до -1. Типичными окислителями . являются атомы и
молекулы неметаллов, катионы металлов, катион водорода, элементы в высшей
степени окисления. Например: S
+6
в серной кислоте, N
+5
в азотной кислоте.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР)
[oxidation — reduction reactions, redox reactions].
Химические реакции, осуществляющиеся за счет полного или частичного
перехода валентных электронов от одних атомных или молекулярных частиц к
другим, в результате которых изменяются степени окисления элементов. На-
пример:
2Са
0
+ О
0
2
= 2Са
+2
О
-2
; Са
+2
С+4Оз-
2
=2Са
+2
О
-2+
С
+4
О
-2
2
В первой реакции изменяются степени окисления элементов, во второй - нет,
поэтому к ОВР относится только первая из приведенных реакций. Процесс от-
дачи электронов, в результате которого степень окисления повышается, назы-
вается реакцией или процессом окисления (Са
0
- 2е~ = Са+2), а процесс присое-
динения электронов, в результате которого степень окисления элемента умень-
шается, называется реакцией или процессом восстановления (О
2
+ 4е = 2О
-2
).
В ОВР участвуют окислители и восстановители. В результате ОВР восстанови-
тель окисляется, а окислитель восстанавливается. ОВР - единый взаимосвязан-
ный процесс. Не может быть окисления без восстановления и наоборот. Число
электронов, участвующих в процессах восстановления и окисления, должно
быть одним и тем же. Это условие составляет основу нахождения стехиометри-
ческих коэффициентов в уравнении ОВР.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЙ ПОТЕНЦИАЛ [redox
potential].
Потенциал электрода в условиях, отличных от стандартных. Определяется
уравнением Нернста. Понятие окислительно-восстановительный потенциал
91
чаще всего используется для характеристики веществ, которые требуют ис-
пользования инертного электрода.
ОКРУЖАЮЩАЯ СРЕДА, [environment].
Внешняя среда, находящаяся в непосредственном контакте с рассматривае-
мой системой, объектом или субъектом. Термин окружающая среда требует
или подразумевает определяющее дополнение. Например, окружающая челове-
ка среда, изменение окружающей среды - изменение окружающей нас среды
и т. д.
ОТНОСИТЕЛЬНАЯ ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ, (ОЭО),
[relative electronegativity].
Величина, характеризующая способность атома притягивать электроны,
осуществляющие химическую связь. Определяется относительно электроотри-
цательности атома лития. Количественно может быть охарактеризована потен-
циалом ионизации и сродством к электрону. ОЭО - важная характеристика эле-
мента. Чем меньше значение ОЭО, тем сильнее выражены его металлические
свойства, чем больше - неметаллические свойства. Разность значений ОЭО
взаимодействующих атомов характеризует степень ионности образованной ими
химической связи: с увеличением разности (ΔОЭО) степень ионности связи
возрастает. Максимальное значение ОЭО имеет фтор (4,0), минимальное - це-
зий (0,7). В периодах периодической системы элементов значения ОЭО элемен-
тов увеличиваются слева направо, в главных подгруппах - уменьшаются сверху
вниз. С увеличением порядкового номера элемента значения ОЭО изменяются
периодически. Изменение значений ОЭО подтверждает характер изменения
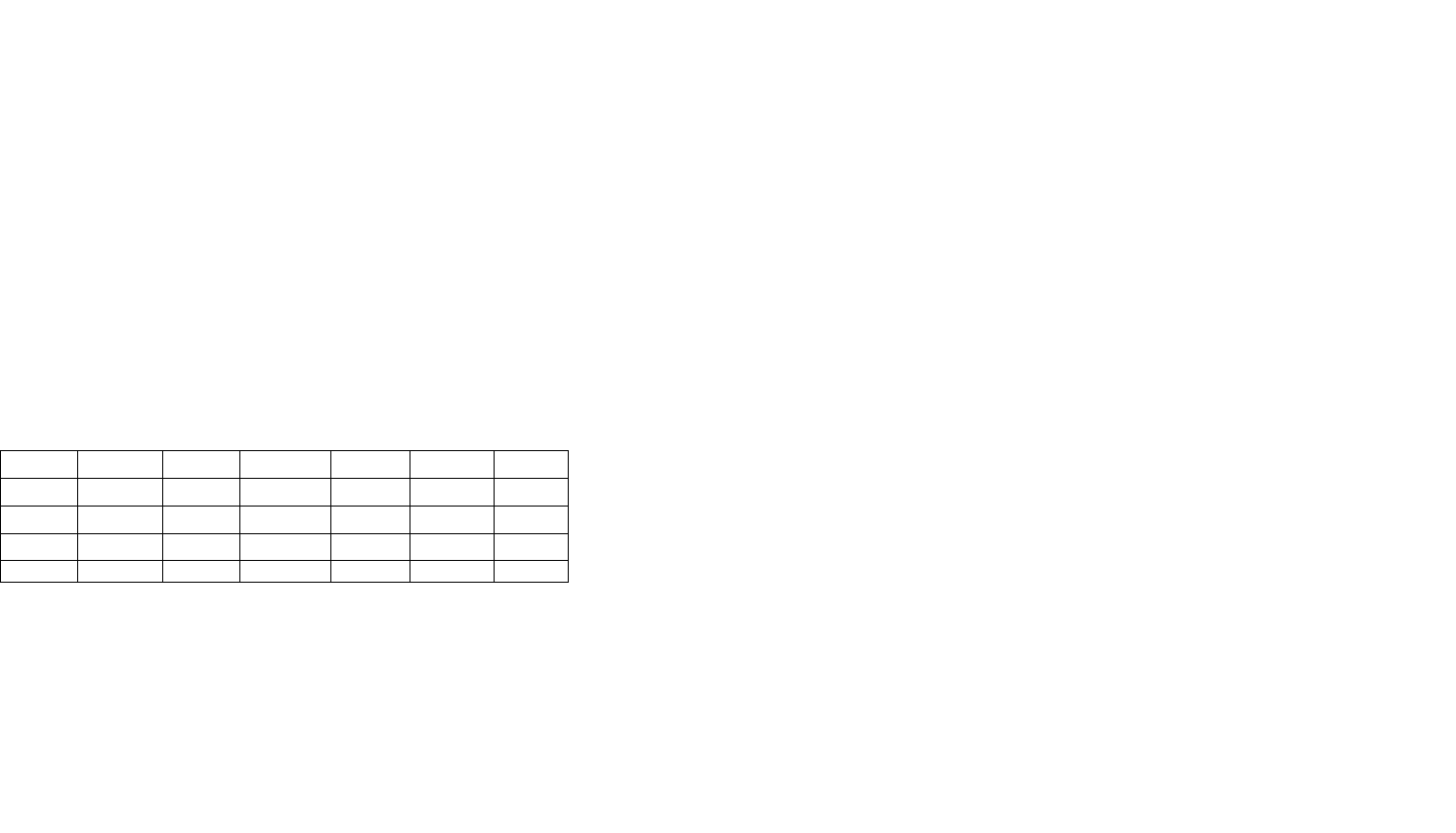
свойств элементов в периодах и группах. Значения ОЭО для некоторых элемен-
тов главных подгрупп первых пяти периодов (кроме инертных газов) приведе-
ны в таблице.
Н 2,1
Li 1.0 Be 1.5 В 2,0 С 2,5 N 3,0 О 3,5 F 4,0
Na 0,9 Mg 1.2 Al 1,5 Si 1,8 P 2,2 S 2,6 SI 3,1
К 0,8 Са 1.0 Ga 1,6 Ge 1,8 As 2,0 Se 2,4 Br 2,8
Rb 0.8 Sr 1.0 In 1.7 Sn 1.7 8b 1,8 Те 2,1 I 2,5
ПАРНИКОВЫЕ ГАЗЫ, [hotebad gases].
Химические вещества в газообразном состоянии в атмосфере, вызывающие
парниковый эффект. К парниковым газам относятся: углекислый газ, водяной
пар, метан, фреоны, оксид азота (I) и некоторые другие. Увеличение содержа-
ния парниковых газов. в атмосфере связано с антропогенной деятельностью и
увеличением числа жителей планеты.
ПАРНИКОВЫЙ ЭФФЕКТ, [hotebad effect].
Потепление климата на планете в результате накопления в атмосфере парни-
ковых газов, задерживающих длинноволновое (ИК) тепловое излучение с по-
верхности Земли.
92
ПАРЦИАЛЬНОЕ ДАВЛЕНИЕ ГАЗА, [partial gas pressure].
Давление, которое создает данный газ в газовой смеси. Равно давлению дан-
ного газа в объеме, равном объему смеси при определенной температуре. Дав-
ление смеси газов, химически не взаимодействующих друг с другом, равно
сумме парциальных давлений составляющих смесь газов.
ПОСТОЯННАЯ АВОГАДРО (N
А
), число Авогадро [Avogadro's constant,
Avogadro's number].
Величина, характеризующая количество частиц в одном моле любого веще-
ства. N
A
= 6,022 · 10
23
.
ПОСТОЯННАЯ ЖЕСТКОСТЬ ВОДЫ [permanent water hardness]. Свой-
ство природной воды, обусловленное содержанием в ней кальциевых и маг-
ниевых солей сильных кислот, главным образом сульфатов и хлоридов. посто-
яннную. жесткость воды можно устранить при введении в воду карбоната на-
трия или пропусканием ее через иониты. Например:
CaSO
4
+ Na
2
CO
3
= СаСО
3
↓ + Na
2
SO
4;
;
MgCl
2
+ Na
2
CO
3
= MgСО
3
↓ + 2NaCl.
ПОТЕНЦИАЛ ИОНИЗАЦИИ (I), ионизационный потенциал, энергия
ионизации [ionization potential, utilization energy].
Энергия, необходимая для удаления электрона из атома на бесконечно
большое расстояние. Измеряется в электрон-вольтах (эВ) или в кДж/моль.
ПРИНЦИП ЛЕ-ШАТЕЛЬЕ [Le Chatelier principle].
Если на равновесную химическую систему оказывается внешнее воздействие
за счет изменения температуры, давления или концентрации, то равновесие в
системе смещается в сторону протекания процессов, которые уменьшают вы-
шеуказанные воздействия.
1. Влияние повышения температуры (Т) на равновесную реакцию состоит в
смещении равновесия в сторону протекания эндотермической реакции, а при
понижении температуры - в сторону протекания экзотермической реакции. На-
пример: N
2
+ ЗН
2
↔ 2NH
3
+ Q
При увеличении Т равновесие реакции смещается влево; при уменьшении Т
равновесие реакции смещается вправо.
2. Для реакции с участием газообразных веществ повышение давления при-
водит к увеличению числа молекул в единице объема. Следовательно, в этом
случае равновесие сместится в сторону уменьшения числа молекул, т. е. в сто-
рону реакции, протекающей с образованием газообразных веществ, занимаю-
щих меньший объем. Например: 2Н
2
+ О
2
↔2Н
2
О
Смещение равновесия: вправо - при росте давления, влево - при уменьшении
давления.
3. Влияние концентрации веществ на равновесную систему. Увеличение
концентрации веществ смещает равновесие в сторону их расходования, а
уменьшение - в сторону их образования. Например: CO + Н
2
О
пар
↔ CO
2
+ Н
2
При увеличении концентрации СО и Н
2
О равновесие реакции сдвигается
вправо, а при уменьшении концентрации этих компонентов - влево. Бывают си-
туации, когда при внешнем воздействии на систему смещения равновесия не
наблюдается. Например: Н
2
+ С1
2
↔2НС1

93
Для этой реакции объемы исходных веществ и продуктов реакции равны.
Поэтому изменение давления для данной системы не вызовет смещения равно-
весия. Принцип Ле - Шателье справедлив и для условно равновесных природ-
ных систем, в том числе экологических, а также живых систем. Для биосферы
действие указанного принципа обеспечивает сохранение её устойчивости и
стабильности. Однако в последнее время наблюдается все больше примеров на-
рушения данного принципа. Одним из подтверждений этого является усиление
процессов опустынивания на нашей планете.
ПРИРОДНАЯ СРЕДА, [natural surroundings].
Совокупность природных и естественных факторов, не измененных деятель-
ностью человека. П.с. характеризуется саморегулированием и самоподдержа-
нием в течение длительного времени.
ПРИРОДНОЕ РАВНОВЕСИЕ, [nature equilibrium]. Состояние природной
среды, обеспечивающее ее длительное существование. См. принцип Ле-
Шателье.
ПРИРОДНЫЕ РЕСУРСЫ,[natural resources].
Общее название водных, минеральных, атмосферных, растительных, живот-
ных, почвенных, климатических и других ресурсов живой и неживой природы.
ПРИРОДНЫЙ АГЕНТ, [natural agent].
Физический, химический, биологический или любой другой природный ис-
точник воздействия на рассматриваемый объект, систему, процесс или явле-
ние.
ПРОТОН, (р) [proton].
Стабильная фундаментальная (элементарная) частица с единичным положи-
тельным электрическим зарядом, массой покоя 1,67 • 10
-
27 кг. Одна из двух со-
ставных частиц ядра атома. Исключение - ядро изотопа атома водорода (про-
тия), состоящее из одного протона. Число протонов в ядре атома определяет за-
ряд ядра и атомный (порядковый) номер элемента в периодической системе.
Масса протона. примерно в 1836 раз больше массы электрона. Стабильность
протона. составляет 10
30
-10
32
лет.
РАДИКАЛЫ, [radicals].
Кинетически независимые атомы, молекулы, атомные группы, обладающие
неспаренными электронами. Обладают повышенной реакционной способно-
стью, при нормальных условиях обычно не устойчивы. Играют важную роль во
многих химических процессах. Радикалы в виде группы атомов обычно при
химических реакциях переходят из одного соединения в другое без изменения.
В неорганических соединениях такими радикалами являются гидроксильные
группы, кислотные остатки и т. д. В органических соединениях -остатки угле-
водородов, которые входят в состав многих органических соединений; эти ос-
татки получили название органических (углеводородных) радикалов. Они обо-
значаются буквой R.
РАДИОАКТИВНЫЕ ИЗОТОПЫ, [radio-active isotopes].
Изотопы, обладающие радиоактивностью. Бывают естественного и искусст-
венного происхождения. Первые образуются, например, при взаимодействии
94
химических элементов атмосферы с космическим излучением, вторые - из про-
дуктов распада, получающихся в ядерных реакторах, при нейтронной бомбар-
дировке атомов химических элементов и другими методами. В настоящее время
для 56 элементов известно около 700 радиоактивных изотопов естественного
происхождения и около 1700 радиоактивных изотопов искусственного проис-
хождения. Из-за своей радиоактивности радиоактивные изотопы являются
опасными. Некоторые из радиоактивных изотопов способны накапливаться в
организме животных и человека.
РАДИОНУКЛИДЫ, [radionuclides].
Часто используемое суммарное название радиоактивных изотопов, радиоак-
тивных химических элементов и радиоактивных веществ в атмосфере, гидро-
сфере, литосфере, биосфере.
РАДОН (Rn). [Radonum].
Радиоактивный химический элемент VIII группы шестого периода периоди-
ческой системы элементов. Атомный номер 86, атомная масса 222,0176. От-
крыт Ф. Дорном в 1900 г. Относится к классу р-элементов. Инертный газ без
цвета и запаха, плотность при 0°С и давлении 1 атм. - 9,73 г/л, плотность жид-
кого радона - 4,4 г/см
3
. Известно 19 радиоактивных изотопов с массовыми чис-
лами 204, 206 - 224. Как и многие другие инертные газы радон образует соеди-
нения с водой, например, Rn ·6Н
2
О. Получены также фториды радона.
Содержание в атмосфере 7 · 10
-
17% по объему, в морской воде -10
-
18% по
массе. В небольших количествах содержится во всех природных водах. Приме-
няется в медицине для приготовления радоновых ванн, при радиационной тера-
пии. В некоторых местностях уровень содержания в воздухе превышает допус-
тимый. Радон является одним из главных источников внутреннего радиоактив-
ного облучения организма. Он повсеместно поступает в окружающую среду из
земной коры, в том числе там, где имеются ее разломы. Основную часть облу-
чения от радона человек получает, находясь в закрытом, непроветриваемом по-
мещении, где радон накапливается. Наибольший вред человеку наносит попа-
дание паров воды с высоким содержанием радона в легкие вместе с вдыхаемым
воздухом. Это чаще всего происходит в ванной комнате. При обследовании до-
мов в Финляндии оказалось, что в среднем концентрация радона в ванной ком-
нате примерно в три раза больше, чем на кухне и примерно в 40 раз выше, чем в
жилых комнатах. Несмотря на химическую инертность Р. является весьма ток-
сичным веществом из-за своей радиоактивности.
РАССЕЯННЫЕ ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ, [dispersed chemical ele-
ments, scattered chemical elements].
Химические элементы, которые практически не встречаются в природе в ви-
де самостоятельных соединений, а находятся в виде примесей к различным ми-
нералам и рудам. Содержание рассеянных химических элементов в них обычно
не превышает тысячных долей процента. К рассеянным химическим элементам
относятся: рубидий Rb, таллий Т1, галлий Ga, индий In и др.
95
РАСТВОРИМОСТЬ, [solubility].
Способность вещества растворяться в том или ином растворителе с образо-
ванием однородной системы. Абсолютно нерастворимых веществ не существу-
ет. Если растворимость вещества очень мала, то считают, что данное вещество
в данном растворителе нерастворимо. Мерой растворимости служит состав
(концентрация) насыщенного раствора. Растворимость веществ зависит от их
природы, от температуры и давления, от присутствия в растворах посторонних
веществ. При повышении температуры Р. большинства твердых веществ увели-
чивается, а газов уменьшается. В зависимости от способности растворяться в
воде вещества делятся на хорошо растворимые [р], малорастворимые [м] и
практически нерастворимые [н].
РАСТВОРИТЕЛИ, [solvents].
Неорганические или органические соединения или смеси, способные раство-
рять различные вещества, образуя с ними растворы. Растворители являются
средой, в которой распределяются растворенные вещества. Типичные раство-
рители - вода, спирт, бензол. Растворитель - компонент раствора, содержащий-
ся в нем в большем количестве по сравнению с растворённым веществом. На-
ходится в том же агрегатном состоянии, что и раствор. Для растворов электро-
литов вода всегда является растворителем, даже если ее очень мало.
РАСТВОРЫ, [solutions].
Однородные гомогенные системы переменного состава, состоящие из двух и
более компонентов и продуктов их взаимодействия, не разделяющиеся на со-
ставные части со временем. Состоят из растворителя и растворенного вещест-
ва. Могут быть газообразными (воздух), жидкими (растворы солей в воде),
твердыми (сплавы металлов). В зависимости от количества растворенного ве-
щества и внешних условий растворы могут быть концентрированными, разбав-
ленными, насыщенными, ненасыщенными, пересыщенными. В зависимости от
состава растворенного вещества растворы могут иметь кислую, нейтральную
или щелочную среду. По способности проводить электрический ток разли-
чают растворы электролитов и неэлектролитов
РЕДКОЗЕМЕЛЬНЫЕ ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ, [rare chemical
earths].
Исторически сложившееся название некоторых элементов III группы перио-
дической системы элементов, включающее иттрий, лантан и лантаноиды. На-
звание сложилось в конце XVIII - начале XIX века, когда ошибочно считали,
что минералы, содержащие La, Се, Рг, Nd, Sm, Eu, Y, Gd, Tb, Dy, Ho, Er, Tu,
Ym, Lu редко встречаются в земной коре. Однако по запасам редкоземельные
элементы не являются редкими, по суммарной распространенности они превос-
ходят свинец в 10 раз, молибден в 50 раз, вольфрам в 165 раз. Редкоземельные
элементы. проявляют между собой большое сходство химических и некоторых
физических свойств, что объясняется одинаковым строением внешних элек-
тронных оболочек их атомов. Все редкоземельные элементы – металлы. их по-
лучают восстановлением соответствующих окислов, фторидов, электролизом
безводных солей и другими методами. Применяются в различных отраслях
96
техники: в радиоэлектронике, приборостроении, атомной технике, машино-
строении, химической промышленности, в металлургии
РИМСКИЕ ЦИФРЫ, [Roman numerals].
Система знаков (I, П, Ш, IV, V, VI и т. д.) для обозначения чисел, основанная
на употреблении особых знаков для десятичных разрядов: I - 1, X - 10, С - 100,
М - 1000 и их половин: V - 5, L - 50, D - 500. В химии римские цифры исполь-
зуются для обозначения номера группы в периодической системе элементов и
численной величины степени окисления (валентности) для элементов с пере-
менной степенью окисления. Например: V группа, Сu
2
О — оксид Сu (I), СuО —
оксид Сu(П).
РТУТЬ (Hg), [Hydrargyrum].
Химический элемент II группы шестого периода периодической системы
элементов. Атомный номер 80, атомная масса 200,59 Известна древним циви-
лизациям. Относится к классу d-элементов, входит в подгруппу цинка. Жидкий
серебристо-белый металл, t
пл.
38,86°С, t
кип.
356,66°С, плотность жидкой Р. 13,5
г/см
3
, твердой - 14,193 г/см
3
(при -38,9°С). Восстановитель, в соединениях про-
являет степени окисления +1 и +2. В природе встречаются семь стабильных
изотопов с массовыми числами 196, 198-202, 204. Получено искусственным пу-
тем 18 радиоактивных изотопов. Ртуть - единственный металл, остающийся
жидким при низких температурах. Заметно испаряется уже при комнатной тем-
пературе. При невысоких температурах инертна ко многим агрессивным сре-
дам, включая кислород. Хорошо растворяется в азотной кислоте и царской вод-
ке. С металлами образует сплавы, называемые амальгамами. Пары и многие со-
единения ртути токсичны.
Содержание в земной коре 4,5 · 10
-6
% по массе, в морской воде 3,34 - 4,9 ·
10
-11
%. Известно около 30 минералов, основным из которых является HgS - ки-
новарь. Мировое производство 8400 т/год. Используется для приготовления
ртутных электродов, термометров, при получении гидроксида натрия и хлора,
при переработке полиметаллического сырья, для изготовления люминесцент-
ных ламп, для калибровки мерной посуды, при изготовлении люминофоров.
Содержание в костной ткани человека 0,45 · 10
-4
%, в мышечной ткани
0,02 - 0,7 · 10
-4
%, в крови 0,0078 мг/л. Ежедневный прием с пищей - 0,004-0,02
мг: При работе с ртутью, ртутными приборами и соединениями ртути следует
соблюдать особую осторожность. Для нейтрализации ртути используют 20%
раствор хлорида железа(III) или 10% раствор КМпО
4
с добавкой соляной ки-
слоты. В первом случае происходит реакция: 2FeCl
3
+ 2Hg →2FeCl
2
+ Hg
2
Cl
2
,
по которой ртуть медленно переходит в нелетучий и малорастворимый хло-
рид ртути (I). В быту опасность могут представлять не только ртутные термо-
метры, но и старинные зеркала, у которых металлический слой часто состоял из
сплава олова и ртути. Из соединений ртути высокотоксичными являются хло-
рид ртути (II) (сулема), метилртуть - CH
3
Hg и диметилртуть. (CH
3
)
2
Hg.. Токси-
ческая доза 0,4 мг. Летальная доза 150-300 мг
97
СВИНЕЦ (РЬ), [Plumbum].
Химический элемент IV группы шестого периода периодической системы
элементов. Атомный номер 82, атомная масса 207,2. Известен древним цивили-
зациям. Относится к классу р-элементов, входит в подгруппу углерода. Синева-
то-серый металл, t
пл.
237,4°С, t
кип.
1745°С, плотность 11,34 г/см
3
. Восстанови-
тель, в соединениях проявляет степени окисления +2 и +4. Природный свинец
состоит из четырех стабильных изотопов с массовыми числами 204 и 206-208.
На воздухе покрывается оксидной пленкой, стойкой к химическим воздействи-
ям. Легко растворяется в азотной кислоте. Свинец и его соединения ядовиты.
Содержание в земной коре 1,6 · 10
-3
% по массе, в морской воде 10
-10
- 10
-9
%.
Важнейший минерал - галенит (PbS). Мировое производство около 4 · 106
т/год. Примерно треть мирового производства свинца идет на изготовление
пластин для аккумуляторов. В больших количествах он расходуется на оболоч-
ки кабелей, в качестве защитных экранов от рентгеновского и радиоактивного
излучений, для производства припоев, отливки типографского шрифта. Являет-
ся конечным продуктом радиоактивного распада урана и некоторых других тя-
желых элементов. Поэтому его количество на планете постоянно увеличивает-
ся. По оценке ученых за время существования Земли содержание свинца вслед-
ствие данного фактора увеличилось примерно на 20%.
Содержание в организме человека (масса тела 70 кг) - 120 мг, в мышечной
ткани 0,23 - 3,3 · 10
-4
%, в костной ткани 3,6 – 30 · 10
-4
%, в крови 0,21 мг/л.
Главным образом содержится в костях, печени, почках. При совместном при-
сутствии с другими металлами увеличивает их токсичность. Ежедневный прием
с пищей 0,06-0,5 мг. Токсическая доза 1 мг, летальная доза 10 г. Способен вы-
зывать раковые заболевания и уродства. ПДК 0,001 мг/л. Для очень токсичного
тетраэтилсвинца Рb(С
2
Н
5
)4, используемого в качестве добавки к бензину, ПДК
5 · 10
-6
мг/л. Одним из источников попадания соединений свинца в организм
человека может быть хрустальная посуда при длительном хранении в ней неко-
торых спиртных напитков
СЕРА (S), [Sulfur].
Химический элемент VI группы третьего периода периодической системы
элементов. Атомный номер 16, атомная масса 32,06. Извесна древним цивили-
зациям. Относится к классу р-элементов, подгруппа кислорода, халькоген. Не-
металл, t
пл.
для разных модификаций от 112,8°С до 119°С, t
кип..
444,6'С, в парах
существует в виде 2-, 4-, 6- и 8- атомных молекул. Степень окисления в соеди-
нениях -2, +2, +4 и +6. Природная сера состоит из четырех стабильных изото-
пов с массовыми числами 32 - 34 и 36. При нагревании образует химические
соединения почти со всеми элементами. К числу важнейших соединений С. от-
носятся серная кислота, сульфаты, сульфиты, сульфиды, оксиды.
Содержание в земной коре 0,05% по массе, в морской воде 9 · 10
-2
%. По рас-
пространенности в природе С. занимает 15 место среди других элементов. В
природе встречается в свободном состоянии и в виде минералов. Мировое про-
изводство 54 · 10
6
т/год. Важна для всех живых существ. Содержание в орга-
низме человека (масса тела 70 кг) - 140 г, в мышечной ткани 0,5+1,1%, в кост-
98
ной ткани 0,05-0,24%, в крови - 1800 мг/л. Ежедневный прием с пищей — 850-
930 мг. Содержится в нефти, угле, природном газе. При их сгорании образуют-
ся оксиды серы, загрязняющие окружающую среду, приводящие к образованию
кислотных дождей.
СЕРНАЯ КИСЛОТА,[sulphuric acid].
Сильная двухосновная кислородсодержащая кислота. Смешивается с водой
во всех отношениях. Один из основных продуктов химической промышленно-
сти. Широко применяется для производства минеральных удобрений, различ-
ных кислот и солей, красителей. Средние соли серной кислоты называются
сульфатами.
СИЛИКАТЫ, [silicates].
Соли кремниевых кислот, например Na
2
Si0
3
, K
4
Si0
4
, CaSiO
3
. Составляют
около 75% массы земной коры. В настоящее время известно более 1000 различ-
ных силикатов Примерами силикатов являются асбест, слюда, полевой шпат,
алюмосиликаты. Из силикатов состоят различные горные породы, например
граниты и гнейсы.
СИЛЫ ВАН-ДЕР-ВААЛЬСА, ван-дер-ваальсовское взаимодействие
(van - der-Waals forces, van-der-Waals interaction].
Силы, обеспечивающие межмолекулярное или межатомное взаимодействие
без дополнительного обобществления электронной плотности взаимодейст-
вующих молекул (атомов). Указанное взаимодействие осуществляется за счет
сил ориентационного, индукционного или дисперсионного происхождения.
Данные силы возникают за счет электростатического притяжения молекул,
имеющих постоянный дипольный момент (ориентационное взаимодействие),
наведенный (индуцированный) дипольный момент (индукционное взаимодей-
ствие), мгновенный дипольный момент (дисперсное взаимодействие). Харак-
терной особенностью является их универсальность, так как они действуют без
исключения между всеми атомами и молекулами. Однако эти силы проявляют
себя только тогда, когда молекулы находятся на близких расстояниях друг от
друга. Как правило, взаимодействие между молекулами возрастает с увеличе-
нием числа электронов в молекуле или атоме, т. е. приблизительно пропорцио-
нально их молярной или атомной массе. Увеличение сил притяжения между
более тяжелыми молекулами подтверждается тем, что в рядах родственных мо-
лекул температуры кипения. растут с увеличением молекулярной массы. Разно-
видностью является водородная связь.
СИЛЬНЫЕ ВОССТАНОВИТЕЛИ, [strong reductants).
Восстановители, выступающие в окислительно-восстановительных реакциях
только в качестве восстановителей. Наиболее сильными восстановителями яв-
ляются щелочные и щелочноземельные металлы, стоящие в начале ряда актив-
ности металлов, а также многие элементы в низшей степени окисления, напри-
мер: S
-2
, N
-3
. Количественной характеристикой активности (силы) восстанови-
теля и окислителя является стандартный окислительно-восстановительный по-
тенциал. Стандартные значения таких потенциалов можно найти в специальных
таблицах. Восстановительные свойства тем сильнее, а окислительные свойства

99
тем слабее, чем меньше алгебраическая величина стандартного окислительно-
восстановительного потенциала, и наоборот.
СИЛЬНЫЕ ОКИСЛИТЕЛИ, [strong oxidants, strong oxidizing agents].
Окислители, выступающие в окислительно-восстановительных реакциях
только (или как правило) в качестве окислителей. Наиболее сильными окисли-
телями являются галогены, кислород, а также неметаллы и металлы в высшей
степени окисления, например: Сг
+6
, Мп
+7
, S
+6
, N
+5
. Количественной характери-
стикой активности (силы) окислителя и восстановителя является стандартный
окислительно-восстановительный потенциал. Окислительные свойства тем
сильнее, а восстановительные тем слабее, чем больше алгебраическая величина
окислительно-восстановительного потенциала, и наоборот.
СТРАТОСФЕРА [stratosphere].
Название части атмосферной оболочки нашей планеты; располагается над
тропосферой на высоте 12-50 км над поверхностью Земли. В стратосфере нахо-
дится основное количество озона (озоносфера).
СУЛЬФАТЫ, [sulphates].
Соли серной кислоты H
2
SO
4
, содержащие кислотный остаток SO
4
-2
, напри-
мер: Na
2
SO
4
, A1
2
(SO
4
)
3
. В сульфатах степень окисления серы +6. Сильная двух-
основная серная кислота может образовывать средние (нормальные) соли - С. и
кислые соли – гидросульфаты, например: K
2
SO
4
- сульфат калия, KHSO
4
- гид-
росульфат калия. Большинство сульфатов, кроме BaSO
4
, RaSO
4
, хорошо рас-
творимо в воде, плохо растворимы CaSO
4
, SrSO
4
, PbSO
4
. Многие сульфаты
встречаются в природе в качестве минералов. Кристаллогидраты сульфатов не-
которых металлов (например, железа (+2), кобальта (+2), никеля, цинка, меди)
часто называют купоросами, а двойных солей - квасцами.
СУЛЬФИДЫ МЕТАЛЛОВ, [metal sulphides].
Соли сероводородной кислоты H
2
S. Например: Na
2
S, PbS. Степень окисле-
ния серы в сульфидах металлов -2. Как двухосновная кислота H
2
S может обра-
зовывать средние соли – сульфиды металлов и кислые соли - гидросульфиды.
Например: K
2
S - сульфид калия, KHS - гидросульфид калия. Большинство
сульфидов металлов нерастворимо в воде. Исключение - сульфиды щелочных и
щелочноземельных металлов. Сульфиды металлов - сильные восстановители.
СУЛЬФИТЫ, [sulphites].
Соли сернистой кислоты H
2
SO
3
, содержащие кислотный остаток SO
3
2-
. На-
пример: Na
2
SO
3
, CuSO
3
. Степень окисления в них серы +4. Как двухосновная
кислота сернистая кислота может образовывать средние соли – сульфиты и
кислые соли — гидросульфиты. Например: K
2
SO
3
- сульфит калия, KHSO
3
-
гидросульфит калия. В воде хорошо растворимы лишь сульфиты щелочных ме-
таллов. Сульфиты во многих окислительно-восстановительных процессах яв-
ляются восстановителями. При их окислении получаются сульфаты. С более
сильными восстановителями выступают в качестве окислителей. При их вос-
становлении образуется элементарная сера или сульфиды. Большое количество
сульфитов содержится в окружающей среде. По своей природе они более ток-
100
сичны, чем сульфаты. При попадании в организм человека превращение суль-
фитов в сульфаты происходит в печени при участии ферментов.
S-ЭЛЕМЕНТЫ, [s-block elements].
Элементы I и II групп главных подгрупп периодической системы элементов.
Атомы этих элементов на внешней электронной оболочке имеют один или два
s-электрона. Элементы первой подгруппы называются щелочными металлами.
К ним относятся: литий, натрий, калий, рубидий, цезий, франций. Элементы
второй подгруппы называются щелочноземельными металлами. К ним относят-
ся: бериллий, магний, кальций, стронций, барий, радий. Сильные восстановите-
ли, проявляют степени окисления +1 или +2. Обладают повышенной химиче-
ской активностью, некоторые самовоспламеняются на воздухе. Взрыво- и по-
жароопасны. Ряд s-элементов и их соединений токсичны.
Таллий (Ti), [Thallium].
Химический элемент III группы шестого периода периодической системы
элементов. Атомный номер 81, атомная масса 204,37. Открыт У. Круксом в
1861 г. Относится к классу р-элементов. Мягкий серебристо-белый металл, t
пл.
303,6°C, t
кип.
1457°С, плотность 11,849 г/см
3
. Восстановитель, в соединениях
проявляет степень окисления +1 и +3. Природный таллий состоит из двух ста-
бильных изотопов с массовыми числами 203 и 205. При комнатной температуре
покрывается оксидной пленкой, реагирует с галогенами, азотной и серной ки-
слотами. Со щелочами не взаимодействует, медленно реагирует с водой при
наличии воздуха. Таллий и его соединения весьма токсичны.
Содержание в земной коре 4,6 · 10
-6
% по массе, в морской воде 1,4 · 10
-9
%.
Входит как примесь в минералы других элементов. Мировое производство око-
ло 30 т/ год. Используется для получения полупроводниковых материалов, при
изготовлении подшипниковых сплавов, оптических стекол.
Содержание в мышечной ткани человека 7 · 10
-6
%, в костной ткани 2 · 10
-
7
%, в крови 0,00048 мг/л. Ежедневный прием с пищей - 0,0015 мг. При работе с
таллием и его соединениями необходимо строгое соблюдение правил техники
безопасности. Способен вызывать уродства, по некоторым данным способству-
ет выпадению волос. Летальная доза 600 мг.
ТЕМПЕРАТУРА КИПЕНИЯ [boiling temperature].
Температура, при которой давление пара над поверхностью жидкости (веще-
ства в жидком состоянии) становится равным внешнему давлению. Важнейшая
характеристика вещества.
ТЕМПЕРАТУРА ПЛАВЛЕНИЯ [melting temperature].
Температура перехода кристаллического вещества в жидкое состояние.
Важнейшая характеристика вещества.
ТОКСИЧНОСТЬ, [toxicity].
Свойство веществ вызывать отравление организма. Характеризуется дозой
вещества, вызывающей ту или иную степень отравления. Различают токсиче-
скую и летальную дозы. Первая характеризует минимальное количество ток-
сичного вещества, вызывающего появление устойчивых признаков отравления,
