Санагурський Д.І. Об’єкти біофізики: монографія
Подождите немного. Документ загружается.

71
На рис. 2.7 зображено зміни активності Na
+
, K
+
–АТФ-ази
(а) та динаміки ТМП зародків в’юна (б) за наявності в
інкубаційному середовищі катіонів нікелю, порівняно з контролем.
Вплив катіонів нікелю у концентрації 10
-6
М веде до помітного
зменшення як активності Na
+
, K
+
–ATФ-ази, так і абсолютних
значень ТМП, яке стає більш вираженим із збільшенням
концентрації катіонів металу до 10
-5
М. Ймовірно, що в той
момент, як в контролі на стадіях VI–X поділу бластомерів
активність Na
+
, K
+
–АТФ-ази та значення потенціалу збільшуються,
в разі дії катіонів нікелю на цих стадіях спостерігається зменшення
значень обидвох показників.
За умов впливу катіонів кобальту (рис. 2.8) зміни є
подібними, але менш вираженими. Значне зменшення активності
Na
+
, K
+
–АТФ-ази (а) та рівня ТМП зародків (б) спричиняв вплив
катіонів кобальту в концентрації 10
-4
М. Вплив катіонів Со
2+
у
концентрації 10
-5
М був менш помітним.
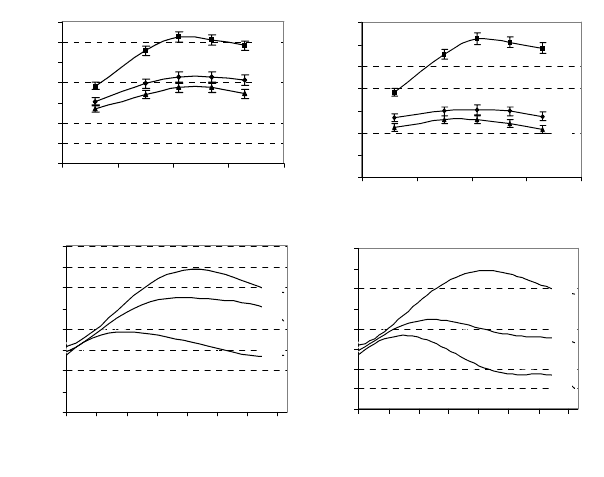
На рис. 2.9 зображено зміни активності Na
+
, K
+
–ATФ-ази
(а) та динаміки ТМП зародків в’юна (б) унаслідок впливу катіонів
марганцю в концентрації 10
-5
М та 10
-6
М, порівняно з контролем.
Очевидно, що вплив катіонів марганцю зумовлює зменшення
активності Na
+
, K
+
–ATФ-ази (а) і зменшення абсолютних значень
потенціалу (б). Зміни є більш вираженими при дії катіонів
марганцю в концентрації 10
-5
М.
72
*
*
** **
*
*
*
**
*
4
6
8
10
12
14
16
18
0 100 200 300 400
t, хв
А, мкмоль Рн/мг білка х год
Рис. 2.9. Зміни активності
Na
+
, K
+
–АТФ-ази (а) та рівня
ТМП (б) при дії катіонів Mn
2+
в
концентраціях 10
-6
M (криві 2) і
10
-5
M (криві 3), порівняно з
контролем (криві 1).
* – р < 0,05, ** – р < 0,01.
Рис. 2.10. Зміни активності
Na
+
, K
+
–АТФ-ази (а) та рівня
ТМП (б) при дії катіонів Sn
2+
в
концентраціях 10
-5
М (криві 2) і
10
-4
М (криві 3), порівняно з
контролем (криві 1).
* – р < 0,05, ** – р < 0,01.
Результати впливу катіонів олова на досліджувані
показники показано на рис. 2.10. Ці зміни, як і в попередніх
прикладах, є залежними від концентрації: при дії катіонів олова в
концентрації 10
-5
М активність Na
+
, K
+
-ATФ-ази зародків в’юна (а)
зменшувалась, як і абсолютні значення ТМП (б). За наявності
катіонів олова в концентрації 10
-4
М деполяризація мембрани була
більш вираженою, як і зменшення активності АТФ-ази.
30
35
40
45
50
55
60
65
70
180 210 240 270 300 330 360 390
t, хв
Е, -мВ
30
35
40
45
50
55
60
65
70
180 210 240 270 300 330 360 390
t, хв
Е, -мВ
**
*
*
**
*
**
** *
**
**
4
6
8
10
12
14
16
18
0 100 200 300 400
t, хв
А, мкмоль Рн/мг білка х год
а
б б
а
2
1
3
1
2
3
1
2
3
1
2
3
73
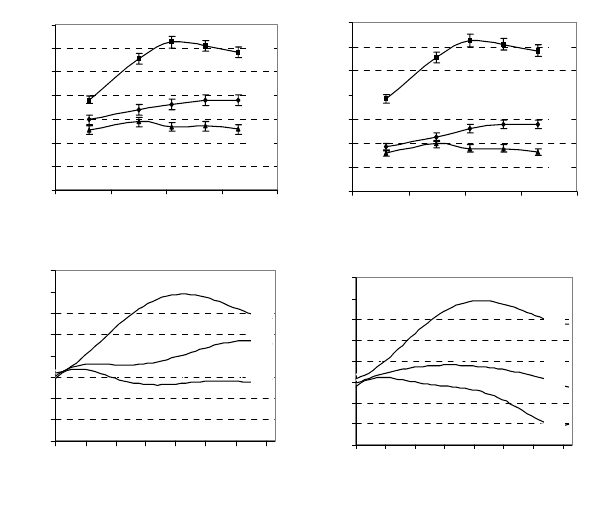
Вплив катіонів цинку (рис. 2.11) зумовлював подібні зміни
як активності Na
+
, K
+
–ATФ-ази (а), так і значень потенціалу
зародків в’юна (б). Причому у разі впливу катіонів цинку в
концентрації 10
-5
М ці зміни були більш суттєвими, ніж при
концентрації катіонів 10
-6
М.
На рис. 2.12 зображено зміни АТФ-азної активності (а) та
динаміки ТМП зародків в’юна (б) за умов впливу катіонів кадмію.
Активність Na
+
, K
+
–ATФ-ази зародків при дії цих катіонів, як і при
дії катіонів нікелю, зменшувалась суттєвіше, ніж унаслідок впливу
катіонів інших металів. Як і в інших дослідах, вплив катіонів
кадмію в концентрації 10
-5
М приводив до більш значних змін обох
показників, ніж вплив катіонів кадмію в концентрації 10
-6
М.
Отже, загалом можна сказати, що дія катіонів важких
металів приводила до залежного від концентрації зменшення
активності Na
+
, K
+
–ATФ-ази і до подібного за характером змін
зменшення абсолютних значень ТМП зародків в’юна на стадії
дроблення бластомерів. Більш виражене зниження активності
ферменту помпи простежували в більш суттєвій деполяризації
мембрани. Причому, якщо в контролі активність Na
+
, K
+
–АТФ-ази
зростала від запліднення до стадії 64 бластомерів, то за умов
впливу катіонів металів активність цього ферменту зменшувалась
або зростала незначно протягом періоду дроблення, як і абсолютні
значення ТМП зародків у нормі та при дії катіонів важких металів.
74
Рис. 2.11. Зміни активності
Na
+
, K
+
–АТФ-ази (а) та рівня
ТМП (б) при дії катіонів Zn
2+
в
концентраціях 10
-6
M (криві 2) і
10
-5
M (криві 3), порівняно з
контролем (криві 1).
* – р < 0,05, ** – р < 0,01
Рис. 2.12. Зміни активності
Na
+
, K
+
–АТФ-ази (а) та рівня
ТМП (б) при дії катіонів Cd
2+
в
концентраціях 10
-6
M (криві 2) і
10
-5
M (криві 3), порівняно з
контролем (криві 1).
* – р < 0,05, ** – р < 0,01
Аналізуючи проведене порівняння, можна вважати, що
інгібування Na
+
, K
+
–АТФ-ази катіонами досліджуваних важких
металів може бути однією з основних причин змін рівня ТМП
зародків в’юна внаслідок впливу катіонів важких металів.
Інгібування Na
+
, K
+
–АТФ-ази катіонами важких металів може
здійснюватись, зокрема, шляхом зв’язування катіонів металів з
сірковмісними групами ферменту (Л.С. Вовканич, Л.О. Дубицький,
1998; Л.О. Дубицький, Л.С. Вовканич, 2000; G.H. Zhang et al., 1990).
*
*
*
*
*
*
**
**
*
*
4
6
8
10
12
14
16
18
0 100 200 300 400
t, хв
А, мкмоль Р
н
/мг білка х год
30
35
40
45
50
55
60
65
70
180 210 240 270 300 330 360 390
t,хв
Е, -мВ
**
**
**
** **
**
**
**
**
*
4
6
8
10
12
14
16
18
0 100 200 300 400
t, хв
А, мкмоль Р
н
/мг білка х год
1
2
3
1
2
3
1
2
3
а а
б б
30
35
40
45
50
55
60
65
70
180 210 240 270 300 330 360 390
t, хв
Е, мВ
1
2
3
75
Доведено (Л.О. Дубицький, Л.С. Вовканич, 2000; 2001;
2003), що інгібувальні ефекти катіонів металів на транспортні
системи мембран залежать від їхніх фізико-хімічних властивостей,
зокрема, від іонного радіуса, ентальпії гідратації, констант
стійкості комплексів металів з біолігандами, SH-лігандами.
Згідно з теорією жорстких і м’яких кислот і основ,
розробленою Пірсоном (Ю.А. Ершов, Т.В. Плетенева, 1989),
катіони металів з великою електронною оболонкою атомів, що
легко поляризуються (м’які кислоти Льюіса), високоспоріднені з
м’якими основами, що мають низьку електронегативність,
зокрема, з групами –SH і –SR (Ю.М. Торчинский, 1977). Відповідно
до припущення цього кадмій належить до м’яких кислот, нікель,
цинк, олово, кобальт – до проміжних, марганець – жорстка
кислота (Ю.А. Ершов, Т.В. Плетенева, 1989). Стає зрозумілим, чому
марганець впливає на активність Na
+
, K
+
–АТФ-ази найменше, а
кадмій – найбільше. Очевидно, такі результати пов’язані саме з
утворенням комплексів металів з SH-групами Na
+
, K
+
–АТФ-ази.
Вплив на активність ферменту металів, що належать до проміжних
кислот, виражений по-різному, що залежить, можливо, від інших
фізико-хімічних властивостей цих металів.
Одержані результати щодо інгібування Na
+
, K
+
–АТФ-ази
катіонами важких металів значно підтверджуються змінами
ультраструктури бластомерів зародків в’юна, які були інкубовані за
наявності катіонів застосованих важких металів.
Крім структурних пошкоджень органел бластомерів за
умов впливу катіонів важких металів, спостерігався набряк
цитоплазми та органел бластомерів. Найбільше такі зміни були
виражені на стадії 16 бластомерів та стадії морули. Простежували
76
зменшення хвилястості плазматичної мембрани, порівняно з
контролем, розрідження гіалоплазми, набряк органел. Це,
очевидно, пов’язано з надмірним надходженням води у клітину,
яке супроводжує вхід у клітину йонів Na
+
(Е.А. Гойда, 1993).
Надлишок води в цитоплазмі може бути пов’язаний зі
зменшенням виходу з клітини йонів натрію, що свідчить про
порушення активного транспортування, яке виводить надлишок
Na
+
з клітини, а отже, – про зниження активності Na
+
, K
+
–АТФ-ази
внаслідок досліджуваних впливів.
Цікавим результатом, одержаним унаслідок проведених
досліджень, є збільшення періоду коливань ТМП зародків в’юна
через вплив катіонів досліджуваних металів, порівняно з
контролем. Як було встановлено за допомогою спектрального
аналізу, збільшення періоду (зменшення частоти) коливань
потенціалу спостерігались у всіх дослідах впливу катіонів
досліджуваних металів. Найсуттєвіше збільшення періоду
відбувалося у разі впливу катіонів нікелю, олова та кадмію,
найменш виражене – при дії катіонів кобальту. Оскільки
тривалість періоду коливань потенціалу збігається з тривалістю
клітинного циклу зародків в’юна, збільшення періоду свідчить про
сповільнення розвитку зародків. Це було підтверджено візуальним
спостереженням під час розвитку зародків та личинок в’юна за
допомогою бінокулярного мікроскопа.
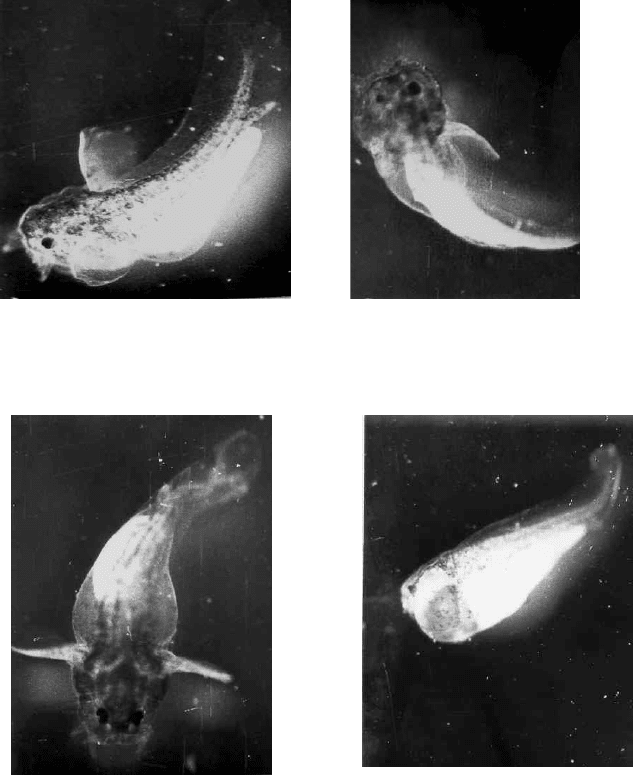
Личинки в’юна у віці 10 діб, які розвивались у нормальних
умовах, були рухливими, мали подовгасту форму тіла, розвинені
плавці та зябра, виражену пігментацію (рис. 2.13). Жовткового
міхура на цій стадії не було.

77
Личинки того ж віку, що розвивалися за наявності в
інкубаційному середовищі катіонів важких металів в концентрації
10
-5
М, мали певні аномалії розвитку. Добре помітним було
відставання розвитку цих личинок, порівняно з контролем: вони
мали менші розміри та залишки жовткового міхура (рис. 2.14–
2.17).
У таких личинок спостерігали суттєві вади розвитку, а
саме: викривлення та перекручення хребта (рис. 2.14), деформацію
кісток черепа та збільшення розмірів голови (рис. 2.15), значний
набряк черевної порожнини (рис. 2.16), недорозвинені плавці,
зябра, вусики (рис. 2.17). Личинки були малорухливими,
серцебиття сповільнене.
Такі аномалії розвитку личинок в’юна виявлено приблизно
в 25–30 % зародків, що збігається з даними, що були одержані на
зародках X. laevis (М.С. Plowman et al., 1991; 1994; F.W.Jr.
Sunderman et al., 1991; 1992; 1995; 1996). Решта личинок, в яких не
Рис. 2.13. Личинки в’юна у віці 10 діб, які розвивались у нормальних
умовах
78
спостерігали виражені аномалії розвитку, були, однак,
малорухливими, їхня шкіра була незначно пігментована,
порівняно з контролем.
Рис. 2.14. Аномалії розвитку у
личинок в’юна, що розвивались за
наявності йонів нікелю (10
-5
М)
Рис. 2.15. Аномалії розвитку у
личинок в’юна, що розвивались за
наявності йонів марганцю (10
-5
М)
Рис. 2.16. Аномалії розвитку у
личинок в’юна, що розвивались за
наявності йонів кадмію (10
-5
М)
Рис. 2.17. Аномалії розвитку у
личинок в’юна, що розвивались
за наявності йонів олова (10
-5
М)

79
Оскільки зародки в’юна Missgurnus fossilis L. є досить
чутливим об’єктом щодо зовнішніх збурень, зокрема, динаміка
їхнього трансмембранного потенціалу суттєво змінюється
внаслідок впливу різних речовин, зокрема гормонів (Е.А. Гойда,
1993), факторів росту (Е.А. Гойда и др., 1981), антибіотиків
(Н.М. Бойко, Д.І. Санагурський, 2000; Е.А. Гойда, 1993), катіонів
важких металів (Н.М. Бойко, Д.І. Санагурський, 2000; Н.М. Бойко
та ін., 2002), та таких фізичних факторів, як відмінні від
нормальних умов температура та атмосферний тиск (Е.А. Гойда,
1993), можна запропонувати цей об’єкт як тест-систему при
вивченні впливу різних фармакологічних, хімічних та біологічних
субстанцій на живі об’єкти.
2.4. Áåçïåðåðâíå ðåºñòðóâàííÿ
ÒÌÏ
Для отримання безперервної інформації
впродовж всього періоду раннього розвитку зародків при
мінімальному порушенні їхньої морфологічної і функціональної
цілісності, використано методику реєстрування ТМП, добре
апробовану на рослинних об’єктах (В.К. Адрианов и др., 1968), з
частковою власною модифікацією, відповідно до вимог
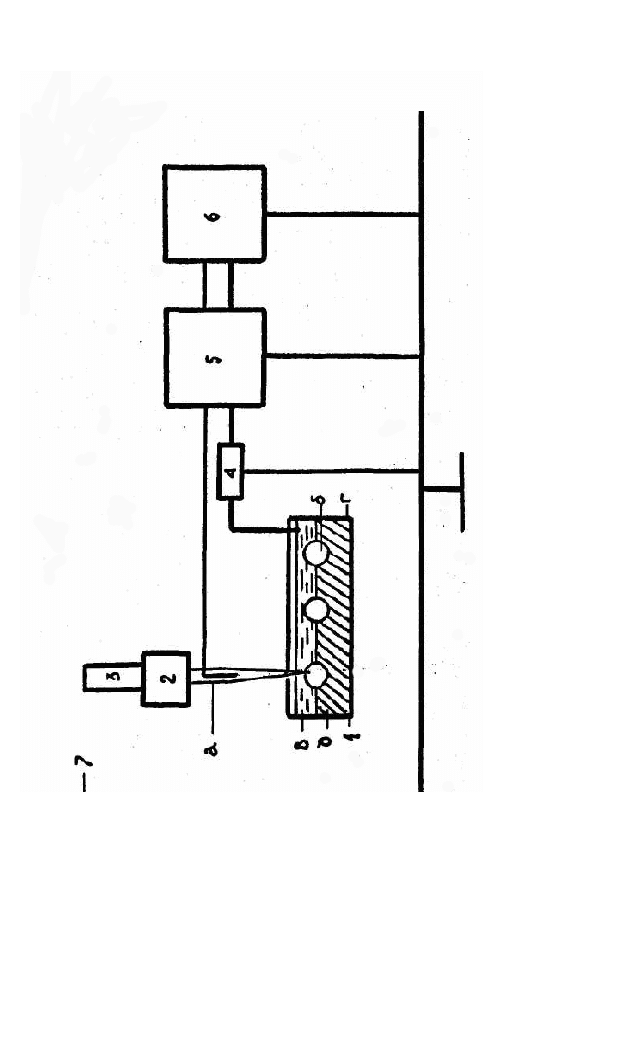
досліджуваного об’єкта. Загальна блок-схема установки для
одноканальних відведень зображена на рис. 2.18. Багатоканальні
відведення складаються з аналогічних елементів, які замикаються
на досліджуваному об’єкті, в нашому разі – ікра в’юна (рис. 2.18 б,
2.19).
80
Рис. 2.18. Блок-схема установки для безперервного реєстрування ТМП у зародків в’юна, що розвиваються:
1 – камера з кюветою для об’єкта дослідження; б – об’єкт дослідження; д – агаровий блок; а – мікроелектрод; в – індеферентний
мікроелектрод; 7 – екран; 2, 3 – блоки маніпулятора; 5 – рН-метр; 6 – самописний електронний потенціометр
