Коган В.Е., Зенин В.С., Пенкина Н.В. Физическая химия. Часть 2. Химическая кинетика
Подождите немного. Документ загружается.


В. Е. Коган, Г. С. Зенин, Н. В. Пенкина
10
довательно, скорость химической реакции связана со скоростью изменения
концентрации реагентов и продуктов через стехиометрические коэффициенты
() () () ()
Q
BE R
1111
dc
dc dc dc
bd ed qd rd
====
−τ−τ+τ+τ
v . (2.4)
Формула (2.2) позволяет заключить, что
скорость гомогенной химиче-
ской реакции, идущей при постоянном объеме, по одному из компонентов
есть изменение концентрации этого компонента в единицу времени
, т. е.
скорость такой химической реакции по одному из компонентов, как и ско-
рость химической реакции [см. формулу (2.4)], выражается в единицах
[концентрация] : [время].
В химии обычно имеют дело с молярной концентрацией [1, 13], выра-
жаемой в моль/л
3
кмоль/м
⎡
⎤
⎣
⎦
. Время измеряют в секундах. Таким образом,
скорость гомогенной химической реакции по одному из компонентов, как и
скорость такой химической реакции, измеряют в
(
)
моль/ лс
⋅
(
)
3
кмоль/ мс
⎡⎤
⋅
⎣⎦
1
.
С учетом вышеприведенного понятия «реакционное пространство» для
гетероген-
ных реакций, протекающих на поверхности раздела фаз
2
, единица измерения
скорости реакции – один
(
)
2
моль/ мс
⋅
(
)
2
один кмоль/ м c
⎡
⎤
⋅
⎢
⎥
⎣
⎦
.
Скорость простой гомогенной реакции равна числу элементарных хими-
ческих актов, которые осуществляются в единице объема в единицу времени.
Скорость реакции совпадает с ее скоростью по одному из компонентов, ес-
ли его стехиометрический коэффициент равен единице
[см. уравнения (2.2),
(2.4)
].
В сложной многостадийной реакции скорость суммарного процесса мо-
жет существенно отличаться от скорости отдельных стадий. Исходя из этого
понятно, что
по изменению концентрации промежуточных продуктов су-
дить о скорости суммарного процесса, как правило, нельзя
.
Для реакции в газовой среде, когда вместо концентраций реактантов мо-
гут использоваться их парциальные давления
i
p
, вместо выражений (2.2), (2.4)
соответственно имеем
1
Единица измерения молярной концентрации в СИ [13, 14] – один
3
моль/м , а следовательно,
единица измерения скорости гомогенной химической реакции – один
()
3
моль/ м c⋅ .
2
Речь идет о гетерогенных реакциях, протекающих на поверхности непористых тел.

Х и м и ч е с к а я к и н е т и к а
11
/
i
dp d
=
±τ
i
v , (2.5)
() () () ()
Q
BE R
1111
dp
dp dp dp
bd ed qd rd
====
−τ−τ+τ+τ
v . (2.6)
В соответствии с уравнениями (2.5), (2.6) скорость химической реакции в
газовой фазе по одному из компонентов, как и скорость такой химической ре-
акции, измеряют в Па/с
Кривые, характеризующие изменение концентрации реактантов (или
связанного с ними свойства системы
) во времени в результате протекания
химической реакции
(ее элементарной стадии для сложных реакций), на-
зывают кинетическими кривыми
. Зависимость концентрации компонента от
времени протекания реакции может быть выражена в графической, табличной
или аналитической форме.
Аналитическое выражение кинетической кривой
компонента
(
)
i
с τ называется уравнением кинетической кривой. Типы кине-
тических кривых разнообразны. Влияние различных факторов на вид кинетиче-
ской кривой и различные типы кинетических кривых обобщены в [2]. Некото-
рые из них будут нами рассмотрены подробно при изложении специфики про-
текания тех или иных химических реакций. Кинетические кривые широко ис-
пользуются на практике, так как тангенс
угла наклона касательной к кинетиче-
ской кривой является графической интерпретацией скорости химической реак-
ции (ее элементарной стадии).
Химическая реакция, как уже отмечалось, происходит при столкновении
частиц, обладающих определенным запасом энергии, так называемые
эффек-
тивные столкновения
(подробно этот процесс будет рассмотрен в 2.2.2.1 –
2.2.2.3). Является очевидным тот факт, что увеличение числа частиц, т. е. их
концентрации, приводит к увеличению числа столкновений между частицами, а
следовательно, к росту скорости химической реакции.
Для простых реакций или элементарных стадий сложных реакций спра-
ведлив
закон действующих масс (действия масс), установленный Гульдбер-
гом и Вааге и, как известно из химической термодинамики [3], выражающий
константу равновесия реакции.
Для химической реакции, схематически представленной как
ABD
ABDПродуктыnnn++→ , (2.7)
на основе закона действующих масс скорость будет равна

В. Е. Коган, Г. С. Зенин, Н. В. Пенкина
12
A
BD
ABD
,
n
nn
kc c c=v
(2.8)
где
A
n ,
B
n ,
D
n – стехиометрические коэффициенты, а
k
– коэффициент про-
порциональности, называемый
константой скорости реакции, или удельной
скоростью реакции
. Величина k численно равна скорости реакции при кон-
центрациях всех реактантов, равных единице. Она является величиной
по-
стоянной при данной температуре
. Таким образом, как
и константа равновесия
[3], константа скорости реакции зависит только от
температуры и природы реактантов
.
Уравнения типа (2.8), характеризующие зависимость скорости химиче-
ской реакции от концентрации реагентов, называют
кинетическими уравне-
ниями химических реакций
(химических процессов). Следует подчеркнуть,
что выражения (2.3), (2.4) и (2.8) справедливы лишь в случае гомогенных реак-
ций. В случае гетерогенных реакций, как и для константы равновесия [3], в ки-
нетические уравнения входят
только концентрации газообразных (для сис-
тем «газ – жидкость» и «газ – твердое тело») или
растворенных (для систем
«раствор – твердое тело» и «раствор – жидкость)
реагентов
1
. При этом по из-
менению концентрации
только газообразных или растворенных реактантов
можно оценивать скорость реакции.
В соответствии с кинетическим уравнением (2.8)
скорость простой или
элементарной стадии сложной химической реакции пропорциональна
концентрации реагентов, взятых в степени, равной их стехиометрическим
коэффициентам.
Рассматриваемое кинетическое уравнение применимо для идеальных сис-
тем, в частности для
идеальных и разбавленных растворов. Для реальных
концентрированных растворов, как известно [3], вместо концентрации исполь-
зуют активность. Напомним, что
активность – это такая концентрация, при
использовании которой реальные растворы приобретают термодинамиче-
ские свойства идеальных растворов.
Активность имеет размерность концен-
трации [1] и определяется выражением
a
ac
=
γ
, (2.9)
где
a
γ – безразмерный коэффициент активности, зависящий от концентра-
ции и температуры;
c – концентрация реального раствора. С учетом сказанно-
1
Обычно говорят, что концентрации жидких и твердых реагентов возводятся в нулевую сте-
пень.

Х и м и ч е с к а я к и н е т и к а
13
го, скорость химической реакции для реальных концентрированных растворов
представляют в виде
A
BD
ABD
n
nn
ka a a=v
, (2.10)
где
A
a ,
B
a ,
D
a – активности компонентов A, B, D в растворе.
Концентрация и активность в формулах (2.8) и (2.10) могут быть выраже-
ны в различных концентрационных единицах. Однако, исходя из того, что для
гомогенных химических реакций реакционным пространством является объем,
удобнее пользоваться молярной концентрацией.
2.2.1.2. Кинетическая классификация химических реакций
В отношении кинетики химические реакции разделяют по признаку
мо-
лекулярности реакции
и по признаку порядка реакции.
Молекулярность химической реакции – это число частиц-реагентов
(молекул, атомов, радикалов, ионов, т. е. любых формульных единиц
1
), одно-
временно участвующих в элементарном химическом акте
. Молекулярность
нельзя отождествлять со стехиометрическими коэффициентами сложной хими-
ческой реакции
2
, которые показывают лишь соотношение между количеством
реактантов. Сложная же реакция протекает через несколько элементарных ста-
дий, которые могут характеризоваться различной молекулярностью. В общем
случае молекулярность следует рассматривать применительно к простым реак-
циям и элементарным стадиям сложных реакций.
Различают
моно-, би- и тримолекулярные реакции. За время элемен-
тарного химического акта
(
15 13
10 10 c
−−
−
) вероятность одновременного
столкновения и взаимодействия трех частиц-реагентов крайне мала – такие
столкновения следует рассматривать скорее как исключения, чем правила. По-
этому
тримолекулярные реакции встречаются сравнительно редко. Примером
такой реакции может служить реакция восстановления оксида азота(II) водоро-
дом, отвечающая уравнению
1
Обозначаемая формулой частица может быть как реально существующей (атом, молекула,
простой или сложный ион), так и условной, реально не существующей («условная молеку-
ла»). Реальная или условная частица, обозначаемая химической формулой, называется фор-
мульной единицей.
2
В некоторых случаях, но только при возможности рассмотрения сложной реакции как фор-
мально простой (см. ниже), подобное отождествление допустимо.

В. Е. Коган, Г. С. Зенин, Н. В. Пенкина
14
22 2
2NO H N O H O
+
→+.
Участие в реакции более трех частиц-реагентов означает, что процесс
протекает через несколько промежуточных стадий, каждая из которых моно-,
би- или тримолекулярна. Например, в реакции, отвечающей уравнению
2+ + 3+
22
4Fe +4H +O 4Fe +2H O→ ,
участвуют девять частиц-реагентов и сумма стехиометрических коэффициен-
тов, стоящих перед их формулами в уравнении реакции, равна девяти. Меха-
низм этой реакции, как было доказано, состоит из семи последовательных би-
молекулярных стадий, т. е. в каждом из семи последовательных элементарных
актов встречаются две частицы.
В то же время, следует
помнить о том, что участие в реакции одной, двух
или трех частиц не обязательно указывает на то, что реакция является простой.
Так, например, длительное время считалось, что реакция, отвечающая уравне-
нию
22
H+I 2HI→ , (2.11)
является простой бимолекулярной реакцией. Однако (см. [5]) было доказано,
что данная реакция является сложной и, строго говоря, можно рассматривать
молекулярность лишь применительно к ее элементарным стадиям. Механизм
данной реакции – это три последовательные элементарные стадии, описывае-
мые уравнениями (2.12), некоторые из которых могут быть обратимыми (дву-
сторонними), что для простоты не
рассматривается:
(
)
()
()
2
2
2
I2I;
I H HI H;
2H H .
a
б
в
→
+→+
→
(2.12)
На стадии
(
)
a происходит гемолитический разрыв (электронная пара
разрывается) ковалентной связи молекулы иода с образованием двух свобод-
ных атомов иода, обладающих неспаренным электроном
(
)
I
1
. На стадии
(
)
б I
легко отрывает атом водорода от молекулы
2
H . Стадия
(
)
б механизма реакции,
описываемого уравнениями (2.12), значительно более вероятна, чем реакция,
1
Активная частица с некомпенсированной валентностью обозначается точкой над химиче-
ским символом атома, обладающего неспаренным электроном.
Х и м и ч е с к а я к и н е т и к а
15
уравнение которой (2.11), так как последняя связана с одновременным разры-
вом двух химических связей и образованием двух новых связей, в то время как
на стадии
(
)
б одновременно разрывается одна и образуется тоже одна химиче-
ская связь. При классическом продолжении цепной реакции (см. 2.2.1.7) обра-
зовавшийся атом
H
должен был бы оторвать атом иода от молекулы
2
I с появ-
лением в результате атома I
, вступающего в реакцию со следующей молекулой
2
H , и т. д. Однако в рассматриваемом случае на стадии
(
)
в механизма реакции,
описываемого уравнениями (2.12), происходит обрыв цепи. В сумме уравнения
трех последовательных стадий (уравнение стадии
(
)
б нужно умножить на два)
дают уравнение реакции (2.11).
Приведенный пример наглядно показывает, что уравнение сложной реак-
ции (2.11) не отражает истинный механизм реакции, которая в действительно-
сти состоит из трех элементарных стадий. В рассматриваемой реакции участ-
вуют пять реактантов; из них два – реагенты (
2
H,
2
I), один – продукт
(
)
HI и
два – промежуточные продукты (H
и I
).
В
мономолекулярных реакциях участвует одна частица-реагент. К числу
мономолекулярных относятся реакции, связанные с внутримолекулярным пре-
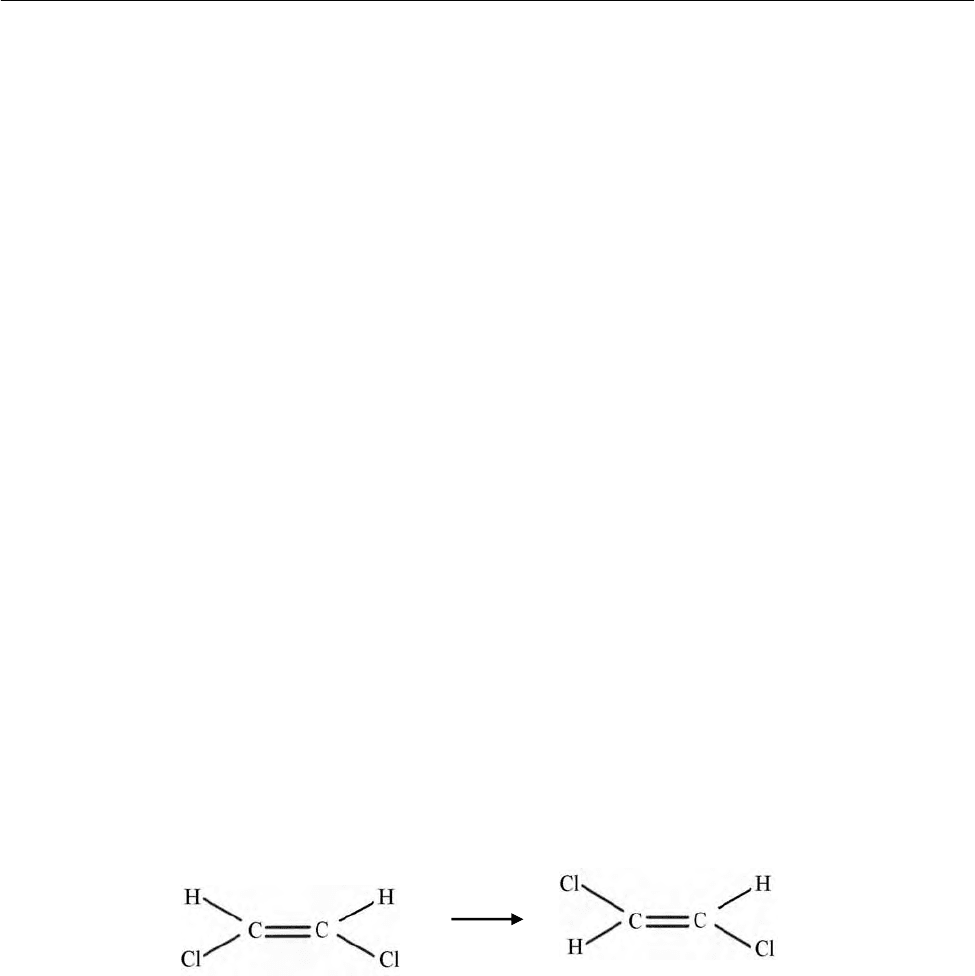
вращением – изомеризацией и распадом одной частицы на несколько других.
Примером изомеризации может служить переход цис-изомера дихлорэтана в
транс-изомер:
а примером распада одной частицы – распад молекулы азометана на два сво-
бодных метильных радикала и молекулу азота
:
3332
CH N N CH 2CH N−=− → +
.
Примером
бимолекулярной реакции является щелочной гидролиз метилио-
дида, протекание которого отражает уравнение
33
CH I OH CH OH I
−
−
+
→+
.
,

В. Е. Коган, Г. С. Зенин, Н. В. Пенкина
16
Перейдем к рассмотрению второго признака, лежащего в основе кинети-
ческой классификации химических реакций – к
порядку реакции. Различают
частный (по данному реагенту) и общий порядки.
В общем случае кинетическое уравнение может иметь довольно сложный
вид, но часто скорость является степенной функцией концентраций реагентов.
Частный порядок
X
n
реакции – это показатель степени при концентрации
одного из реагентов в кинетическом уравнении, а общий порядок
(порядок)
n реакции – сумма показателей степеней при концентрациях всех реаген-
тов.
При этом для простых реакций (и элементарных стадий сложных реакций)
порядок реакций определяется значениями стехиометрических коэффициентов.
Так, для гомогенной
1
простой реакции, схематически представленной как (2.7),
кинетическое уравнение которой имеет вид (2.8), частный порядок, например,
по реагенту A есть стехиометрический коэффициент
A
n этого реагента в урав-
нении реакции, а общий порядок реакции равен
ABD
nn n n
=
++. (2.13)
Общий порядок простой реакции не превышает трех. При этом различают
реакции
первого, второго и третьего порядков.
Обобщенно простые реакции или элементарные стадии сложных реакций
различного порядка и их кинетические уравнения можно представить следую-
щим образом:
реакции первого порядка
A Продукты→
1n
=
kc
=
v
(2.14)
реакции второго порядка
AB Продукты+→
2A Продукты→
2n
=
(
)
A
сс
=
AB
kc c
=
v
2
kc
=
v
(2.15)
(2.16)
реакции третьего порядка
ABD Продукты++→
2A B Продукты+→
3A Продукты→
3n
=
(
)
A
cc
=
ABD
kc c c
=
v
2
AB
kc c=v
3
kc
=
v
(2.17)
(2.18)
(2.19)
1
Для гетерогенных реакций (см. 2.2.1.1) частные порядки по жидким и твердым реагентам
равны нулю.

Х и м и ч е с к а я к и н е т и к а
17
При равенстве числовых значений частного и общего порядка реакции, имею-
щем место для кинетических уравнений (2.14), (2.16), (2.19), необходимость
уточнять, о каком порядке реакции идет речь, отпадает.
Кинетические закономерности, определяемые порядком реакции, относят
к формальной кинетике, так как порядок реакции является понятием формаль-
ным. Закономерности формальной кинетики для уяснения механизма реакции
теряют смысл, если
механизм реакции, суждение о котором сформулировано по
порядку реакции, не соответствует экспериментальным данным.
Закон действующих масс, несмотря на то, что на практике очень мало
строго доказанных простых реакций, сохраняет свое важное значение и часто
его называют
постулатом химической кинетики для простых реакций. Это
обусловлено, с одной стороны, тем, что знание хотя бы наиболее вероятного
механизма протекания сложной реакции позволяет применить закон дейст-
вующих масс к каждой элементарной стадии, а с другой стороны, – примени-
мостью этого закона к некоторым сложным реакциям, например к реакции, от-
вечающей уравнению (2.11), подчиняющейся закону действующих масс для ре-
акций второго порядка.
Закон действующих масс выполняется при определенных условиях, кото-
рые для простой реакции заключаются в следующем [2].
1. При протекании реакции не нарушается максвелл-больцмановское рас-
пределение энергии по степеням свободы реагирующих частиц. Это условие
выполняется при достаточно медленном протекании химической реакции по
сравнению с физическими процессами обмена
энергий (поступательной, коле-
бательной, вращательной) от частицы к частице. Нарушение этого распределе-
ния отражается на кинетике реакции, примером чего служит рассматриваемый
далее случай мономолекулярной реакции, имеющей второй порядок.
2. Изменение концентраций реагентов заметно не меняет свойств среды и
физического состояния реагентов, что в жидкой фазе обычно выполняется
только для сильно разбавленных
растворов.
3. Химическая реакция осуществляется только за счет тепловой энергии.
Если реакцию вызывают свет, электрический ток и т. д., то скорость реакции
зависит от этих факторов, а закон действующих масс видоизменяется.
При моделировании химико-технологических процессов используют по-
нятие
формально простых реакций. В узком смысле это сложные реакции,
состоящие из последовательности элементарных стадий с неустойчивыми
промежуточными продуктами, что позволяет формально рассматривать ее

В. Е. Коган, Г. С. Зенин, Н. В. Пенкина
18
(последовательность) как одну стадию. В определенном интервале изменения
концентраций реагентов для таких реакций часто оправдывается степенная за-
висимость скорости реакции от концентраций реагентов, но с показателями
степеней, отличными от значений соответствующих стехиометрических коэф-
фициентов.
В широком смысле любые сложные реакции, для которых ки-
нетическое уравнение в требуемом интервале изменения концентраций
реагентов может быть получено на опыте приближенно в виде степенной
зависимости скорости реакции от концентраций реагентов, относят к фор-
мально простым.
Реакцию, схематически представленную в виде (2.7), для данного кон-
кретного момента времени можно записать как
ABDПродукты
x
yz++→ (2.20)
Кинетическое уравнение в таком случае принимает вид
ABD
x
yz
kc c c=v (2.21)
и называется
кинетическим уравнением в алгебраической форме. Данное
уравнение показывает [10], что
скорость реакции в каждый момент времени
пропорциональна произведению наличных, возведенных в некоторые сте-
пени, концентраций реагентов
(основной закон кинетики). В уравнении
(2.21)
x
, y , z – порядки реакции по реагентам A, B, D, т. е. показатели сте-
пени, в которые нужно возвести концентрации соответствующих реагентов,
чтобы получить экспериментально наблюдаемую скорость реакции
1
.
Вопросы, связанные с кинетикой протекания сложных химических реак-
ций, подробно будут рассмотрены в последующем изложении. Здесь же для
полноты освещения вопроса кинетической классификации химических реакций
отметим лишь следующее.
При кинетическом изучении сложных реакций применяют
принцип неза-
висимости
, являющийся по сути дела одним из постулатов химической кине-
тики:
если в системе протекает несколько реакций, то каждая из них под-
1
В случае обратимой реакции, схематически представленной как
AB CD
AB CD,nn nn++
кинетическое уравнение в алгебраической форме для прямой реакции имеет вид
AB
y
x
kcc
+ +
=v
(общий порядок реакции
nxy=+), а для обратной реакции –
11
D
C
x
y
kc c
−−
=v (общий порядок
реакции
11
nx y=+). В данных уравнениях
+
≡
vv
и
kk
+
≡
– скорость и константа скорости
прямой реакции, а
−
≡vv
и kk
−
≡
соответственно эти же величины для обратной реакции.

Х и м и ч е с к а я к и н е т и к а
19
чиняется основному закону и протекает независимо от других реакций.
Полное изменение системы представляет сумму этих независимых изменений.
Исходя из сказанного, одной из возможных общих форм написания кине-
тического уравнения сложных реакций является приводимое в [1] выражение
3
12
123
n
nn
kc c c=v , (2.22)
где
1
n ,
2
n ,
3
n , в отличие от
A
n ,
B
n ,
D
n в уравнении (2.8), есть порядки реакции
по промежуточным продуктам
1
A
,
2
A
,
3
A
. При этом для правильного толкова-
ния уравнения (2.22) необходимо пояснить два момента, которые, к сожалению,
не отмечаются авторами учебника [1]. Во-первых, концентрации промежуточ-
ных продуктов могут быть выражены через концентрации реагентов. Во-
вторых, величина
k в уравнении (2.22), в отличие от константы скорости k в ки-
нетическом уравнении (2.8) для простой химической реакции, уравнение кото-
рой (2.7), представляет собой эффективную величину, являющуюся сложным
комплексом констант скоростей элементарных стадий реакции.
Исходя из уравнения (2.22), общий порядок сложной реакции равен
123
nn n n
=
++. (2.23)
Для сложных реакций порядок реакции может быть равен нулю, положи-
тельному целому и дробному числу, а частный порядок может принимать и от-
рицательные значения. С общим порядком выше третьего практически не при-
ходится встречаться [10], хотя известны реакции с порядком больше четырех
[5].
В реакциях нулевого порядка скорость не зависит от
концентрации реа-
гентов, т. е. остается постоянной в течение всей реакции. Кинетическое уравне-
ние реакции нулевого порядка имеет вид
0
kc
=
v , или k
=
v . (2.24)
Нулевой порядок характерен, в частности, для реакций, идущих по цепному
механизму (см. 2.2.1.7).
Одной из причин наличия дробных порядков может быть тот факт, что
при получении одного и того же продукта реакция идет по нескольким путям. В
результате этого порядок реакции является усредненным значением, отражаю-
щим вклад каждого из этих путей
в общее выражение для скорости реакции.
Примером может служить протекающая в газовой фазе реакция, уравнение ко-
торой
