Тетра Пак. Технология производства молока
Подождите немного. Документ загружается.

Кислотный раствор с pH ниже 7.
pH = 7 – нейтральный раствор
pH < 7 – кислотный раствор
Щелочной раствор с pH выше 7.
Нейтральный раствор с pH 7.
Нейтрализация
При смешивании кислоты со щелочью гидроксидные ионы реагируют с ионами гидроксония с
образованием воды. Если смешать кислоту и щелочь в определенной пропорции, можно получить нейтральную
смесь без избытка ионов гидроксония или гидроксидных ионов, которая имеет pH 7. Этот процесс называется
нейтрализацией, а химическая формула Н
3
О
+
+ ОН
–
преобразуется в Н
2
О + Н
2
О
Нейтрализация приводит к образованию соли. Когда соляную кислоту (HCl) смешивают с гидроксидом
натрия, она при реакции с ним образует хлористый натрий (NaCl) и воду (Н
2
О). Соли соляной кислоты
называются хлоридами, а другие соли называются подобным же образом на основании тех кислот, из которых
они образованы: лимонная кислота образует цитраты, азотная – нитраты и так далее.
Диффузия
Частички, присутствующие в растворах (ионы, молекулы или коллоидные частицы), испытывают
воздействие сил, под влиянием которых они мигрируют (диффундируют) с участков с высокой концентрацией
на участки с низкой концентрацией. Процесс диффузии протекает до тех пор, пока весь раствор не станет
однородным с одной и той же концентрацией во всем своем объеме. Растворение сахара в чашке кофе является
примером диффузии.
Сахар быстро растворяется в горячем напитке, и его молекулы диффундируют до однородногоих
распределения.
Скорость диффузии определяется скоростью перемещения частиц, которая, в свою очередь, зависит от
температуры, размера частиц и разности концентраций в разных частях раствора.
Применяемая U-образная трубка разделена на 2 половины проницаемой мембраной. Левую половину
трубки заполняют водой, а правую раствором сахара, молекулы которого проходят через мембрану. Через
некоторое время благодаря диффузии концентрация сахара выравнивается по обе стороны мембраны.
Осмос
Термин “осмос” применяют для описания спонтанного течения чистой воды в водный раствор или из
менее концентрированного раствора в раствор с большей концентрацией при разделении этих растворов
подходящей мембраной.
Явление осмоса. U-образная трубка разделена на 2 половины полупроницаемой мембраной. Левая
половина трубки заполнена водой, а правая – раствором сахара, молекулы которого не могут пройти через
мембрану. В этом случае молекулы воды будут диффундировать через мембрану в раствор сахара и разбавлять
его. Этот процесс и называют осмосом.
Объем раствора сахара при разбавлении растет. Уровень сахарного раствора в правой части трубки
повышается, а гидростатическое давление «а» раствора на мембрану становится больше, чем давление воды с
другой ее стороны. В этом неравновесном состоянии вода начинает диффундировать обратно, в
противоположном направлении, под влиянием более высокого гидростатического давления в растворе. Когда
диффузия воды в обоих направлениях выравнивается, система приходит в состояние равновесия.
Если же гидростатическое давление изначально приложить к раствору сахара, прохождение воды через
мембрану может быть уменьшено. Гидростатическое давление, необходимое для предотвращения выравнивания
концентрации за счет диффузии воды в раствор сахара, называют осмотическим давлением этого раствора.
Обратный осмос
При приложении к раствору сахара давления, превышающего осмотическое давление, молекулы воды
смогутдиффундировать из раствора в воду, вызывая повышение концентрации раствора.
Этот процесс, применяется в промышленности для повышения концентрации растворов и называется
обратным осмосом.
Диализ
Диализ является процессом применения разности концентраций в качестве движущей силы для
разделения в растворе крупных и небольших частиц – например белков и солей. Обрабатываемый раствор
помещают по одну сторону мембраны, а растворитель (воду) – по другую. Мембрана имеет поры с диаметром,

допускающим прохождение через нее небольших молекул соли, но препятствующим прохождению крупных
молекул белка.
Скорость диффузии зависит от разности концентраций, так что диализ можно ускорить частой заменой
растворителя по другую сторону мембраны.
Состав коровьего молока
Содержание различных составных компонентов молока может сильно различаться у разных особей
коров, как разных пород, так и одной и той же породы. Поэтому могут быть приведены лишь пределы, в
которых может изменяться содержание этих компонентов. Цифры в таблице 2.3 приведены только в качестве
примера. При обсуждении состава молока помимо общего сухого остатка применяют и термин “твердые
вещества без жира”. Он означает обезжиренный общий сухой остаток. Средняя величина этого показателя,
согласно таблице 2.3, составляет 13,0–3,9 (9,1%). У обычного молока величина pH лежит между 6,5 и 6,7 при
наиболее типичном значении 6,6 (измеряется при температуре около 25С).
Молочный жир
Молоко и сливки являются примерами эмульсий “жир (масло) в воде”. Молочный жир существует в
виде небольших шариков или капель, диспергированных в молочной плазме. Их диаметр составляет 0,1–20 мкм
(1 мкм = 0,001 мм). Средний их размер равен 3–4 мкм, и они присутствуют в количестве порядка 15 млрд в 1 мл.
Данные эмульсии стабилизированы наличием очень тонкой оболочки толщиной 5–10 нм (1 нм = 10
–9
м),
окружающей шарики и имеющей сложный состав.
Молочный жир состоит из триглицеридов (в качестве доминирующих компонентов), ди- и
моноглицеридов, жирных кислот, стероидов, каротиноидов (обусловливающих желтый цвет жира),
жирорастворимых витаминов (A, D, E и К) и других компонентов, являющихся второстепенными и
присутствующих в незначительном количестве.
Оболочка состоит из фосфолипидов, липопротеинов, цереброзидов, белков, нуклеиновых кислот,
ферментов, элементов в следах (металлов) и связанной воды.
Необходимо отметить, что состав и толщина оболочки не являются постоянными, так как ее
компоненты находятся в постоянном обмене с окружающей молочной плазмой.
Так как шарики молочного жира являются не только самыми крупными частицами, но и самыми
легкими (с плотностью 0,93 г/см
3
при 15,5С), они имеют тенденцию всплывать к поверхности, если молоку дать
в течение некоторого времени отстояться.
Скорость подъема жировых шариков подчиняется закону Стокса, но их маленькие размеры замедляют
процесс выделения сливок.
Однако этот процесс может быть ускорен вследствие агрегации жировых шариков посредством белка,
называемого агглютинином. Эти агломераты поднимаются значительно быстрее, чем отдельные шарики, и
легко разрушаются нагреванием или механической обработкой. Агглютинин денатурируется за 10 минут при
65С или за 2 минуты при 75С.
Химическая структура молочного жира
В свежевыдоенном молоке при температуре 37С молочный жир находится в жидком состоянии. Это
означает, что шарики жира легко изменяют форму при умеренном механическом воздействии (например, при
подаче молока насосом или при протекании его по трубопроводам) без разрушения их оболочек.
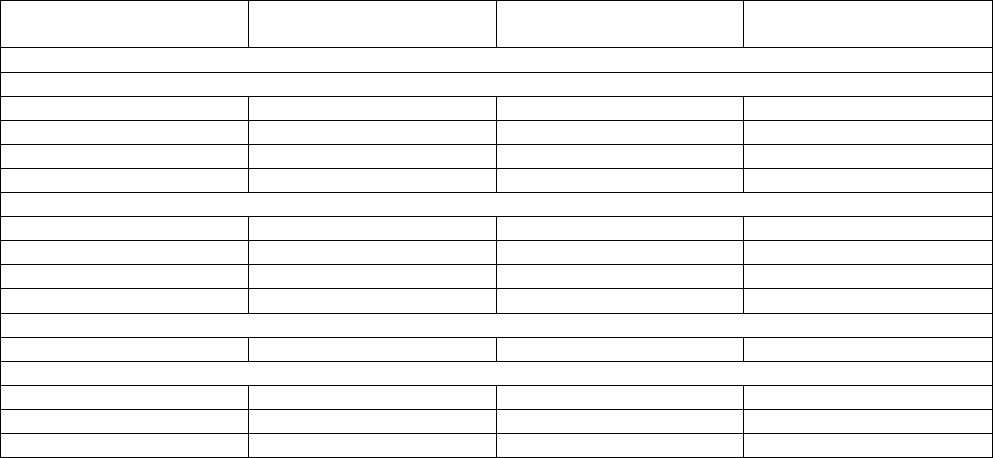
Таблица 2.3
Количественный состав молока
Основные компоненты Пределы изменений величин Средняя величина
Вода 85,5 – 89,5 87,5
Cухой молочный остаток 10,5 – 14,5 13,0
Жир 2,5 – 6,0 3,9
Белки 2,9 – 5,0 3,4
Лактоза 3,6 – 5,5 4,8
Минеральные вещества 0,6 – 0,9 0,8
Все жиры относятся к группе веществ, называемых сложными эфирами, являющимися соединениями
спиртов и кислот. Молочный жир является смесью разных эфиров жирных кислот, называемых
триглицеридами, которые состоят из спирта, называемого глицерином, и различных жирных кислот,
составляющих до 90% молочного жира. Молекулы жирных кислот состоят из углеводородной цепи и
карбоксильной группы и имеют формулу RCOOH. В насыщенных жирных кислотах углеродные атомы
соединены вместе в цепь простыми связями, в то время как в ненасыщенных жирных кислотах в
углеводородной цепи присутствуют и двойные связи. Каждая молекула глицерина может присоединять три
молекулы жирной кислоты, а присоединенные кислоты не обязательно являются одинаковыми, что приводит к
очень большому разнообразию глицеридов в молочном жире.
В таблице 2.4 приведены наиболее важные жирные кислоты триглицеридов молочного жира.
Этот жир характеризуется относительно высоким содержанием масляной и капроновой кислот.
Таблица 2.4 показывает, что наибольшее процентное содержание в молочном жире соответствует
миристиновой, пальмитиновой, стеариновой и олеиновой кислотам. Первые три из них являются твердыми, а
последняя жидкой при комнатной температуре. Как показывают приведенные данные,
относительноесодержание различных жирных кислот может значительно изменяться. Это изменение может
влиять на твердость жира. При этом жир с высоким содержанием высокоплавких кислот, таких как
пальмитиновая, будет твердым. С другой стороны, жир с высоким содержанием низкоплавкой олеиновой
кислоты определяет мягкость приготовляемого масла.
Определение относительного количества отдельных жирных кислот само по себе является предметом
чисто научного интереса. Для практических же целей достаточно определение одного или нескольких констант
или индексов, обеспечивающих определенную информацию об относительном составе жира.
Таблица 2.4
Основные жирные кислоты молочного жира
Кислоты
Общее %-ное содержание
жирных кислот
Температура
плавления,°С
Число атомов H С О
Насыщенные
Жидкие при комнатной температуре
Масляная 3,0 – 4,5 –7,9 8 4 2
Капроновая 1,3 - 2,2 –1,5 12 6 2
Каприловая 0,8 – 2,5 +16,5 16 8 2
Каприновая 1,8 –3,8 +31,4 20 10 2
Твердые при комнатной температуре
Лауриновая 2,0 – 5,0 +43,6 21 12 2
Миристиновая 7,0 – 11,0 +53,8 28 14 2
Пальмитиновая 25,0 – 29,0 +62,6 32 16 2
Стеариновая 7,0 – 3,0 +69,3 36 18 2
Ненасыщенные
Олеиновая 30,0 – 40,0 +14,0 34 18 2
Жидкие при комнатной температуре
Линолевая 2,0 – 3,0 –5,0 32 18 2
Линоленовая до 1,0 –5,0 30 18 2
Арахидоновая до 1,0 –49,5 32 20 2
Йодное число
Жирные кислоты с одним и тем же числом атомов С и Н, но с различным числом простых и двойных
связей имеют совершенно различные характеристики. Наиболее важным и наиболее часто применяемым
методом индикации специфических характеристик этих кислот является измерение йодного числа (IV) жира.
Йодное число указывает на процент йода, который может связать жир. Йод присоединяется по двойным
связям ненасыщенных жирных кислот. Так как одной из самых распространенных из ненасыщенных жирных
кислот является жидкая при комнатной температуре олеиновая кислота, то йодное число, а тем самым и
мягкость жира, в значительной мере характеризует содержание этой кислоты.
Йодное число жировой фракции масла обычно лежит в пределах 24–46. Такой разброс его значения
зависит от вида корма коров. Зеленый подножный корм летом вызывает повышение содержания олеиновой
кислоты, так что летний молочный жир является мягким (с высоким йодным числом). Некоторые кормовые
концентраты, такие как жмых подсолнечника или льняных семян, тоже способствуют получению мягкого жира,
в то время как такие типы корма, как жмых кокосовых орехов или пальмового масла или ботва корнеплодов,
дают твердый жир. Поэтому подбором подходящей диеты для коров можно влиять на консистенцию молочного
жира. Масло с оптимальной консистенцией должно иметь йодное число в пределах 32–37.
Показатель преломления
Содержание различных жирных кислот в животном жире влияет и на то, как он преломляет свет.
Поэтому получила распространение практика определения показателя преломления жира, который может быть
использован для расчета йодного числа. Это является быстрым способом оценки твердости жира. Показатель
преломления жира обычно меняется в пределах 40–46.
Ядерный магнитный резонанс (ЯМР)
Вместо использования значений йодного числа или показателя преломления количественное отношение
насыщенного жира к ненасыщенному можно определить при помощи импульсного ЯМР. При желании
полученные данные по ЯМР можно при помощи соответствующего коэффициента преобразовать в величины
йодного числа.
Метод с применением ЯМР может быть также использован и для определения кинетики степени
кристаллизации жира. Опыты, проведенные в лаборатории SMR в Мальмё (Швеция) в 1979–1981 гг.,
показывают, что кристаллизация в 40%-ных сливках, охлажденных с 60°С до 5°С, протекает длительное время.
Отмечается также, что в течение 2 минут после достижения 5С закристаллизовывалось только 15–20%
жира. Показания ЯМР по содержанию жировой фракции в масле обычно изменяются в пределах 30–41%.
Жир с высоким содержанием высокоплавких жирных кислот является твердым.
Жир с высоким содержанием низкоплавких жирных кислотявляется мягким.
Кристаллизация жира
Во время кристаллизации жировые шарики являются очень чувствительными и легко разрушаются
даже при умеренных механических воздействиях.
Исследования, проведенные с помощью электронного микроскопа, показали, что жир кристаллизуется в
мономолекулярные сферы. В это же время происходит фракционирование жира, приводящее к образованию
внешних сфер из триглицеридов с самой высокой температурой плавления. Из-за того, что кристаллический
жир имеет более низкий удельный объем, чем жидкий жир, внутри шариков жира при кристаллизации
возникают напряжения, которые придают им нестабильность и предрасположенность к распаду.
Это приводит к выделению жидкого жира в молочную плазму с образованием комочков агломератов, в
которых свободный жир склеивает распавшиеся жировые шарики вместе (такое же явление происходит и при
получении масла). Кристаллизация жира идет с выделением теплоты плавления, повышающей в некоторой
степени его температуру (40%-ные сливки, охлажденные с 60 до 7–8°С, в период кристаллизации становятся
теплее на 3–4°С). Это важное свойство молочного жира необходимо учитывать при получении сливок
различного применения.
Молочные белки
Белки являются существенной частью нашего рациона. Потребляемые нами белки распадаются на
более простые соединения в пищеварительной системе и в печени. Эти соединения транспортируются к клеткам
организма, где они используются в качестве строительного материала для собственных белков организма. В
огромном большинстве химические реакции, происходящие в организме, регулируются активными белками,
называемыми ферментами.
Белки – это гигантские молекулы, состоящие из меньших единиц – аминокислот. Белковая молекула
состоит из одной или нескольких цепей с внутренними связями между аминокислотами, расположенными в
специфическом порядке. Белковая молекула обычно содержит около 100–200 соединенных аминокислот, хотя
известны белки как с большим, так и с меньшим числом аминокислот.
Аминокислоты
Аминокислоты являются строительными блоками, образующими белки, и характеризуются
одновременным присутствием в их молекулах по одной аминогруппе (NH
2
) и по одной карбоксильной (СООН)
группе. Белки образуются из специфических аминокислот – α-аминокислот, то есть таких, у которых
карбоксильная группа и аминогруппа присоединены к одному и тому же углеродному атому – α-углероду.
Аминокислоты принадлежат к группе химических соединений, которые могут выделять ионы гидроксония в
щелочных растворах и присоединять эти ионы в растворах кислот. Такие соединения называются амфотерными
электролитами, или амфолитами. Эти аминокислоты могут существовать в трех состояниях:
1 Отрицательно заряженными в щелочных растворах
2 Нейтральными при равных количествах положительных и отрицательных зарядов
3 Положительно заряженными в кислотных растворах.
Белки конструируются приблизительно из 20 аминокислот, 18 из которых найдены в белках молока.
Важным фактом с точки зрения питания является то, что восемь (для детей девять) из 20 аминокислот
не могут быть синтезированы человеческим организмом. Так как они являются необходимыми для поддержания
соответствующих процессов обмена веществ, то непременно должны поступать в организм вместе с пищей. Они
называются незаменимыми аминокислотами и как раз все присутствуют в белках молока.
Тип и порядок аминокислот в белковой молекуле определяют природу белка. Любое изменение в типе
аминокислот или в местах их расположения в молекулярной белковой цепи вызывает соответствующие
изменения в свойствах белков. Так как число возможных комбинаций 18 аминокислот в цепи, содержащей 100–
200 аминокислот, почти неограниченно, то и число белков с различными свойствами неограниченно в такой же
степени. Характерной чертой аминокислот является то, что они содержат аминогруппу (–NH
2
) со слабыми
основными свойствами и карбоксильную группу (–СООН) со слабыми кислотными свойствами. Эти группы
присоединены к боковой цепи (R).
R– органический радикал, присоединенный к центральному углеродному атому.
Если боковая цепь полярна, свойство притяжения воды основной и кислотной группами, в дополнение
к полярной боковой цепочке, будет преобладать, то есть вся аминокислота в этом случае будет притягивать воду
и легко растворяться в ней.
Такую аминокислоту называют гидрофильной (водолюбивой).
С другой стороны, если боковая цепь является углеводородной и не содержит гидрофильных радикалов,
то будут доминировать свойства этой цепи. Длинная углеводородная цепь отталкивает воду и делает
аминокислоту менее растворимой или менее совместимой с водой. Такая аминокислота называется
гидрофобной (водоотталкивающей).
При наличии в углеводородной цепи некоторых радикалов, таких как гидроксильные (–ОН) или
аминогруппы (–NH
2
), ее гидрофобные свойства могут быть изменены в сторону повышения гидрофильности.
Если гидрофобные аминокислоты превалируют в одной части белковой молекулы, эта ее часть будет обладать
гидрофобными свойствами. Совокупность гидрофильных аминокислот в другой части данной молекулы будет
по аналогии придавать ей гидрофильные свойства. Поэтому белковая молекула может быть гидрофильной,
гидрофобной, промежуточной или же локально гидрофильной или гидрофобной.
Некоторые белки молока демонстрируют очень большую разницу внутри молекулы в отношении
совместимости с водой, что сильно влияет на некоторые очень важные свойства этих белков.
Гидроксильные группы в аминокислотных цепях у казеина могут быть эстерифицированы фосфорной
кислотой. Такие группы придают способность казеину связывать ионы кальция или коллоидный
гидроксифосфат кальция с образованием прочных мостиковых связей внутри белковых молекул или между
ними.
Электрическое состояние белков молока
Боковые цепи некоторых аминокислот белков молока несут электрический заряд, зависимый от pH
молока. Когда pH изменяется при добавлении кислоты или основания, изменяется также и распределение заряда
белка. При обычной pH молока, равном 6,6, белковая молекула имеет общий отрицательный заряд. Молекулы
белка остаются разделенными из-за отталкивания идентичных зарядов.
При добавлении ионов водорода они адсорбируются белковыми молекулами. При величине pH, при
которой положительный заряд белка становится равен отрицательному заряду (когда число групп NH
3
+
и СОО
–
в боковых цепях одинаково), общий заряд белка будет нулевым. Белковые молекулы больше не отталкиваются
друг от друга, а положительные заряды одной молекулы притягиваются отрицательными зарядами соседних
молекул, что приводит к образованию огромных белковых скоплений с последующим выпадением белка из
раствора. Величина pH, при которой происходит это явление, называется изоэлектрической точкой данного
белка.
При наличии избытка водородных ионов белковые молекулы приобретают общий положительный
заряд. Это снова приводит к взаимному отталкиванию белковых молекул, что позволяет оставаться им в
растворе. С другой стороны, при добавлении раствора сильной щелочи (NaOH) все белки приобретают
отрицательные заряды, остаются в растворенном состоянии.
Классификация белков молока
Молоко содержит сотни видов белков, большинство из которых присутствует в очень незначительных
количествах. Белки можно классифицировать разными способами на основе их химических или физических
свойств и биологических функций. Старый способ разделения белков на казеины, альбумины и глобулины дает
путь к более адекватной системе их классификации. В таблице 2.5 приведен сокращенный список белков молока
в соответствии с современной системой. Незначительные группы белков при этом для простоты исключены.
Понятие “сывороточный белок” часто используют в качестве синонима для белков молочной плазмы, но его
нужно было бы зарезервировать для белков сыворотки, получаемой в процессе приготовления сыра. В
добавление к белкам молочной сыворотки сывороточный белок содержит и фрагменты молекул казеина.
Некоторые белки присутствуют в меньшей концентрации, чем в исходном молоке. Это обусловлено
тепловой денатурацией при пастеризации молока в процессе производства сыра. Три основные группы белков в
молоке значительно различаются между собой характеристиками и свойствами. Казеины могут легко
осаждаться в молоке различными способами, в то время как белки сыворотки обычно остаются в растворе.
Белки оболочки жировых шариков, как и положено им по названию, прилипают к поверхности этих шариков и
выделяются только при механическом воздействии – например, при сбивании сливок в масло.
Казеин
Казеин является групповым названием преобладающего класса белков молока. Казеины легко образуют
полимеры, содержащие несколько идентичных или разных типов молекул. Благодаря большому количеству в
молекуле казеина ионизируемых групп, а также гидрофильных и гидрофобных участков полимерные молекулы,
образованные казеинами, являются очень специфичными. Эти полимеры построены из сотен и тысяч отдельных
молекул и образуют коллоидный раствор, придающий обезжиренному молоку его характерный беловато-
голубой оттенок.
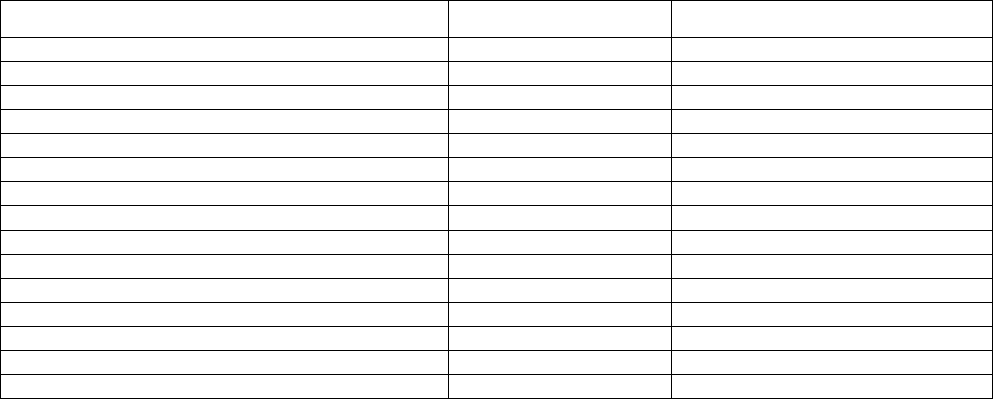
Таблица 2.5
Концентрация белков в молоке
Концентрация в молоке, г/кг Вес % от общего содержания белка
Казеин
s
1
-казеин*) 10,0 30,6
s
2
-казеин*) 2,0 8,0
-казеин**) 10,1 30,8
-казеин 3,3 10,1
Общее содержание казеина 26,0 79,5
Сывороточные белки
-лактальбумин 1,2 3,7
-лактоглобулин 3,2 9,8
альбумин сыворотки крови 0,4 1,2
иммуноглобулины 0,7 2,1
прочие (включая протеозо-пептонную фракцию) 0,8 2,4
Общее содержание сывороточных белков 6,3 19,3
Белки оболочки жировых шариков 0,4 1,2
Общее содержание белка 32,7 100
*) далее именуемые s-казеин
**) включая -казеин
Эти молекулярные комплексы известны в качестве мицелл казеина. Величина этих мицелл может
достигать 0,4 мкм, и они могут быть видны только под электронным микроскопом.
Мицеллы казеина
Три подгруппы казеина – s-казеин, _____-казеин и -казеин – все являются гетерогенными и состоят
из 2–8 генетических вариантов, которые отличаются друг от друга только несколькими аминокислотами.
Общим для этих подгрупп является то, что у них одна из двух аминокислот, содержащих гидроксигруппы,
эстерифицирована фосфорной кислотой, присоединяющей кальций и магний и некоторые комплексные соли с
образованием внутримолекулярных или межмолекулярных связей.
Мицеллы казеина, состоят из комплекса субмицелл с диаметром 10–15 нм (нанометр = 10
–9
м).
Содержание -, - и -казеиновых фракций неодинаково распределено в различных мицеллах. Кальциевые
соли s и -казеин почти нерастворимы в воде, а -казеин легко растворим.
Благодаря доминирующей локализации последнего из казеинов на поверхности мицелл растворимость
его кальциевой соли превалирует над нерастворимостью двух других казеинов, содержащихся в мицеллах, и
потому вся мицелла в целом растворима с образованием коллоидного раствора. (Современные данные о химии
молока. Том 1. Белки. П.Ф.Фокс – Advanced dairy chemistry. Vol.1 Proteins. P.F. Fox).
Согласно Роллема (Rollema) (1992), комбинация моделей Слаттери и Эвард (Slattery & Evard) (1973),
Шмидт (Schmidt) (1982) и Валстра (Walstra) (1990) дает наилучшее из имеющихся объяснений того, каким
образом образуются и стабилизируются мицеллы.
Фосфат кальция и гидрофобное взаимодействие между субмицеллами приводят к объединению
казеиновых мицелл. Гидрофильные С-концевые части -казеина, содержащие углеводную группу, выступают
снаружи комплексных мицелл, придавая им “волосистый” вид и, что важно, стабилизируют их. Основой этому
является сильный отрицательный заряд углеводов.
Размер мицелл зависит в большой степени от содержания ионов кальция (Са++). Если эти ионы
покидают мицеллу – например, при диализе, то она распадается на субмицеллы. Мицелла среднего размера
состоит приблизительно из 400–500 субмицелл, которые объединяются, как описано выше.
При расщеплении С-окончания -казеина на поверхности мицелл – например, под действием
сычужного фермента – мицеллы теряют растворимость и начинают агрегировать с образованием казеинового
сгустка.
В неповрежденных мицеллах имеется избыток отрицательных зарядов, и потому они взаимно
отталкиваются. Молекулы воды, удерживаемые гидрофильными участками -казеина, являются важной частью
этого равновесия. При удалении этих гидрофильных участков вода начинает покидать структуру, что является
сигналом к началу действия сил притяжения. Образуются новые связи – например, солевого типа с активным
кальцием и гидрофобного типа.
Образование связи приводит к вытеснению воды, и вся структура в конце концов осаждается с
образованием плотного сгустка.
Низкая температура отрицательно воздействует на мицеллы, вызывая диссоциацию цепей -казеина и
удаление гидроксифосфата кальция из их структуры, в которой он присутствует в коллоидном виде, в раствор.
Объяснение этого явления состоит в том, что -казеин является наиболее гидрофобной фракцией
казеина, и что гидрофобные взаимодействия ослабляются при понижении температуры. Эти изменения делают
молоко
Примечание: При большом избытке кислоты, добавляемой к коагуляту, казеин будет растворяться с
образованием соли и кислоты.
При применении соляной кислоты раствор будет содержать гидрохлорид казеина, частично
диссоциированный на ионы.
-казеин, кроме того, после выхода из мицеллы легче подвергается гидролизу различными протеазами,
содержащимися в молоке. Его гидролиз до -казеина и протеозопептонной фракции приводит к более низкому
выходу получаемого сыра из-за того, что протеозопептонные фракции отходят в сыворотку. Распад -казеина
может также привести к образованию пептидов, вызывающих горечь и таким образомприводящих к ухудшению
вкусовых качеств сыра.
В этом контексте необходимо упомянуть, что когда сырое или пастеризованное и хранившееся в холоде
молоко нагревают в течение 20 секунд до 62–65С, то -казеин и гидроксифосфат кальция возвращаются в
мицеллы, вызывая при этом полное или частичное восстановление исходных свойств молока.
Осаждение казеина
Способность казеина к осаждению является одним из характерных его свойств.
Из-за сложной природы молекул казеина и образующихся из них мицелл это осаждение может быть
вызвано многими различными агентами. Необходимо помнить о том, что существует большая разница между
оптимальными условиями осаждения для казеина в мицеллярной и немицеллярной форме – например, в виде
казеината натрия. Последующее описание относится в основном к осаждению мицеллярного казеина.
Осаждение кислотой
При введении кислоты в молоко или при росте в нем бактерий, продуцирующих кислоту, происходит
понижение pH молока. При этом происходит двухстадийное изменение среды, окружающей мицеллы. Прежде
всего коллоидный гидроксифосфат кальция, присутствующий в мицеллах казеина, растворяется с образованием
ионов кальция, проникающих в структуру мицелл, и создает прочные внутренние кальциевые связи. Затем pH
раствора достигает изоэлектрических точек отдельных видов казеина.
Оба эти процесса инициируют изменения внутри мицелл, начиная с их роста через агрегацию и
заканчивая более или менее плотным коагулятом.
В зависимости конечной величины pH коагулят будет являться солью казеина и/или казеином в его
изоэлектрическом состоянии.
Величина изоэлектрических точек компонентов казеина зависит от наличия других ионов,
присутствующих в растворе. Теоретические величины pH для этих точек, при определенных условиях
совпадающие с реальными его значениями, составляют 5,1–5,3. В солевых растворах при условиях,схожих с
теми, которые характерны для молока, интервал кислотности для оптимального осаждения составляет pH 3,9–
4,5, а практическая его величина для осаждения казеина в молоке равна 4,7.
При большом избытке гидроксида натрия, вводимого в осажденный казеин, вновь растворенный казеин
будет превращаться в казеинат натрия, частично диссоциируемый на ионы. Кисломолочные продукты имеют
обычно pH в пределах 3,9–4,5, лежащий в кислой области интервала изоэлектрических точек. При получении
казеина из обезжиренного молока добавлением серной или соляной кислоты часто выбирают pH 4,6.
Осаждение ферментами
Аминокислотная цепь, образующая -казеин, состоит из 169 аминокислот. В этой цепи связь между
аминокислотными остатками в положениях 105 (фенилаланин) и 106 (метионин) легко доступна для многих
протеолитических ферментов. Некоторые из них атакуют эту связь и расщепляют полипептидную цепь.
Образующийся концевой аминосодержащий фрагмент содержит аминокислоты между 106-м и 169-м
положениями, среди которых преобладают полярные аминокислоты, а также углевод, придающий этой
последовательности гидрофильные свойства. Эта часть молекулы -казеина, называемая гликомакропептидом,
выделяется в сыворотку при изготовлении сыра. Остальная часть -казеина, состоящая из аминокислот между
1-м и 105-м положениями, нерастворима и остается в сгустке вместе с s- и фракциями казеина. Эту часть
называют пара--казеином. Раньше считали, что весь сгусток состоит из пара-казеина.
Образование сгустка обусловлено внезапным удалением гидрофильных макропептидов и наступающей
при этом неравновесностью внутримолекулярных сил. Это приводит к развитию и усилению связи между
гидрофобными участками цепи за счет кальциевых связей, образующихся, когда молекулы воды, содержащиеся
в мицеллах, начинают покидать структуру. Данный процесс обычно называют стадией коагуляции и
синерезисом. Расщепление связи 105–106 в молекуле -казеина часто называют первичной стадией действия
сычужного фермента, а стадию коагуляции и синерезиса – второй стадией процесса. Имеется также третья
стадия этого процесса, при которой сычужный фермент воздействуетна компоненты казеина более обычным
путем. Это происходит при созревании сыра.
Продолжительность всех трех стадий определяется главным образом значением pH и температурой.
Кроме того, вторая стадия сильно зависит от концентрации ионов кальция и от присутствия или отсутствия
сывороточных белков молока на поверхности мицелл.
Сывороточные белки
Сывороточными белками обычно называют белки молочной сыворотки.
При удалении казеина из обезжиренного молока каким-либо методом осаждения (таким, как
добавление неорганической кислоты) в жидкости остается группа белков, которые и называют белками
молочной сыворотки. До тех пор пока они не будут подвергнуты денатурации нагреванием, они не осаждаются
при их изоэлектрических точках. Однако они обычно осаждаются полиэлектролитами, такими как
карбоксиметилцеллюлоза. Технически для выделения сывороточных белков часто используют подобные
вещества или комбинацию нагревания и регулирования pH. При нагревании молока некоторые сывороточные
белки денатурируют и образуют комплексы с казеином, понижая способность казеина подвергаться
воздействию сычужного фермента и присоединять кальций. Сгусток из молока, прошедшего
высокотемпературную обработку, не выделяет сыворотку, как это происходит обычно с сырным сгустком, из-за
меньшего в этом случае числа связей в виде мостиков внутри молекул казеина и между ними. Сывороточные
белки вообще и -лактальбумин, в частности, имеют очень высокую питательную ценность. Их
аминокислотный состав очень близок к тому, что считается биологическим оптимумом. Производные
сывороточных белков широко применяются в пищевой промышленности.
-лактальбумин
Этот белок можно считать типичным сывороточным белком. Он присутствует в молоке всех
млекопитающих и играет важную роль в синтезе лактозы в вымени.
Сывороточными белками являются:
-лактальбумин
-лактоглобулин
Имеются два способа вызвать флокуляцию и коагуляцию частиц казеината: осаждение их кислотой и
осаждение ферментами.
-лактоглобулин
Этот белок найден только у копытных животных и является основным компонентом молока коров.
При нагревании молока выше 60С начинается его денатурация, в которой реакционная способность
серосодержащей аминокислоты -лактоглобулина играет заметную роль.
Сера начинает образовывать связи в виде мостиков между молекулами -лактоглобулина, между -
лактоглобулином и -казеином и между -лактоглобулином и -лактальбумином.
При высоких температурах во время этого процесса начинают постепенно выделяться такие соединения
серы, как сероводород. Эти соединения вызывают появление привкуса “кипяченого молока”.
Иммуноглобулины и родственные побочные белки
Эта группа белков чрезвычайно неоднородна, причем детально изучено лишь малое число ее
представителей. В будущем из молочной сыворотки, возможно, будут выделены в промышленных масштабах
многие полезные вещества. Лактоферрин и лактопероксидаза являются веществами, которые потенциально
могут найти применение в фармацевтической и пищевой промышленности и в настоящее время выделяются из
сыворотки. Способ выделения этих веществ разработан в Мальмё (Швеция) д-ром Х.Барлингом (H. Burling) с
сотрудниками отдела научных исследований Шведской молочной ассоциации.
Белки оболочек жировых шариков
Белки оболочек – это группа белков, которые образуют защитный слой вокруг шариков жира для
стабилизации его эмульсии. Их консистенция лежит в пределах от мягкой и желеобразной для некоторых из них
и до довольно плотной и твердой для других. Некоторые из этих белков содержат липидные остатки и
называются липопротеинами. Их липиды и гидрофобные аминокислоты направляют гидрофобные участки
своих молекул к жировой поверхности, в то время как участки этих молекул с меньшей гидрофобностью
ориентированы в направлении воды.
Тем же путем воздействуют на соответствующие белковые слои и белки оболочек, обладающие слабой
гидрофобностью, образуя градиент гидрофобности от поверхности жира к воде.
Градиент гидрофобности в такой оболочке делает ее идеальным местом для адсорбции молекул со
всеми степенями гидрофобности. В частности, в структуре оболочки адсорбируются фосфолипидыи
липолитические ферменты. Никакие реакции между ферментами и их субстратом не идут до тех пор, пока не
будет нарушена структура оболочки, но как только это происходит, ферменты получают доступ к субстрату и
начинают реагировать.
Примером таких реакций является липолитическое высвобождение жирных кислот, когда холодное
молоко прокачивается неисправным насосом или после гомогенизации холодного сырого молока, без
последующей его пастеризации.
Жирные кислоты и некоторые другие продукты этой ферментной реакции придают получаемому
продукту прогорклый привкус.
Денатурированные белки
До тех пор пока белки существуют в окружающей среде при значениях температуры и pH, толерантных
для этих белков, они сохраняют свои биологические функции. Но при нагревании выше некоторой
максимальной температуры их структура будет изменяться. Как говорят, они денатурируются. То же самое
происходит, когда белки обрабатываются кислотами или основаниями, подвергаются облучению или
интенсивному перемешиванию. Денатурированные белки теряют исходную растворимость.
При денатурации белков исчезает их биологическая активность. Ферменты-белки, являющиеся
катализаторами некоторых биохимических реакций, теряют способность ускорять реакции в результате
процесса денатурации. Причина этого состоит в том, что нарушаются определенные связи в их молекулах,
вызывая изменение структуры белка. После слабого денатурирования белки могут иногда возвратиться в свое
исходное состояние с восстановлением их прежних биологических функций.
Однако во многих случаях денатурация является необратимой. Например, белки сваренного яйца не
могут быть возвращены в исходное состояние.
Молоко – буферный раствор
Молоко содержит огромное число веществ, которые могут действовать либо как слабые кислоты, либо
как слабые основания – например, такие как молочная, лимонная и фосфорная кислоты и их соответствующие
соли – лактаты, цитраты и фосфаты. В химии подобная система называется буферным раствором, потому что в
некоторых пределах при добавлении кислот или оснований кислотность (pH) в ней остается постоянной. Это
явление может быть объяснено специфическими свойствами белков.
При подкислении молока вводят огромное количество водородных ионов (Н
+
). Эти ионы
присоединяются к аминогруппам в боковых цепях аминокислот с образованием ионов NH
3+
. При этом, однако,
величина pH из-за очень незначительного повышения концентрации свободных водородных ионов почти совсем
не меняется.
При введении в молоко основания ионы (Н
+
) выделяются из карбоксильных групп СООН боковых
цепей с образованием ионов СОО
–
. Поэтому величина pH и в этом случае остается более или менее постоянной.
Чем больше основания вводится, тем большее число водородных ионов выделяется.
Другие компоненты молока также обладают этой способностью связывать или выделять ионы, и
потому величина pH при добавлении кислот или оснований изменяется очень медленно.
Почти вся способность молока к буферизации исчерпывается, если оно уже является кислым из-за
длительного хранения при высоких температурах.
В этом случае для изменения pH достаточно добавления небольшого количества кислоты.
Ферменты, присутствующие в молоке
Ферменты являются белками, продуцируемыми живыми организмами.
Они способны инициировать химические реакции и влиять на ход и скорость этих реакций. Ферменты
катализируют реакции, при этом не изменяя своего количества. Поэтому иногда их называют
биокатализаторами.
Действие ферментов является специфичным: каждый тип ферментов катализирует только один
определенный тип реакций. Два фактора сильно влияют на ферментные реакции – температура и pH.
Как правило, ферменты наиболее активны при оптимальной температуре в интервале 25–50 С. Их
активность падает при выходе температуры за верхний предел этого интервала, исчезая где-то в интервале 50–
120С. При этих температурах ферменты практически полностью денатурируются (инактивируются).
Температура инактивации изменяется от одного типа фермента к другому – явление, которое широко
используют для определения степени пастеризации молока. Ферменты имеют оптимальный интервал значений
pH: некоторые из них лучше всего функционируют в кислых растворах, а другие – в щелочных. Ферменты,
присутствующие в молоке, попадают в него или из коров, или от бактерий. Первые из них являются
нормальными компонентами молока и называются нативными ферментами. Вторые, бактериальные ферменты,
различаются по типу и распространенности в соответствии с природой и величиной бактериальной популяции.
Ряд ферментов молока используется для тестирования его качества и контроля. Наиболее важными из этих
ферментов являются пероксидаза, каталаза, фосфатаза и липаза.
Пероксидаза
Пероксидаза переносит кислород от пероксида водорода (Н
2
О
2
) к другим легко окисляемым веществам.
Этот фермент инактивируется в молоке нагреванием до 80С в течение нескольких секунд. Этот факт может
быть использован для установления наличия или отсутствия пероксидазы в молоке, и таким образом – для
проверки того, была ли температура пастеризации молока выше 80С.
Этот тест называют пробой Сторча (Storch) на пероксидазу.
Каталаза
Каталаза расщепляет пероксид водорода на воду и свободный кислород. Количественным
определением кислорода, выделяемого этим ферментом, можно определить содержание каталазы в молоке и
узнать: получено это молоко от животного со здоровым выменем или нет?
Молоко животного с больным выменем содержит большое количество каталазы, в то время как в
молоке из здорового вымени наблюдается только незначительное количество каталазы. Однако существует
большое количество бактерий, продуцирующих данный фермент. Каталаза разрушается при тепловой
обработке, протекающей при температуре 75С в течение 60 секунд.
Фосфатаза
Фосфатаза обладает свойством расщеплять некоторые эфиры фосфорной кислоты до этой кислоты и
соответствующего спирта. Присутствие фосфатазы в молоке может быть обнаружено добавлением эфира
фосфорной кислоты и реагента, изменяющего окраску в результате взаимодействия с высвобождающимся
спиртом. Изменение окраски свидетельствует о том, что молоко содержит фосфатазу. Этот фермент
разрушается при обычной пастеризации (температура 72С, выдержка 15–20 секунд), таким образом тест на
фосфатазу может быть использован для определения, был ли выдержан данный режим пастеризации. Этот
рутинный тест, применяемый в молочном деле, называется тестом Шарера (Scharer) на фосфатазу. Этот тест
предпочтительно проводить сразу же после нагревания. В противном случае молоко должно быть охлаждено
ниже 5С и выдерживаться при этой температуре до проведения анализа, который должен быть проведен в тот
же день. В противном случае может происходить процесс реактивации, при котором инактивированный
фермент снова становится активным и дает положительный результат на тест. Этому, в частности, наиболее
подвержены сливки.
Липаза
Липаза расщепляет жир на глицерин и свободные жирные кислоты. Избыток этих кислот в молоке или
молочных продуктах приводит к появлению прогорклого привкуса. Действие этого фермента, по-видимому, в
большинстве случаев является очень слабым, хотя молоко от некоторых коров может обладать сильной
липазной активностью. Считается, что количество липазы в молоке увеличивается к концу лактационного
периода. Липаза в значительной степени инактивируется пастеризацией, но для полной ее инактивации
требуются более высокие температурные режимы. Липазу продуцируют многие микроорганизмы. Это может
вызывать серьезные проблемы, так как этот фермент является термостабильным.
Лактоза
Лактоза – является сахаром, находящимся только в молоке, и принадлежит к группе химических
соединений, называемых углеводами.
Углеводы являются наиболее важным источником энергии в нашей пище. Хлеб и картофель, например,
обогащены углеводами и представляют собой питательный резервуар. Углеводы распадаются на соединения,
обладающие высокой энергетической ценностью. Данные соединения участвуют в биохимических реакциях,
обеспечивая их протекание необходимой энергией. Углеводы также поставляют материал для синтеза
некоторых важных химических соединений в организме. Они присутствуют в мышцах в качестве мышечного
гликогена и в печени – в качестве гликогена печени.
