Жариков В.А. Основы физической геохимии
Подождите немного. Документ загружается.

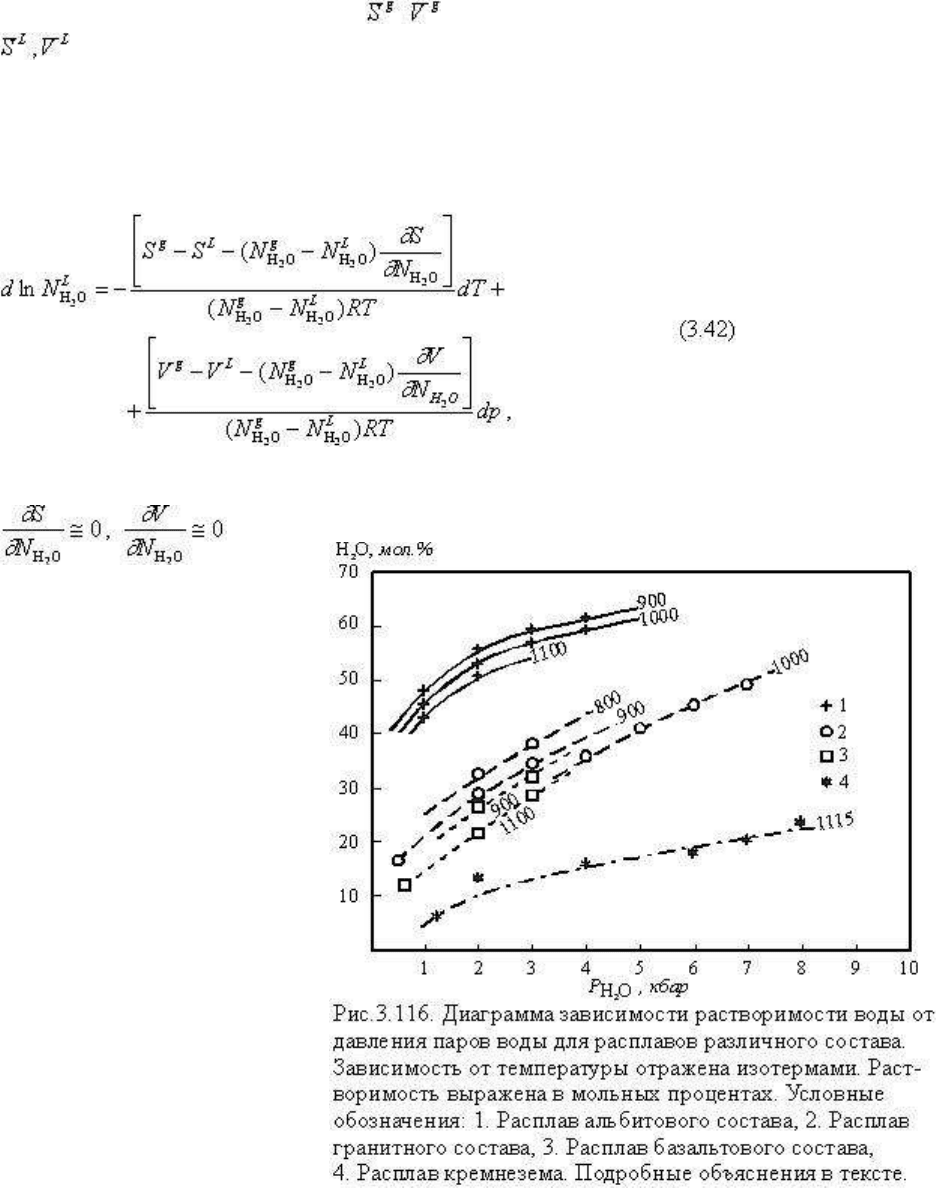
где N - содержание воды в расплаве в мольных или весовых единицах, соответственно в
мольных или объемных единицах - энтропия и объем воды в газовом состоянии,
-энтропия и объем воды в расплаве. dG
ex
= - d ln γ
L
H2O
- отклонение поведения воды
от идеального, которое обычно невелико и им в первом приближении можно пренебречь.
Как было показано выше, растворимость компонента в сосуществующем растворе
(расплаве) более строго определяется условием Ван-дер-Ваальса:
которое при
легко
приводится к (3.41), а в случае
значимости этих величин
преобразуется к виду с
линейной зависимостью S и V
от N
H2O
.
Согласно условиям (3.41) и
(3.42) растворимость воды
уменьшается с увеличением
температуры (так как S
g
H2O
>
S
L
H2O
) и возрастает с
увеличением давления p
H2O
(поскольку V
g
H2O
> V
L
H2O
). Это
справедливо для области
обычных магматических
температур и не сверхвысоких
давлений (для расплавов
одного и того же фазового
состава). В качестве примера на
рис.3.116 приведена диаграмма
зависимости растворимости от
давления и температуры для
расплавов альбитового,
гранитного и базальтового состава, а также для расплава кремнезема. Диаграмма в
координатах N (мольные проценты H
2
O) - p
H2O
, влияние температуры показано
изотермами. Диаграмма построена по экспериментальным данным Р. Горансона, Н.
Хитарова, А. Кадика, О. Татла, В. Бернема, Дж. Кеннеди и др. Растворимость выражена в
мольных процентах от одного моля вода + альбит, вода + гранит и т.д., на которые
пересчитаны экспериментальные данные.
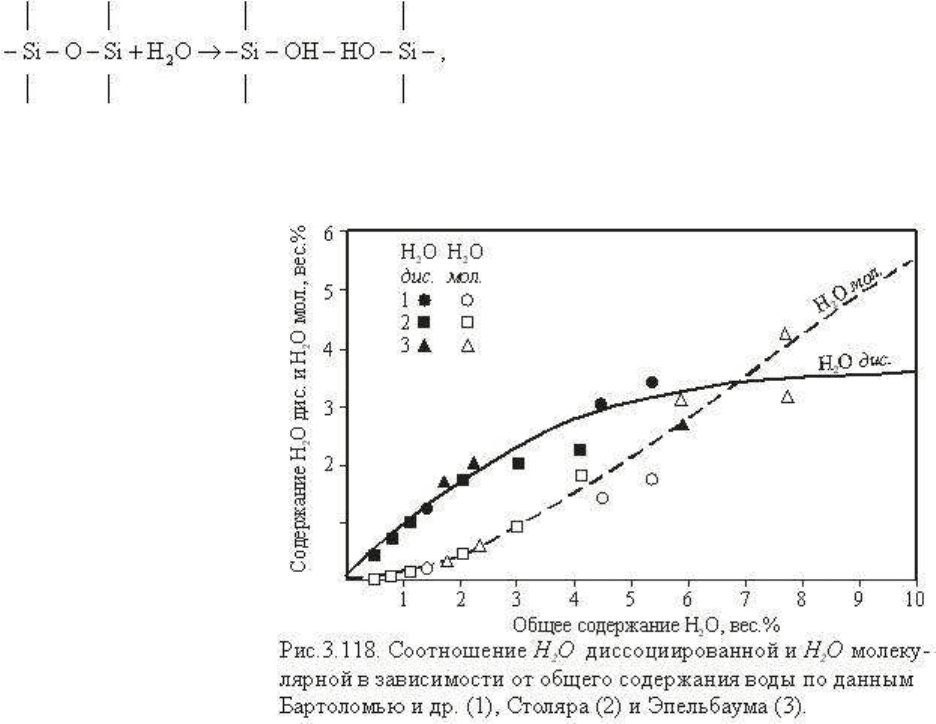
Кроме очевидной зависимости растворимости воды от давления и температуры,
диаграмма 3.116 отчетливо выражает также явную зависимость растворимости воды от
состава расплава. Это обусловлено разной структурной позицией воды в расплавах
различного состава.
Растворение воды в силикатном расплаве сопровождается ее диссоциацией. Возможны и
осуществляются различные схемы диссоциации:
(I) H
2
O → 2H
+
+ O
-2
(II) H
2
O → H
+
+ OH
-
(III) H
2
O + O
-2
→ 2OH
-
(3.43)
Схема диссоциации зависит от состава расплава. Растворение в расплаве воды с
диссоциацией нередко называют "химическим" растворением воды.
В расплав кремнезема молекула воды входит, разрушая связи кремнекислородного
каркаса, таким образом, что связь Si-O-Si преобразуется в две связи Si-OH по схеме
которая показана на рис.3.117, А. Это вызывает деполимеризацию и уменьшение
кислотности расплава.
Высокая прочность связей
Si-O (см рис. 3.99)
обусловливает весьма
ограниченную
растворимость воды в
расплаве кремнезема.
В расплавах, содержащих
кроме кремнекислородных
тетраэдров различные
катионные группы
(например, Me -
двухвалентные катионы),
вода занимает иное
структурное положение.
Молекулы воды
разрывают связи Me-O,
заменяя ее связями Me-OH
и Si-OH. На рис. 3.116, В это показано в левой части структурной схемы на примере
расплава ортопироксена. Прочность связи Me-O значительно меньше кремнекислородной
связи (см. рис. 3.99), поэтому растворимость воды в основных расплавах существенно
выше, чем в расплавах кремнезема. Тем более, что при дальнейшем повышении p
H2O
происходит полный отрыв Me от кремнекислородной цепочки с образованием свободных
групп Me(OH)
2
в различной степени диссоциированных. Такая ситуация показана в
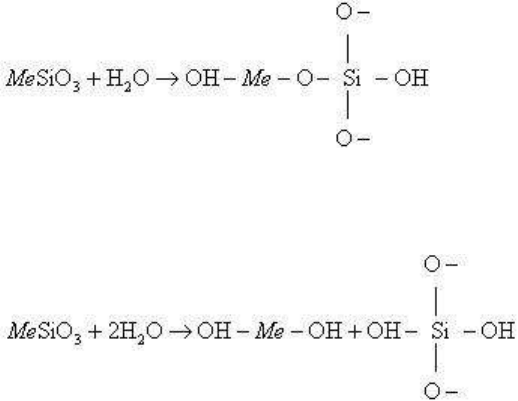
правой части рис. 3.117, В. Отмеченные соотношения можно записать в виде
схематических структурных реакций:
первоначально
и при больших давлениях воды
Особенно существенно для петрогенетических целей поведение воды в алюмосиликатных
расплавах, где катионы представлены щелочными металлами (R). Растворяясь в таких
расплавах молекула воды, диссоциируя, отщепляет ион водорода, который вытесняет
щелочной металл в связи R-O, занимая его положение в "дальней" структуре. Щелочной
металл оказывается ассоциированным с гидроксильной группой и располагается в
свободном объеме расплава. Это показано на рис.3.117, С и может быть представлено
схемой: [-O-R] + [ H
+
+ OH
-
] → [-O-H] + [ R
+
+ OH
-
], или, конкретно, на примере альбита:
[Na - AlSi
3
O
8
] + [ H
+
+ OH
-
] → [H - AlSi
3
O
8
] + [Na
+
+ OH
-
].
Как показывают приведенные нами расчеты (они частично отражены на рис.3.99),
замещение катионов щелочных металлов ионами водорода оказывается наиболее
энергетически благоприятным из всех возможных реакций растворения воды в
силикатном расплаве. Оказывается, что связи H-O порядка 10-19 ккал/г
.
атом (в
зависимости от координационного числа, см. рис.3.99) существенно выше, чем связи K-O,
Na-O, равные 4-8 ккал/ г
.
атом или того же порядка, как связи Li-O, Ca-O, Mg-O, Fe-O,
равные 13-19 ккал/ г
.
атом , и существенно ниже, чем энергия связей Al-O, Si-O, Zr-O, (45-
90 ккал/ г
.
атом ). Поэтому наиболее благоприятными (экзотермическое растворение) для
замещения водородом оказываются связи щелочной металл - кислород, благоприятными -
связи Ca-O, Mg-O, Fe-O и т.д., и менее благоприятными (эндотермическое растворение) -
связи катионов с высоким ионным потенциалом: Si-O, Zr-O, Ti-O, Al-O.
В соответствии с изложенным находятся экспериментальные данные о зависимости
растворимости воды от состава расплава, особенно от содержания щелочей, от
электропроводности и других физических свойств расплава. Это подтверждают малые
мольные объемы воды в расплавах, экзотермические реакции растворения, данные
инфракрасной спектроскопии и протонного ядерного магнитного резонанса расплавных
стекол. Соответствующие материалы читатель найдет в специальной литературе.
Кроме диссоциированной воды в силикатных расплавах присутствует и молекулярная
вода, особенно при высоких давлениях воды ("физическое" растворение воды). Формы
нахождения молекулярной воды недостаточно исследованы. Молекулярная вода может
образовывать гидратные оболочки ионов или входит в состав водных комплексов, но, в
основном, она присутствует в виде изолированных или непрерывных молекулярных

групп, вызывающих микрорасслоение расплава. В условиях высоких давлений водная
фаза в отношении главных характеристик (плотность, растворимость, диссоциация и т.д.)
ведет себя как жидкость и, находясь в равновесии с расплавом, растворяет часть его
компонентов. При этом водный раствор остается молекулярной жидкостью и обладает
меньшим поверхностным натяжением по сравнению с ионным расплавом (Есин, Гельд,
1966). Для удержания водного раствора в расплаве требуется повышенное давление p
H2O
.
Понижение внешнего давления, например, при подъеме магм и повышение внутреннего
давления, например при кристаллизации расплава, вызывает отделение водных растворов
от расплава. Водные растворы обладают высокой подвижностью в расплавах,
обусловливая многие важные особенности водных силикатных расплавов, в том числе
вполне подвижное поведение воды и щелочей. Подчеркивая это, Д.С. Коржинский назвал
эти магматические растворы "трансмагматическими". Вполне подвижное поведение
щелочей имеет очень важное значение для гранитоидных расплавов, обусловливая
разнообразие парагенетических типов гранитоидов и различную последовательность
кристаллизации минералов в них. В дальнейшем мы рассмотрим это подробно.
Относительное количество диссоциированной и молекулярной воды в расплавах зависит
от давления воды, повышение p
H2O
вызывает увеличение относительной доли
молекулярной воды. Абсолютные количества оценить можно лишь приблизительно в
связи с многоминеральностью магматических расплавов и различными формами
растворения. Например, для лейкократового гранитоидного расплава количество
химически растворенной воды с замещением всех R
+
на H
+
отвечает растворимости 3,8-
4,2 вес.% H
2
O. Общая растворимость H
2
O в лейкократовом расплаве на ликвидусе при 2,0
кбар порядка 6,0-6,4. Это значит, что 1,8-2,6 вес. % воды приходится на молекулярную
воду и другие формы химического растворения (замещение Al-O, Si-O и т.д.). При 3 кбар
общая растворимость на ликвидусе порядка 7,2-7,5 и на молекулярную воду (и другие
формы химического растворения) приходится уже 3,3-3,7 вес.% H
2
O. Неоднократно
производились попытки определить соотношения диссоциированной и молекулярной
воды по ИК-спектрам закаленных силикатных стекол. Результаты некоторых опытов
приведены на рис.3.118. Эти данные тоже ориентировочны (при заполнении стекол
вероятен переход H
2
O дисс → H
2
O мол), но подтверждают общую тенденцию увеличения
молекулярной H
2
O при увеличении p
H2O
и общего содержания воды.
Обратим внимание на следующее. Краевые зависимости температуры плавления
минералов и горных пород от давления паров воды имеют характерный вид: сначала
следует резкое понижение температуры плавления, затем, при p
H2O
=2-3 кбар, кривая
выполаживается и далее продолжается в область высоких p
H2O
(до 10-12 кбар) с
небольшим отрицательным наклоном. Такое поведение кривых плавления, несомненно,
связано с характером растворения воды: химическое растворение, нарушающее
квазикристаллическое строение расплавов и изменение их структуры приводит к
существенному понижению температуры кристаллизации минералов и их плавления. При
высоких p
H2O
роль химического растворения уменьшается, соответственно
выполаживается кривая плавления. Молекулярная вода существенно влияет на
физические свойства расплавов (вязкость и т.д.), мало влияет на температуры плавления
минералов и горных пород.
Влияние на кристаллизацию расплавов окислительно-восстановительных условий.
Принципиальная зависимость температур плавления минералов от химического
потенциала электрона (редокс-потенциала) или от химического потенциала кислорода
может быть выражена следующими соотношениями (вывод см. в гл. 2):
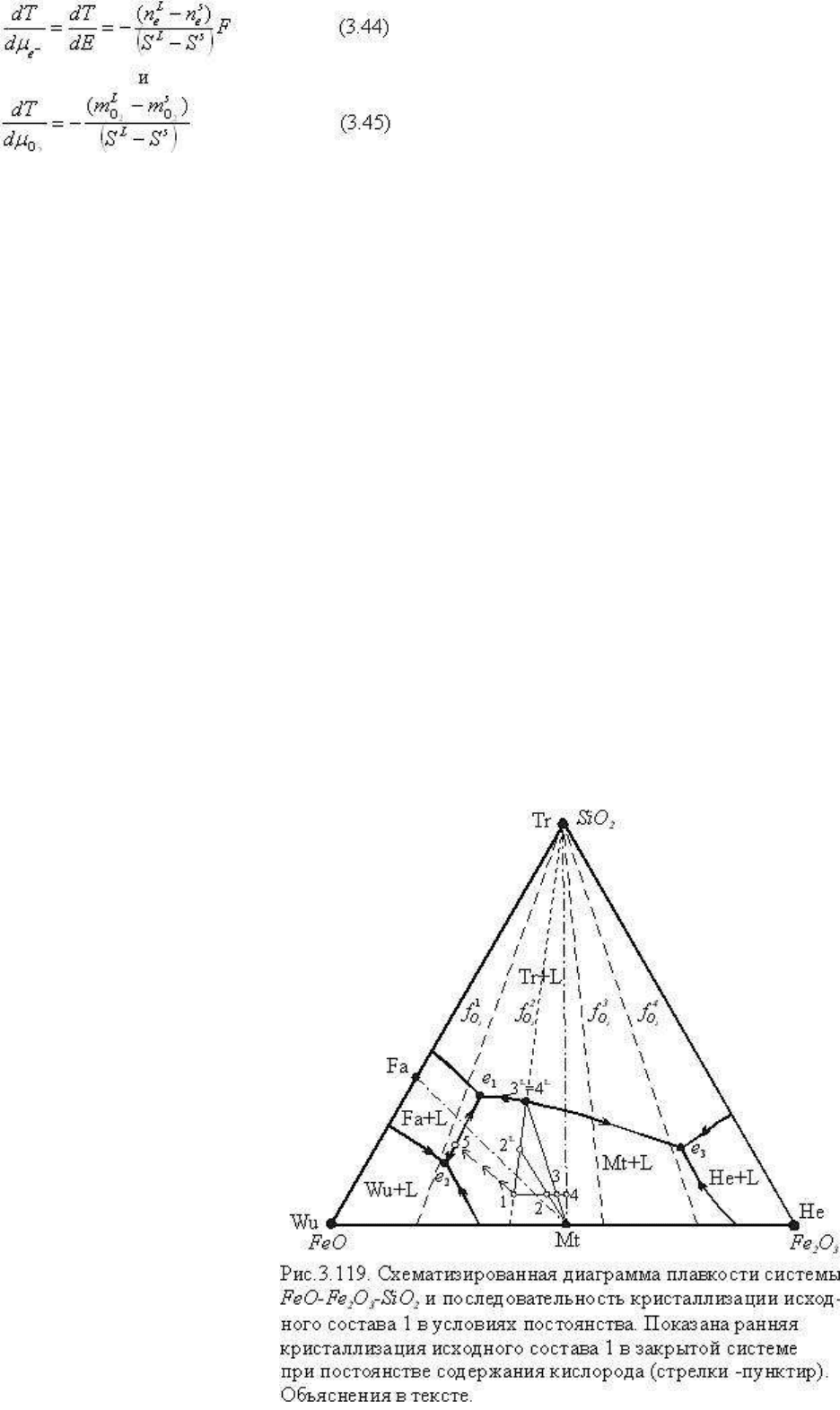
где n
e
L
, n
e
S
- количества электронов в расплаве и в твердой фазе; F - заряд электрона
(число Фарадея); E - восстановительный (редокс) потенциал; m
O2
L
, m
O2
S
-содержание
кислорода в расплаве и в твердой фазе; S
L
, S
S
- энтропия расплава и твердой фазы. Эти
уравнения, полученные путем перекрестного дифференцирования соответствующего
уравнения изобаро-изоэнтропического потенциала, показывают, что повышение редокс-
потенциала будет повышать температуры плавления тех минералов, которые
представляют более восстановленные формы, чем расплав, и, наоборот, понижать
температуры плавления минералов, содержащих больше окисленных форм компонентов,
чем расплав. Повышение окислительного потенциала или химического потенциала
кислорода будет вызывать противоположное действие.
В результате изменение окислительно-восстановительных условий приведет к изменению
температур плавления, полей и последовательности кристаллизации минералов для
расплавов, содержащих элементы переменной валентности в жидкой и твердой фазах. В
природных расплавах главным таким элементом является железо, и окислительно-
восстановительный режим оказывается особенно существенным для основных и других
богатых железом магм.
Рассмотренные зависимости справедливы для вполне подвижного поведения кислорода,
или (что то же) независимых, извне заданных, окислительно-восстановительных условий.
Отметим, что порядок кристаллизации на диаграммах плавкости для систем, содержащих
компоненты переменной валентности и вполне подвижный кислород, отличается от всех
рассмотренных выше примеров. Главные отличия состоят в том, что состав системы
оказывается непостоянным: при вполне подвижном поведении кислорода и заданном
извне его химическом потенциале в процессе кристаллизации происходит изменение
содержания кислорода в
системе и смещение
положения фигуративной
точки исходного состава.
Кроме того, для определения
путей кристаллизации на
диаграмме необходимо
обозначить
изопотенциальные линии,
фиксирующие изменение
состава системы при
постоянстве химического
потенциала кислорода.
В качестве примера
рассмотрим схему
кристаллизации в системе
FeO-Fe
2
O
3
-SiO
2
,
представленную на рис.3.119,
где показаны поля
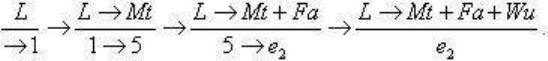
кристаллизации тридимита (Tr), фаялита (Fa), вюстита (Wu), магнетита (Mt), гематита
(He). Oбласть расслоения в системе для упрощения опущена. Пунктиром нанесены линии
постоянной фугитивности кислорода (ƒ
O2
= ƒ
O2
1
, ƒ
O2
2
, ƒ
O2
3
, ƒ
O2
4
). Рассмотрим особенности
кристаллизации в этой системе в условиях, когда кислород является вполне подвижным
компонентом и фугитивность его поддерживается постоянной в течение всего периода
кристаллизации. Пусть исходный состав в момент начала кристаллизации обозначится
точкой 1 и фугитивность кислорода равна ƒ
O2
2
. При температуре, отвечающей точке 1, из
расплава начнет кристаллизоваться магнетит. Состав расплава должен изменяться по
линии постоянной фугитивности кислорода (1
L
→ 2
L
→ 3
L
), а общий состав системы будет
обогащаться привнесенным в систему кислородом, поскольку выделившийся магнетит
содержит кислорода больше, чем исходный расплав 1 при данной летучести кислорода
(ƒ
O2
2
). Отношение Si/Fe в системе остается постоянным, и линия изменения общего
состава системы расположиться параллельно стороне FeO-Fe
2
O
3
(линия 1 → 2 → 3 → 4).
Для какого-либо промежуточного состояния , например обозначенного точкой 2: 2
L
-
состав расплава , 2 - общий состав системы, Fe
3
O
4
- состав кристаллизующейся фазы, - все
точки по правилу слагаемости составов расположены на одной прямой. При достижении
расплавом котектической кривой (точка 3
L
) из расплава вместе с магнетитом начнет
кристаллизоваться тридимит. Состав расплава будет оставаться постоянным, поскольку
он удерживается в точке 3
L
постоянной фугитивностью кислорода, а общий состав
системы будет обогащаться привнесенным кислородом, который необходим для
образования магнетита, изменяясь по линии 3 → 4.
Кристаллизация закончится исчерпанием расплава, состав которого будет оставаться
неизменным при совместной кристаллизации Tr + Mt (3
L
= 4
L
). Общий состав
закристаллизовавшейся системы будет отвечать точке 4, лежащей на конноде SiO
2
-Fe
3
O
4
.
Обычным сопоставлением отрезков можно определить количество фаз для любого
промежуточного состояния системы. Нетрудно также убедиться, что рассмотренная
кристаллизация в системе FeO-Fe
2
O
3
-SiO
2
при вполне подвижном поведении кислорода
представляла, по существу, кристаллизацию в бинарной системе Si-Fe при данной
постоянной фугитивности кислорода.
Для сравнения на рис. 3.119 показана пунктирными стрелками кристаллизация исходного
состава 1 в закрытой системе FeO-Fe
2
O
3
-SiO
2
, при постоянном содержании кислорода.
Кристаллизация проходит по принципу простой эвтектики:
Сравнив эвтектические составы, легко убедиться, что при ƒ
O2
= const эвтектический состав
(3
L
) двухфазовый и существенно обогащен кремнеземом. При постоянном содержании
кремнезема эвтектический состав (e
2
) трехфазовый, содержит заметно меньше кремнезема
и обогащен FeO.
Различный режим кислорода имеет существенное значение для понимания генезиса
базальтовых серий. Например, Е. Осборн на основании анализа системы FeO-Fe
2
O
3
-SiO
2
выделяет две серии: а) толеитовую, образующуюся при постоянном содержании
кислорода, обогащенную железом при небольшом увеличении содержания кремнезема и
б) известково-щелочную, формирующуюся при независимом ƒ
O2
(обычно ƒ
O2
= const),
характеризующуюся значительным возрастанием содержания кремнезема. Существуют и
другие более сложные интерпретации, но важное петрологическое значение режима
кислорода признается всеми исследователями.
Обратим внимание на то, что отмеченные особенности изменения характера
кристаллизации справедливы и для любого другого случая вполне подвижного режима
какого-либо компонента. Например, для анализа фазовых соотношений в системе
KAlSi
2
O
6
-CaMgSi
2
O
6
-SiO
2
, при вполне подвижном поведении K
2
O, необходимо знать
положение на диаграмме изопотенциальных линий μ
K2O
, которые будут определять
положение фигуративных точек расплава, кристаллизующегося при каком-то μ
K2O
= const.
Состав системы в отношении содержания K
2
O будет изменяться в зависимости от μ
K2O
и
соотношения масс инертных компонентов.
Влияние кинетических и динамических факторов.
Рассмотренные выше диаграммы состояния и вытекающие из них в процессе
кристаллизации соотношения фаз основывались на соблюдении условий равновесия. Оно
осуществляется всякий раз, когда "кинетические скорости"- такие, как скорость
кристаллизации, скорость реакций взаимодействия твердых фаз и расплава, скорость
перемещения компонентов в расплаве и т. д. - намного выше, чем скорости изменения
факторов минералообразования: температуры (или энтропии), давления, химических
потенциалов вполне подвижных компонентов. Однако в природной (и
экспериментальной) обстановке равновесная кристаллизация расплавов проявляется
скорее как общая главная тенденция процесса, в ходе которого в той или иной степени, но
почти всегда, наблюдаются отклонения от состояния равновесия, обусловленные
различными кинетическими и динамическими причинами.
Подробный анализ этих причин выходит за рамки настоящей работы, а для сложных
систем он все равно будет носить самый общий качественный характер. Поэтому
ограничимся кратким схематическим обсуждением обычных форм проявления
кинетических и динамических факторов.
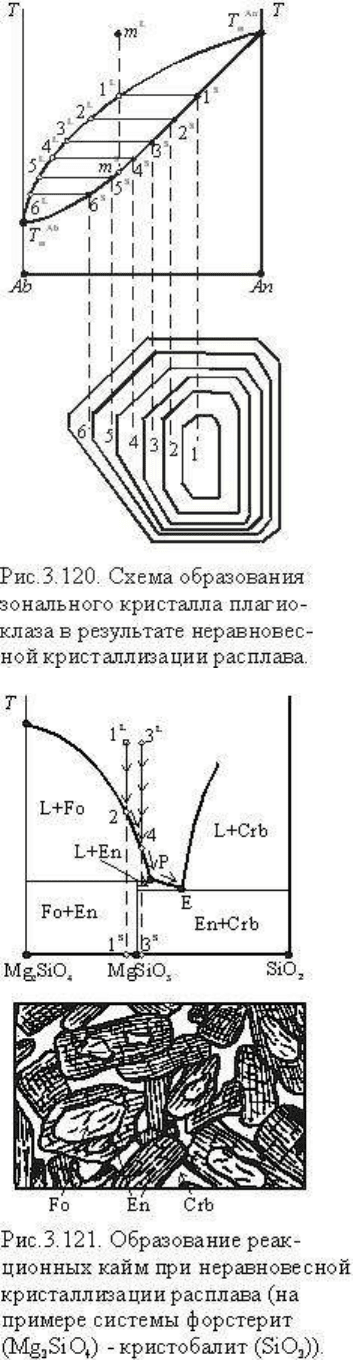
Характерным признаком неравновесной
кристаллизации являются зональные кристаллы (очень
типичны для плагиоклазов вулканических и
субвулканических пород). На рис.3.120 представлена
схема кристаллизации зонального плагиоклаза. Из
расплава состава m
L
первыми начинают
кристаллизоваться плагиоклазы состава 1
S
(75%
анортитовой молекулы). В условиях равновесной
кристаллизации эти кристаллы, реагируя с расплавом,
непрерывно изменяют свой состав до состава m
S
, когда
весь расплав будет исчерпан. При неравновесной
кристаллизации - вследствие быстрого понижения
температуры или малой скорости взаимодействия -
выделившиеся кристаллы не успевают прореагировать
с расплавом и на них нарастают грани иного состава, с
меньшим содержанием анортита 2
S
, 3
S
, 4
S
и т.д. ,
вплоть до исчерпания расплава. В таком случае
остаточный расплав и внешние зоны кристалла будут
иметь менее анортитовый состав, чем равновесный
кристалл (m
S
). Зональность может быть непрерывной и
дискретной (см. рис. 3.120), что также обусловлено
кинетикой процесса. Присутствие зональных
кристаллов с небольшим числом зон резко различного
состава свидетельствует о существенных изменениях
физико-химических условий кристаллизации.
Другим характерным признаком неравновесной
кристаллизации служат реакционные каймы
минералов. Такой пример рассмотрен на рис.3.121, где
представлена часть диаграммы форстерит (Mg
2
SiO
4
) -
кристобалит (SiO
2
). Перитектическая реакция,
происходящая в системе (при T
p
), вследствие изоляции
от расплава ранее выделившихся кристаллов Fo
каймами En, или вследствие быстрого понижения
температуры, протекает не до конца, и из расплава на
пути PE начинает кристаллизоваться En, и затем в
эвтектике En + Crb. В результате возникает в целом
неравновесная минеральная ассоциация с
характерными реакционными соотношениями
минералов. В многокомпонентных природных
магматических системах такие соотношения
проявляются многообразнее, чем рассмотренный
простенькой случай, но в принципе они подобны.
В связи с обычным проявлением неравновесной
кристаллизации изверженных горных пород,
влияющий на минеральный состав, целесообразно
уточнить понятие парагенезиса минералов
применительно к магматическим горным породам. В
общем определении парагенезис минералов - это
совокупность совместно сосуществующих,
находящихся в равновесии минералов. Тогда, применительно к магматическим
образованиям парагенезис - это совокупность совместно кристаллизующихся
минералов (т.е. находящихся в эвтектических, котектических и перитектических
соотношениях) и его следует отличать от минерального состава или минеральной
ассоциации изверженной породы.
Среди особенностей изверженных пород, обусловленных неравновесным течением
процессов, следует указать также на широкое распространение стекловатых разностей
среди вулканических пород. Быстрое понижение температуры, сопровождающее излияние
расплавов или внедрение их небольших масс в непрогретые вмещающие породы,
приводит к тому, что в расплаве не успевают возникнуть и вырасти кристаллы, и расплав
застывает в виде стекла. Образование стекол, представляющих твердые переохлажденные
метастабильные жидкообразные (по структуре) состояния, - характерная особенность
силикатных расплавов. Превращение метастабильного стекла в кристаллический агрегат -
расстеклование (девитрификация) - происходит в природной обстановке в разнообразных
условиях, отличающихся , как правило, от условий нормальной кристаллизации
расплавов, поэтому продукты кристаллизации стекол многообразны по структуре и
составу.
Кроме рассмотренных и других кинетических факторов, влияющих на состав и строение
изверженных горных пород, в их образовании существенное, а иногда и определяющее
значение имеют динамические процессы, приводящие к разделению и обособлению
жидких и кристаллизующихся расплавов. Эти процессы назвываются процессами
дифференциации. Причины, вызывающие магматическую дифференциацию,
разнообразны. Магматические массы существуют и кристаллизуются в поле градиентов
температур (T), давления (p), и потенциала гравитационного поля (θ). Эти факторы
воздействуют как на гомогенные, так и, особенно, на гетерогенные расплавы, вызывая
разделение компонентов и фаз расплава в соответствии с их термодинамическими и
физическими свойствами. Процессы разделения усугубляются естественной и
вынужденной конвекцией в расплавах, возникающей как вследствие существования в
поле градиентов T, p и θ, так и под воздействием дополнительных наложенных сил.
Процессы магматической дифференциации можно подразделить следующим образом.
I. Дифференциация в гомогенном расплаве:
а) термодиффузионная,
б) бародиффузионная,
в) гравитационная.
II. Дифференциация в гетерогенном расплаве:
а) ликвационная,
б) кристаллизационная (фракционная кристаллизация),
III. Конвективная или динамическая дифференциация:
а) собственная,
б) вынужденная,
в) флюидная.
Охарактеризуем кратко выделенные типы магматической дифференциации. Крупные
магматические массы, или камеры, располагаются в поле градиентов температуры,
давления и сил гравитации таким образом, что внутренние части магматических масс
будут находиться при более высокой температуре, а более глубокие части - под большим
давлением, при более высокой температуре и под большим влиянием силы тяжести.

Поэтому, в соответствии с термодинамическими свойствами компонентов расплава будет
происходить их перераспределение в пределах однородного (гомогенного) расплава.
Благодаря градиенту температуры будет происходить термодиффузия компонентов
(эффект Сорэ), приводящая к тому, что более нагретые части расплава будут обогащаться
компонентами, имеющими большие энтропии и энтальпии. Вследствие градиента
давления возникнет бародиффузия компонентов, которая вызовет обогащение глубоких
частей магматического тела компонентами, имеющими меньшие парциальные (удельные)
объемы. Наконец, наличие градиента гравитационного поля приведет к обогащению более
глубоких частей магматического тела компонентами, имеющими большие массы
(удельные веса или плотности). Разделению компонентов в поле градиентов T, p и θ будет
в определенной мере препятствовать обычная концентрационная или, как ее нередко
называют, химическая диффузия (хемодиффузия), порожденная разностью концентраций
компонентов, возникающей при разделении их в градиентном поле.
В результате по прошествии значительного времени в пределах магматического тела
установится стационарное распределение с разделением компонентов, т.е. произойдет
дифференциация первично однородного расплава.
Оценить количественно охарактеризованные процессы пока еще трудно: отсутствуют
экспериментальные определения необходимых кинетических характеристик
(коэффициенты термодиффузии, бародиффузии и т.д.). Однако, общую тенденцию можно
выявить, исходя из термодинамических характеристик компонентов расплава, учтя при
этом известные трудности в выборе независимых компонентов расплава (оксиды, или
кластеры, или молекулы) вследствие особенностей его внутреннего строения (см. выше),
изменяющегося в зависимости от температуры и некоторых других факторов. В табл. 3.1
приведены характеристики некоторых компонентов расплава, представленных как в виде
оксидов, так и в форме минеральных молекул. Эти характеристики показывают, что такие
компоненты, как FeO, MgO, CaO будут накапливаться в более прогретых и глубоких
частях магматических тел. Для других компонентов влияние T и p неоднозначно:
например, для K
2
O, Na
2
O - благоприятны условия более высоких температур и меньших
давлений, для SiO
2
и Al
2
O
3
наоборот - более высоких давлений и меньших температур.
Если принимать за исходные компоненты минеральные молекулы, то несомненна
тенденция обогащения более прогретых и глубинных частей магматических тел железо-
магнезиальными минералами. Однако в целом влияние термодиффузионного,
бародиффузионного и гравитационного разделения компонентов в гомогенном расплаве,
по-видимому, невелико, так как эти процессы протекают медленно (коэффициенты термо-
и бародиффузии ориентировочно на полтора - два порядка меньше, чем коэффициенты
обычной диффузии), и для их осуществления необходимы большие магматические массы,
сохраняющиеся в жидком состоянии десятки миллионов лет.
Значительно более существенны и петрологически весьма значимы процессы
дифференциации в гетерогенных расплавах. Заметные различия в плотностях и удельных
объемах жидких и твердых фаз различного состава обусловливают возможности
эффективной ликвационной и кристаллизационной дифференциации. Рассмотрим эти
явления на двух примерах.
Таблица 3.1. Некоторые характеристики компонентов расплава
Компоненты в
расплаве
S
L
1000
o
C
V
L
M
d
Компоненты в
расплаве
S
L
1000
o
C
V
L
M
d
