Смирнов М.В. Электродные потенциалы в расплавленных хлоридах
Подождите немного. Документ загружается.


'гемпературе
соответствует
определенный
скачок
дифу3ионного
потен_
йй',',
к6Ёорь:й
не
явлйется
функшией
х.9то
по3воляет
ре1пить
уравне'
ния
вь:ну>кд{енной дифу3ии
и
получить
такие
}ке вырах{ения
для
ста_
ционарн6го
дифузиойного
потенциала'
если
ввести
вместо
переменных
й'сйЁ*""'*'ффйтивн,те
значения
коэфишиентов
дифу3ии
и электро_
йр'"'л"'""и.
Б
качестве
фФктивнь[х
ну}|(но
брать
их
минимальнь1е
ве_
лйчиньп
и3 всех
во3мо}кных
вариантов
проме}куточных
составов
солевых
смесей.
8
простейтшем
случае'
когда
они
меняются
с
составом
аддитивно'
т. е.
ли!|еййо,
их
эффктивные
3начения
совпадают
со
3начениями
в том
оасплавленномсолевомэлектролите'гдеонинаимень1||ие.
'
в качес.ве
примера
приведем
расчет
дифу3ионного
потенциала
на
по_
риеюй
диафрагме
с
постояннь|й
г!8,[|иёнт0м
электрического
потенциала'
;;;;;;й;ъъ'ййс{,'е
расплавленны".
хлориды
натрия
и
калия
при.1100"
к'
йз
и*е,'щ'хся
в
лийратуре
данных
для
этой
т€мпературы-
к-оэфициен-
тй
дифу6ии
ионов
в^раёйлавах
ука3анных
солей
равны
,'10б
см2|сек:
8,8
1х{а+
((€1)
€1_
(ша€|)
с1_
(кс1)
11,8
6,5
8,4
.
9,8
9,17
}дельная
электрпроводность
расплавленного
шас1
р3в}3
3,67
|
-^а
к91
';:,й-Б;;.
';_'.^
||Ёотности
этих
солей
соответственно
1,532
и \,493
е|см$,
откуда
ш&"'-2,123'
10_2
и
:![сг:2,002
.\0-2
моль|
см3.
вд:1'984.
10_4718
(.т!о!,6)'
*
{ш'л,6)!
$
о,6
|[олагая,
что
коффициенты диф:}узии
ионов
в солевых
смесях
.}ч]а€1
_
1(€1,
заполняющих
поры
диафрагмы'
и
их
удельная
электропро'
водность
меняются
с составом
монотонно'
берем
в качестве
эффктивных
значений
соответствующих
величин
наименьт1]ее
и3
приводимь1х
вы|пе'
1огда
в,
=
0,0039
в.
(оэффишиенты
дифу3ии
боль|]]инства
ионов
в индивиду1{"^1?*
#]];
ких
хло'идах
и
их смесях
имеют
величинь[
одного
порядка
\\1)_"
см"/сек)
в
1пироких
интервалах
температур
вь}|11е точек
их
плавления.
поэтому
в
€лучае
расплавов
с
близкимй
пйотностями
упаковки
частиц'
т.
е. близ-
киьи
числами
грамм-ионов
в единице объема, дифу3ионнь|е
потенциалы
составляют
несколько
милливольт
да)ке
тогда'
когда
диафрагма
ра3де-
ляет
расплавь!
ра3ных
солей,
если'
конечно'
их
электропроводность
до_
статочно
велкка.
}(огда
коэфициенты диффузии
||лп
электропроводность
меняются
'с
составом
расплавленнь|х
солевь!х
смесей'
3апо'няющих
поры
диафраг_
мы'
не
монотонно'
а
экстремально'
3а эффктивнь|е
3начения
ну>кЁо брать
минимальнь|е.
$
3.
€тационарпь[е дпффузио|{нь[е
потевцпадь[
па
поРисть!х
дпафрагмах
с переме[|нь[ми
градие|!тами
алектРического
шо^я
Ранее
при
вь1воде
уравнений
3ависимости
дифу3ионного
потенциала
от
концентрации
и
коэфициентов
дифу3|4ш'
а так}ке
электропроводности
й'"й''Бй""1'ой
солевой'6реды
.пРеАпойагалось'
что
в
пределах
диафраг-
!иьт,
толщина
которой
равна
! см,
трациент
электрического
потенциала
постоянен:
ёе'|ёх:е'||:соп51.
6|

3то предполох{ение в какой_то мере
отвечает
действительности
в
случае
диафрагм
с
однородной
структурой. 8сли
х{е электрические
свойства,
материала
диафрагмьт
и
ее
пористость неоднороднь| и'меняютс{
|]Ф ?Фй:
щине'
то градиент
потенциала
мох(ет
оказаться
непостояннь|1\!. 1огда
в
уравнении
вь|нух(денной
диффу3ии
ионов'
имеющих постояннь|е
коф_
фишиенть:
дифузии
(диафрагма
ра3деляет расплавь|
бо1}|3(}1)(
составов)
0|+]
(х'т)
-
,02|ц!
(х,
т|
-
о(х,
Ф
цР
0т 0х2
0х
скорость
их перемещения под во3действием электрического поля
в
диа-
фрагме ух(е
не
постоянна'
поскольку она связа!|а
с
градие}ттом
потег|ци-
ала соотнотпением о:_цё.ед16х, где ш
_
подви}кность ионов.
9тобьт
ре1шить
дис}ференшиальное
уравнение
с
переменнь:м
коффициен_
том в
условиях
стационарной
линейной
дифузии
(0!л{(х,1)|о1:0)
42[']
(х|
_,(!.ё!'!
(х)
:.
4х2 о
-|7-"'
надо
3нать
явньтй вид
функшиш
о(х), когда электринеский потешциад
меняется в 3ависимости
от .х в пределах
диафрагмьт
(!}--х>-0)
ра3личнь|м
обра3ом. Рассмотрим несколько случаев его монотонного
и3менения (бе3
экстремальнь1х точек
внутри
диафрагмь:),
опись:ваемого
функциями:
9т:атх2; ч':''{*; 9з:ав(е*
-|);
9ц:ац1п
(1
+х);
9ь:аь1с.
3десь с_параметрь!' 3ависящие
от типа
диафрагм,
сорта
диффундиру_
ющих
ионов' их концентрации, температурьт.
|1осле
диффренширования
этих вь|ра!(ений
по
.т
и
подстановки
градиентов
электрического
потенциала
в соотно|пение
Ёернста
_
3йнтлтейна
(для
упроще}{ия
выкладок полагаем
}:1,
помня'
что
поправочнь|й коэфициент мо'(но ввести
в
конечные
вь|ра2кения в виде сомг1о}кителя перед величинами
электрических
3аря_
дов'
2е' ионов),
имеем:
о'(х):-
2ат1:ох
;
оу(х):_
а'2е1=1
о'(х)--
.{3,
,';
д\/
ьт
2ьтт;
ьт
о'($:_##3;
оь(х):-#
1огда
дис}френциальное
уравнение
пРинимает вид:
42?:|
(х|
,
2а'а,ех ё!:/
(х)
_ ..
ах,
-
ьт
_а*
_"'
для
стационарной
линейной
диффузиш
42!:/
(х)
,
442€ ё!'|
(х)
-
..
а'"
-т
нц1+х)- а'
_"'
ё2!'{
(х|
,
422ё
ё!'[
(х)
^.
ё2!ъ|
(х)
,
а52е ё!'|
(х)
^
-т-----------:=
_=-:9,
а'"
=
нт а'
:".
4х2
2ьт1[;
4х
42['[
(х)
,
а"ае!х
4[,|
(х\
^.
а',
-
ьт
_77:"'
|1осле
двукратного
интегрирования
этих
однороднь1х
уравнений
при
граничнь|х
условиях
/г(0):ш0
и 00(!):0'
получаем их
ре1'пение
в
виде
3ависимостей
!я{
(х):
&(.
в2
00,
(х):00.
0,['
+')
"*(_,,{т)
_0
'
0,1/
у
+т).*р
(_а,
1/г)
_1
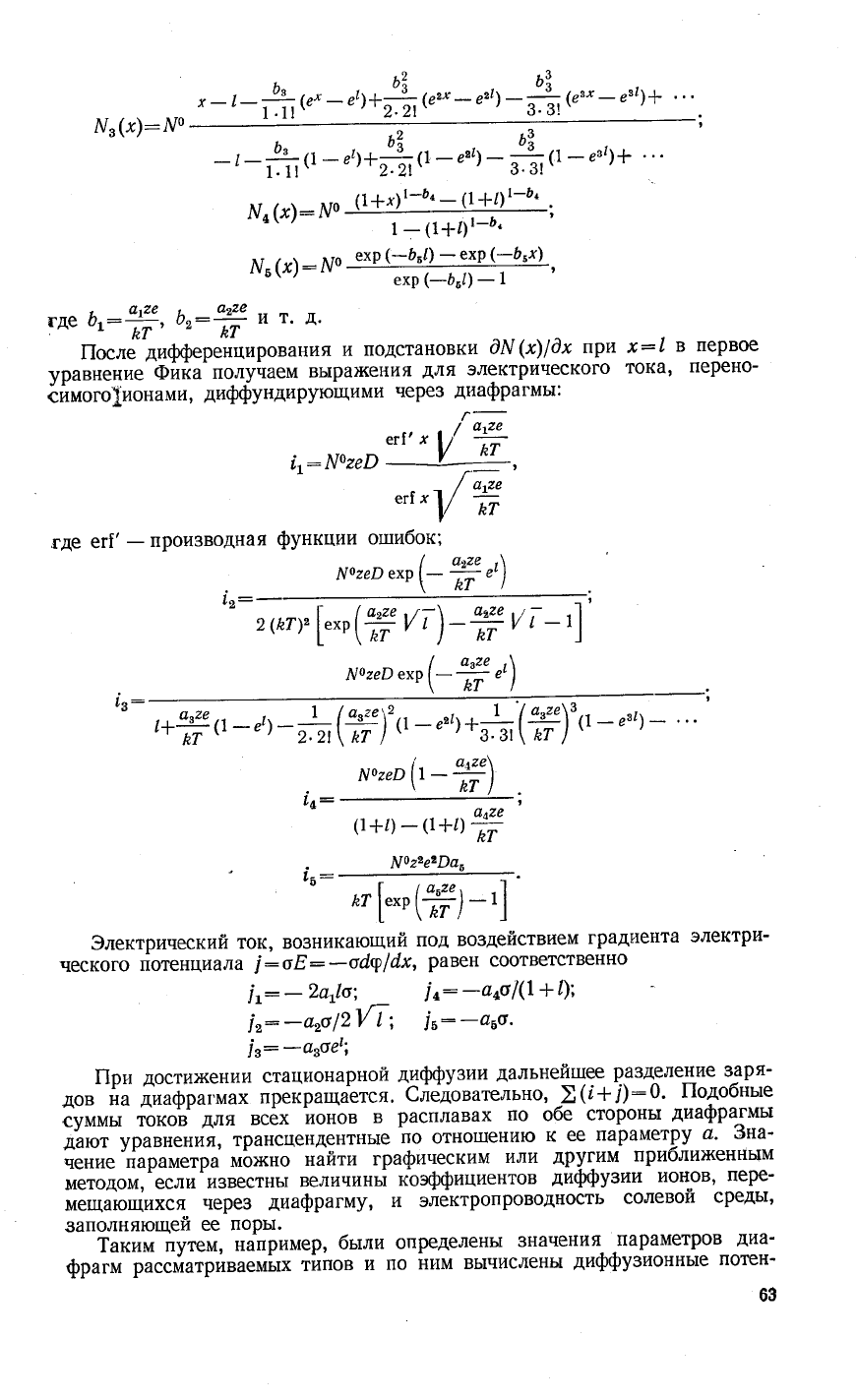
А/'(я):до
'
-
ь*к'-
-
',)+*у(еох
_
ее!1-*
1'зх
-
ев!14'.'
-, -*,,(|
-
ы'+*(
_
еас7_
*
(
_
ез!)+'
"
:!^
(х):
дло
(11х11_а*
_
(1+,)1_0'
1
_
(1+01_ь'
1т:
[',|0эеР
/ а'2е
"гг'
х
|/'
#
{7.'
"'1'у
й
где
ег['-
прои3водная
функции
оп:ибок;
-
м,.,о
"*р
(-
#
,!)
.
;Б|:"'ьт)-ж/с
-т]'
!,!0аеР
ехр(_#
')
|а:
[3:
*(#)'
11
_
е"|)
-*(#)'{1
_
":1
-'
"
,+#0-,!)-
о4_
!6:
! а^2е\
['!оэеР\|-
*
)
а^2е
(1+/)-
(\+|';
[:|оэ2е2|аь
*г[.*,
(#:_']
3лектринеский
ток, во3никаю]ций
лод
воздействием
град[1ента
электри_
чес
ко
го т|оте
н
ци
а
л а
|':"!;
;
"
'''
'''
|
^::;;Ё;;'"-
""
';:_|:!#п'
!ь:_аьс'
|1р:п
достих<ении
стационарной
4!фузии
дальнейшее
ра3деление
3аря-
до"
йа
1иафра:'мах
прекраща!тся.
€ййовательно'
)('+0:0.
||одобнь:е
суммь|
токов
для
вс6х
йонов
в
расплавах
по
обе
стороны
диафрагмы
дают
уравнения'
трансцендентньте
по
отношению
к
ее
парамет!}
о.
3на'
чение
параметра
мо}кно
найти
графинеским
или
другим
приблих<енным
методом'
если
и3вестньт
величиньт
коффишиентов
дифузии
ионов'
пере_
мещающихся
чере3
диафрагму,
и эйектропроводность
солевой
средь|'
3аполняющей
ее
поры.
1аким
путем'
например,
бьтли
определены
3начения
_параметров
диа'
фрагм
рассйатриваемь1х
типов
и
по
ним
вь|числены
диффузионнь1е
потен_
63
\
*/,
\
|
|5
60
цееп
|00
т,с€/(
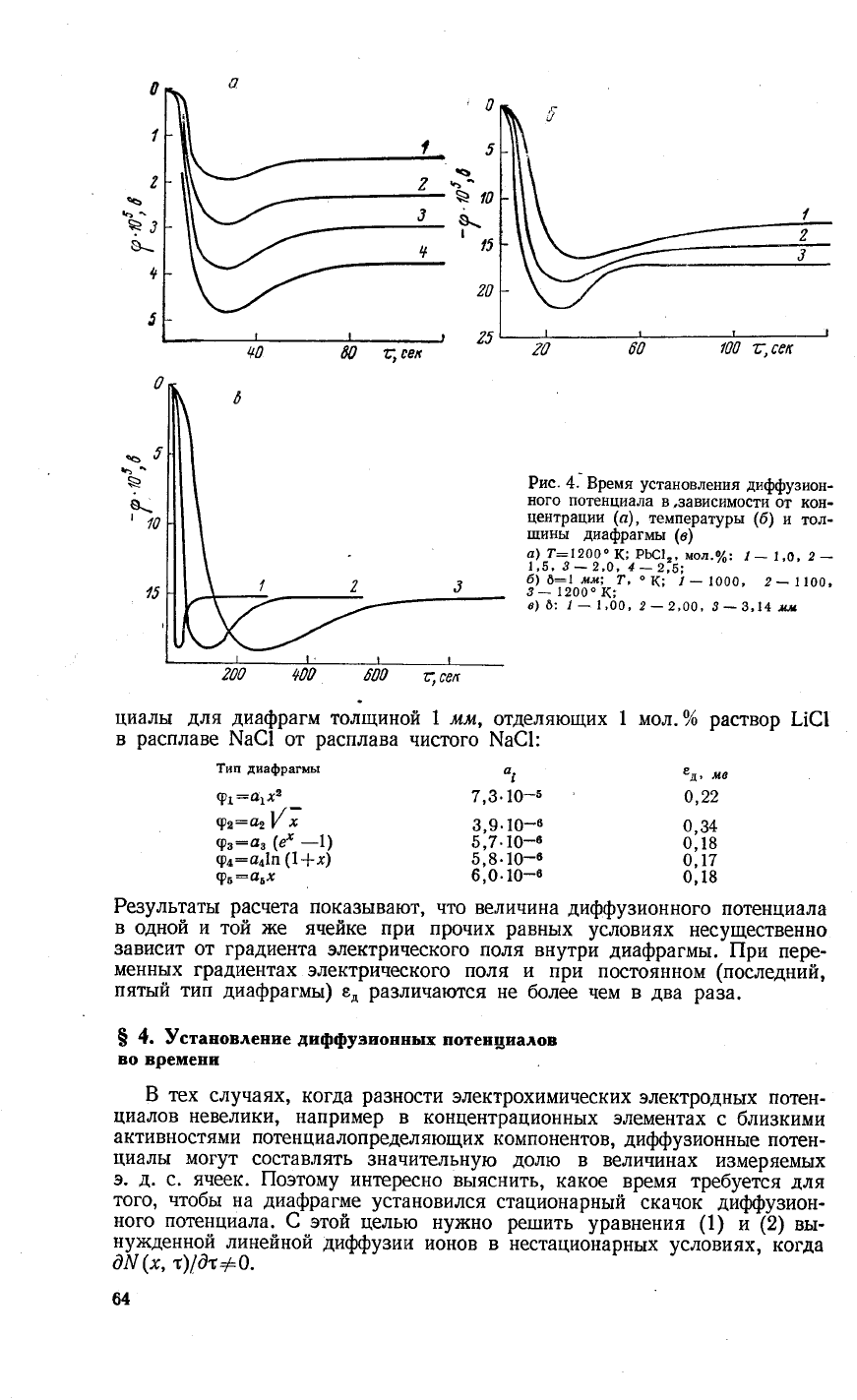
Рпс.
4,
8ремя
установления
диффузион_
ного
потенциала
в,зависимости
от
кон_
центрации
(а),
температуры (6)
и
тол-
ш:ины
диафрагмь:
(с)
а)
!_^\200о-к:
РБ€|',
мол.о/':
|
-
1,0, 2
-
1,5,3-2,0,4-2:5:
б,
о:1
лм:
?'
"
к;
:
_
|000,
2
-
1100,
3
_
1200"
к:
6) 6: 1
-
1,00'
2
_
2'00'
3
*3'14
п.у
200
+00 600
цсеп
циалы
для
диафрагм
тойин
ой
1
мм,
отделяющих
1 мол.
%
раствор
!!€!
в
расплаве
}.,1а€1
от
расплава
чистого 1т{а€1:
тип
двафрагмь!
9т:@тх2
9':а'/}
Фз:аз
(ех
_|\
чц:ад1п
(|{х)
9в:@ьх
а.
'
7,3.10-5
3,9.10_в
5,7.10-6
5,8.10-6
6,0.10-0
ед,
л@
0,22
0,34
0,18
о,17
0,18
Результатьп
расчета
пока3ывают'
что
величина
диффу3ионного
потенциала
в
одной и той х(е
ячейке при
прочих
равнь1х
условиях
несущественно
зависит
от градиента
электрического
поля
внутри
диафрагмь|.
при
пере_
менных
градие}1тах
электрического поля
и при постоянном (последний,
пятый
тип
диафрагмы)
ед
ра3личаются
не
болёе
чем
в
два
ра3а.
$
4.
}становденпе
диффу3поншь|х
потешцпалов
во
временп
8 тех
случаях'
когда
ра3ности
электрохимических
электродных потен-
циалов
невелики'
например
в концентрационнь|х
элементах
с близкими
активностями
потенциалопределяющих
компонентов'
дифу3ионньте
потен-
циаль[
могут
составлять
3начительную
долю
в величинах
и3меряемых
э.
д.
с.
ячеек. ||оэтому
интересно
вь|яснить'
какое время требуетъя
для
того' чтобы
на
диафрагме
установился
стационарньтй
скачок
дйфузион_
ного
потенц|1ала.
€
этой
целью
нух<но
ре|пить
уравнения
(1)
й
!2)
вы-
ну_х{денной
линейной
дифу3ии
ионов в нестационарных
условиях'
ко}ца
0!'|
(х,
т)|0т10.
64

|1роизводя
довольно
громоздкие
выкладки
[170],
связанные
с
дифф-
ренцированием
по
.х
выра}{(ения' получаемого
и3
уравнения
(2) при
учете
начальнь|х
и
граничньтх
условий,
с подстановкой
результат0в
в
первое
уравнение
Фика и
суммированием
электрических токов'
пере[!осимых
ионами
нерез
диафрагму'
получаем
трансцендентное
уравнение.
Фно
опи.
сывает и3менение
диффузионного
потенц|1ала
со
временем
0г начала
диф-
фузии
ионов нерез
диафрагму
толщиной
! см
с
постоянным
градиентом
электрического
поля.
3 слунае
расплавленнь1х
солевьтх смесей близких составов
с
высокой
электропроводностью
трансцендентное
уравнение
мохшо
упростить
и по-
лучить
в
явном виде вь!ра'(ение
для
3ависимости
дифузионного
п0тен-
циала
от
времени:
т
.-/
€уммирование прои3водится
по
всем
ионам'
участвующим
в
пеРносе
тока чере3
порьт
диафрагмь['
3аполненные
солевь|м
расплавом'
с тем
х{е
правилом
3наков' как
при
ре1пении
стационарной
задати.
3десь
гп:1, 2,
3,
.
. .
|{ри т
_>
оо'
т. е.
при
подходе
к
ста1|ионарному
состояни:о
диф_
фузии
терез
диафрагму'
получается
ух(е
и3вестное нам приблип<енное
вырах(ение
(7)
для
стационарного
диф}3ионного
потенциала.
8ремя
установления
стационарного
лот€нциала
не 3ависит
от гради-
ента
концентраций ионов в
расплавах
по оф сторонь|
диафратмы,
но
оно 3начительно во3растает с
увеличением
ее
толщинь|
и
умень1пается
при
повь|1пении
температурьт' так как
увеличивается
скорость
диФФрии.
Бсе
это
иллюстрируется
ре3ультатами
расчетов
для
ячейки
!шРьс1, +
( 1
-
00) 1.{а€1
|
кр"., >
| |
1'{а€1
1 рас'-1
в
3ависимости от концентрации'
(рис.
4).
]
температурь|
|4
толщи}1ь|
дпафрагмы
Ф-
чд_
*у#
{'
*,
!
с_'г.-р
[_
(#)ъ-"]}
.
5м.в.
€мирнов

1'лава
у
тБмпв,РАтуРнАя
и
концвнтРАционнАя
зАвисимость
э.
д.
с.
вь!сокотБмпБ,РАтуРнь!х
гА^ьвАничБских
э^БмЁнтов
с РАсп^Ав^вннь!ми
со^Б,вь[ми
э^ЁктРо^итАми
$
1.
йзмерение
а.
д.
с.
вь[сокотемпературнь|х
ячеек
с
расп^ав^еннь[ми
солевь[ми
а^ектродитамп
3лектродви)кущая
сила
гальванических
элементов
представляет
собой
ра3ность
потенциалов
мех(ду
их
электродами
в отсутствие
тока.
Фна
не
совпадаетснапря}кениемвь!сокотемпературнь1хячеекстокоподводами
и3ра3нь1хматериаловиэлектролитамивполуэлементах'разделеннь1ми
.'рй.','й"
д'афраг"а"и,-котор.ое
включает
еще
термо-э.
А.
с..
(в') мокАу
;;;;;;;йд{й,
!ё".'''.
1тт,
$'д)
т1
диффузионньтй
потенциал
(в')
|1а
диа'
фрагмах
(см. гл.
|\/):
е'1зм:8
*
8т*0д.
|[ри
измерениях
обь:чно
устанавливают
равновеснь1е
значения
э.
д.
с.
в
определенных
условиях,
когда
на
обоих
электродах
достигается
состо-
яние
термодинамического
равновесия'
Фб-этом
судят
по
постоянству
величинЁт
измеряемой
э.
д.
с.
во
времени.
Фднако
нередко
э.
д.
с.
вь1со_
й''"йй"ра.урн6и
ячейки
в
течение
пРодол)кительного
времени
меняется
мало'асистемавцеломе|цедалекаоттермодинамическогоравновесия.
Аело
в
том'
что
при
вь]соких
температурах
в
хлориднь|х
расплавах
отсутствуют
заметнь:е
3атруднения
в
пере3аряде
и
ра3ряде
ионов'
а
так-
>ке
ионизации
вешеств
на_
электродах.
Бследствие
этого
мех(ду
поверх-
ностнь|мислоямиэлектродовиприлегающимикнимслоямирасплавлен-
нь|х
солевь1х
электролитов
очены
бьтстро
устанавливается
термодинами-
ческое
равновесие.
1'1х составь|
могут
при
этом
сильно
и3мениться
по
соавнению
с
объемнь:ми
в
электролите
й
в
электроАе'
А4е>кду
повеРх;
йБ"",",
и глубиннь:ми
слоями
во3никаю'т
-градиентьт
концентрации
и поро}кдаемь1е
ими
ди{'фузионньте
потоки'
!,иффузионное
вь1равнивание
й'"шБ"'рЁший,
особенно'
й-тверАьтх
фазах
электродов'
происходит
3начи-
тельномедленнее'врезультатечегоэлектродньтепотенциальт'опреде.
ляемь|е
активностями
йотенциалопределяющих
компонентов
на
гранидах
раздела
фаз
электр'![''.й'р'лит'^
медленно
менятотся
во
времени'
Фни
йрйо'"*Ё,'тся
к
р1вн6весньтм
3начениям
по
мере
того'
как
вь1равниваются
составь|
поверхностнь|х
и
глубинных
слоев
электродов
}1
9,/1€(1|Фо'1и1ФБ.
1(онечнь:е
сйтавьт
их
отличатотся
от
исходньтх
тем
больш:е'
чем
даль1це
от
равновесньтх
бьтли
последние.
1ак,
например'
в
равновесии
с
металлическим
цирконием
"ч:
}00Р^]
в оасплаве
|;с:-
"
мольнодолевой
концентрашией
егч.ионов
|тт|:т'о,,
;-Б;;'ши
й",р''*'пится
на
долю
7т2+'и
литль
|7о'6
-""-ё9{у^.3.:::
[ьь1.
по''ому
на
циркониевом
электроде,
погру}кенно1\{
8
!8€||а'128'/|енньти
!!€
1,
содер>кащий
[-
;;';'.';;"
;ю1;;
й;Ё;"
;;й;
/;;;
г
т^'
!
уте+.
Бозни-
кают
градиенть1
концентраций,
под
в6здействием
которьтх
ионьт
7г2+
дифун!цируют
и3
приэлект-родного
в глубиннне
с9о1эдектролцта'
где
концентрацр|я
их
вн)чале
6ь:ла
равна
нулю'
Б обратном
направлении
дифундируют
ионь[
7гц+.
|\олное
термодинамическое
равновесие
ме}кду
66

электродом
и всем объемом
электролита
достигается
тогда, когда
вь|рав-
ниваются
составь| его
приэлектроднь!х
и
глубинньтх
слоев.
Фбщая
кон-
центрация
ионов
циркония
в солевом
расплаве
во3растает при
этом более
чем
в
полтора
ра3а
по
сравнению
с
первоначальной.
[змерения
э.
д.
с.
проводят в ятлейках,
устройство
которь1х
обеспе_
чивает
максимально
во3мох(ное
приблих<ение
исследуемь!х
систем
к
рав-
новеснь1м
условиям.
||осредством
диафрагм
исключается
бестоковь:й
перенос
металлов
и
хлора через
электролит
с'одного
электрода
на
дру-
гой.
Фсобое
внимание
уделяется
тому, нтобьт
электролит не взаимодей-
ствовал
со стенками
и
га3овой средой
ячейки
или'
по
крайней мере'
их
взаимодействие
не ока3ь1вало существенного влия|1ия на
активности
потенциалопределяющих
ионов
3а
время измерений. в
полуэлементах
с
металлическими
электродами' которь]е
обмениваются с электролитами
ионами
ра3нь1х
валентностей, требуеплую
концентрат1ию их
3адают
анод-
нь1м
растворением
металлов.
Фчень
ва)кно' чтобьт температура
ячейки поддерх{ивалась при
задан-
ном 3начении
постоянной, а электролит и электродьт находились
в и3о-
термической
зоне
нагрева.
1емпературньте
коэффициентьт
большинства
гальванических
элементов
_
величиньт
порядка
десятьтх
долей
милли_
вольта
на градус.
|1оэтому колебания тем|1ературь!
да}ке
на
2-3"
вь|3ь1вают
разброс
экспериментальньтх
точек
в
пределах
нескольких
милливольт.
1(огда
электродьт
име}от
ра3нь1е
температурь!'
мех(ду
ними
возникает
термо-э.
д.
с.
|171-179|.
Фна во3растает
с
градиентом
температурь|
и 3ависит
от состава электролита.
Б
зависимости
от соотно1пения
тепло-
вь1х
потоков'
переносимь]х
анионами
и
катионами' термо-э.
д.
с.
мо'(ет
бьтть
одного
|1ли
лротивоположного
3нака с
ра3ностью
электрохимических
потенциалов
ме)кду электродами
неи3отермических
ячеек.
Ёеобходимо
тщательно
удалять
из
ячейки кислород
и влагу'
которь|е
могут
образовывать
с
потенциалопределяющими
катионами
нераствори-
мь|е
в хлориднь1х
расплавах
оксисоединения и тем
самь1м
умень1пать
их
к0нцентрацию
в электролите.
€ этой
целью
ячейки
гермети3ируют'
их
содерх{имое
вь|дер>*(ивают
под поних{еннь1м
/(авлением'
постепенно
повьг
шая
температуру
до
полного плавления
солей. 9ерез
расплавь!
проду-
вают
сухой
хлористь:й
водород и хлор, чтобьт
растворить
оксисоединения,
образовавтпиеся
под воздействием следов
влаги
и кислорода
во3духа
[180].
1акую очистку
электролита нух(но
производить
особенно в
тех
случаях'
когда он содер'(ит
много3аряднь]е
катионьт'
а так}ке хлорид
л|1тия
[131].
!{тобь]
удалить растворецнь!е
хлористь:й водород
и х.пор,
чере3 солевь|е
расплавь}
перед погрух(ением электродов продувают
аргон
или
гелий, очищенньтй
от
следов
кислорода'
влаги и
да'(е
а3ота' кото-
рый
образует
при температуре опыта нитридьт
с
исследуемь|ми
металлами.
||ри
работе
с
хлорнь]м
электродом необходимо
следить
за тем' чтобьт
в окру}кающем
его
электролите не бьтло взве1пенных частиц
окислов
и
оксихлоридов
металлов.
||опадая на хлорньтй
9лектрод'
они ока3ь1вают
на
него сильное
деполяри3ующее действие;
его
потенциал
становится
неустойчивь!м:
падает' а
3атем
вновь во3растает' когда попав[пее
на
электрод
оксисоединение
полностью прохлорируется.
||о характеру
и3менения э.
д.
с. во
времени мох(но
судить
о
вь]3ь1ва-
ющих его
причинах.
8сли, например' в
элементах с
хлорнь!м
и металли_
ческими
электродами э.
д.
с.
монотонно
умень1пается'
то это
свидетель-
ствует
о непрерь'вном
увеличении
концентрации
ионов
металлов
в
ре3уль-
тате
попадания окислителей, в том числе
хлора' на
металлические
электродьт.
Ёаоборот, э.
д.
с. возрастает' когда их концентрация
падает'
например'
при испарении летучих
хлоридов
и3 электРолита.
Аногда
приходится со3давать электродь[
непосредственно
в
самой
ячейке электролизом'
оса>т(дая исследуемьтй
металл'
например плутоний,
на
катоде.
Б
подобнь:х
случаях и3мерения 9.
А.
€; начинают
не сразу
к*
67

после вь1ключения
тока
электроли3а'
а
спустя
некоторое
время' необхо-
димое
для
того' чтобь1
исче3ла
концентрацион1{ая
поляри3ация металли-
ческого
электрода.
Равновесньле
значения
э.
д.
с.
вьтсокотемпературнь|х элементов
дости_
гаются
в течение
продол}кительного
времени
да)ке
в ячейках с
хоро1по
продуманной
конструкшией.
|1ри
этом всегда
имеется опасность
принять
сйупййнь:е
стационарнь1е
величинь1 3а
равновесные
э.
д.
с.
1олько по'
вторнь1е
и3мерения
с
варьированием
конструкционнь|х
особенностей
используемьтх
ячеек
дают
во3мо}кность
исключить
источники слунайнь:х
или систематических
ош.тибок
и оценить
достоверность
получаемь|х
ве-
личи!|.
$
2. [емпературная
завпсимость
а.
д.
с.
вьпёокотемшеРатурнь[*
тадьванических
адементов
с
расп^ав^еннь[мп
хдориднь[ми
эдектролитами
3.
д.
с.
всех концентрационных
элементов
во3растает с
повь11пением
температурьг'
притом
тем быстрее'
чем больгце отно1пение активностей
потенциалопределяющих
компонентов
в
полуэлементах
и мень|ше их
вале|{тность.
Б гшироких
температурных
интервалах эта 3ависимость
ли-
Бейн'},
поскольку Активности
одних
и тех
>ке коп,1понентов в близких
по
компо3иции
средах'
в
которь|х
они содер)катся-
в
ра3ных
концентрациях'
меняются
с
температурой
почти одинаковым обра3ом.
Более сло}к!|ую
температурную
3ависимость
имеют
э.
д.
с. химических
элементов.
|1ококем
это
на примере
элементов с хлорным
и металличе-
скими электродащи.
|[ри
Рс\,
| агпм
ьн
!'|е
+
1
|
2п
^13'
'
*
'
'-
^н8т"с:,
1
*
1
пР
-|
3%*'/аа53г',",_
5&"с:',*,*
&
1п
с*",+'с3:-_
пР
3десь
А//0
и 50
_
соответственно
энтальпии и
энтропии
-веществ
в чистом
виде
и
указанном
агрегатном
состоянии
(металл мох(ет
бьтть твердьтм
или
хсилким)
при
данной
температуре
/'' причем
АЁ*т"сг,
с*
:
:
.'}"?*,
*
'л|/3п-*
:
и
5$т"с1л
(,к)
:
в1^"?*,
*
*3,
',,
где
^Ё10
и
50
_'энтальпии
и энтропии
ука3анных
ионов
в
чистом
жидком
хлориде
йе€1,,
'^"1#",,,
!1 о61|'аспл)
-
их
активности
в хлоридном
рас_
плаве'
содерх{ащем
Б'растворенйом
состоянии
хлорид
йе€1' и
находя-
щемся
в контакте
с
мёталлическим
электродом.
|1ереходя
к мольнодоле-
вым
концентрациям'
имеем:
ьн!""+\
АЁ3''с":
-
АР$тес|а(:к'_
&?'
1п
|*''*
пР
я!'"+{
з$,'1г1
_
$8тес:,,
1*1*&1
1п
[[{е'+]
_т
пР
|1ервый
член 9гого
равенства
свя3ан
с и3менением
энтальпии'
а
второй
-
энтропии
при
реакцйях
обра3ования
хлоридов
йе€1, не
в чистом
>т(идком
виде,
а
в
расплавлен!!ых
солевь|х
смесях
данного
состава'
где
конце-н_тра-
ц,{"
"
кофишиенты
активности
их
катионов
равнь|
соответственно
[:!1е'+]
68

,
|^.'*
(мольнодолевая
концентрация
ионов
хлора
во всех
хлориднь1х
расплавах равна
единице'
а
их т<оэффициент
активности
мо)кно
условно
поло)кить
равнь|м
единице):
!м1е
+
|
|
'п
€|э1
г1
:
йе€1,.
1аким
образом,
о:
_
[|]
|пР
+|
[5|пР
:
_
\\6|пР.
Аналогичньте
вь!ра}1(ения
получаются
для
любого
химического
элемента.
3нта,тьпии
и энтропии
Р|акший
меняются
с температурой,
поэтому
"линейная
3ависимость €
от ?
наблюдается
ли1пь
в
тех
температурньт1
интервалах'
где
и3менения [[.||пР
и А'3|пР
не вь1ходят
за, пределы_тон_
ности и3мерений
э.
д.
с.
Фневидно,
чем
она вь]т]1е'
тем
ух(е
эти
интер-
вальт.
€
рас1пирением
их
на политермах
э.
д.
с. появляется
криви3на'
превосходящая
разброс
экспериментальнь1х
точек
[162].
!,ля
многих
реакций
изменение
энергии
[иббсй
в
зависимости
от
тем_
пературь{
хоро11]о
описьтвается
эмпирическими
уравнениями
вида:.
\\6
:
ц'
*Р'
7 1п
[
1
у'
72
*
|,
|_1
1
$,
7.
9исленньте
3начения &',
Р',
\', €'
и
ф'
находятся
и3
экспериментально
определяемь|х температурнь]х
зависимостей
теплоемкостей
компонентов
реакший,
которь|е об_ь11н9
вь1рах(аются
уравт{ени
ямитипа
€р:а*07
+ст-2.
.[|ля
ка>кдого
компонента
^н$:
[[]9,,+
'!
с,ат,в}:58ов*
|
?
'',
^ст:
^н|-
т53.
298
2э8
(ледовательно'
политермь[
э.
д.
с. мо}кно
более
точ!{о
вь1ра3ить
эмпири-
ческими
уравнениями:
е
:
с
*
Р7
1п
7
+
\72
+Ё?-!
+
т}7,
о"^8'
где
с:_-='
р:_-
и
т.
д.
п! пР
1емпературньтй
коффициент
э.
д.
с. получается
равным:
(а,
:р
19
7+ 2у7
_
€7-'
+0,4343р+ Ф.
|[одобные
эмпирические
уравнен|тя
для
э.
д.
с. и
ее
температурного
коффициента
вьтводятся и3
экспериментальнь]х
даннь1х
способой
"'"'1,"й1_
!ших
.квадратов:
составляются
системь1
и3
пяти
характеристических
урав_
19]!й:
которь|е
ре[|]а}отся
относительно
искомь]х
величйн
с,
$,
у,
-5'йБ.
оная их'
мох(но
определить энтропию
реакции,
идущей
в
элементе.
3ависимост"
,.
1-^9.^
о:
тм1ературьт
мо)кно
вьтрах<ать
в
виде
эмпири-
ческих
уравнений
иного
вида. 1ак,
например'
из
!езультатов
изпсереЁий
напря'(ения
разло'(ения- р_асплавленного
хлорида
свинца
с
помощью
элек_
:Р9-1''-|'_
*о_м],1утатора
[72|
.Р^,пределах
точности
определени
й
'*0,2 -мв
бьтло получено
вь!рах(ение
[73]
е:
1 158,90
_
54,1'
(1#)+0,833
(#)'+0,062
(#),
-
+0.116
(2тоо
''
\
тоо
)''
!0,8
мв в
интервале
498_750
ут
*7,2
мв
в
\4н,|ервале
750-в66"с.
1(огда
точность
измерений
э.
д.
с.
не
превы1п!ет
10_3
6' температур_
ная
3ав1'1симость
хоро1по
опгсьтвается
линейнь:ми
уравнениями
типа
в:а*0|
в
довольно
1пироких
интервалах
те*перату'р'
доходящих
до
нескольких
сотен градусов.
это
мох(но
видеть
на
прййерах
конкретнь1х
травнений,
которьте
рассчитаны
и3
'
известнь:х
темпфафньтх
3ависимо-
69

стей
^с
для
реакций
в
соответствующих
элементах
с
расплавленнь1ми
хлоридами в качестве
электролитов:
.&1е
|
&1е€1,1*1
|€12,",,
с
[183].
1. 1
!
']'с*;
*7
€12
1",:$а€11х11
,
1073-1162"
к.
^с
:
_94
500
-
2' 52т
1л
!
-
2,27'
10_вт
2
+
0,
42.
70-6т
3
-
17 000
/
7'
+
38, 027
кал'
1
2.
$а1г1
*
,
с1'
111:$а€11*1,
1162-1300"
к.
^с
:
-12о
9оо
-
6,72т
1п
7{0,
01
5. 10_3т2
-
17 000/7+88' 05]л кал,
АЁ!,
',
:-э0
150 кал
/
моль
8:3'919
-
6'34.10-{7+0,001 в,
^;/0:-90
380 кал/моль,
^30:-14,62
кал
/
ера0'
моль.
^н?200
:-1
1
2
900 кал/
моль,
АЁ|..'
:-:
1
2 200
кал
/
моль,
е:4'880
_
1,45.10_з7+0'000
в'
^но:-\12543
клл/моль,
А5о:-33,44
кал/
ера0. моль.
^н3'':-
27 450
кал/моль,
АЁ?''.
:-
25 650 кал1
моль,
8:1
'
156
-2
'о.10_д?+0,002
е
^н0:-
2666Ф кал/моль,
^50:-
4,61
кал/
ера6. моль.
1175
1200
1225
125о
1275
1300
--:73252
-72
407
-71
587
-70728
-69
893
-69
062
3,176
3,140
3,104
3,067
3,031
2,995
8ф
9ш
1000
1 100
1200
0,998
0,975
0,954
0,935
0,918
1
3.
(1г1
*7(1',.,:(€11ж1,
1043-1200'
к.
^с
:
-122
000
-
5' 697
1л ?
+
0,042' 1 0-3т2
-
1 5 000/7+79,28|
кал,
^л?
1
00
:
-1
1 5 800 кал/ моль,
АЁ?'''=_ 115 250 кал/моль,
€:5'014
-
1'
46.
10-з7{0,000 в'
^н0:-
115'633 кал/ моль,
^50:-33'67
кал
|
ера0'
моль'
1
4. сш(')+'
(121'1:€ш€|.*),
703-1200'
к'
^с:-
31
800
-
6,07
1п т+0'765.10-3?2-
17 0о0/т
+5о,57
кал,
А,6,
кал
!
",
,
-23о17
-22
482
-21
999
-21
559
-21161
1
5.
А8с'>*7 с12
(г):А8с11ц;,
728_900'
(.
^с:-29
940
-
6'50т
1п 7*1,03.10-з7'9+1000/?+54'5!
кал,
^н3'.
:-
25
400
кал7
моль'
^н3,'
:
-
24 900
кал
/
моль,
70
