Мамаев Н.Н. Гематология: руководство для врачей
Подождите немного. Документ загружается.


Chromosome
22
Chromosome
9
• •!// Ill
JlLy
•
Illl
»ll ill
р230
Ьсг
-
Яис.
9.3. Структура генов ABL и BCR; основные механизмы их повреждения
при
хроническом миелолейкозе
мющий
различные сигналы из самой клетки и из внешней среды, способен
тровать как процессы клеточной пролиферации, так и апоптоз. Что касает
ся
П1|ипннкиназной
активности, за нее отвечает домен SH1, в то время как S{^2
И
НШ обеспечивают связывание этого белка с другими протеинами.
Другой участвующий в патогенезе ХМЛ BCR-протеин имеет молекулярчу
ю
v 160 кДа. Он также состоит из нескольких доменов, один из которых обл
а
_
jitirr
тирозин-киназной активностью (рис. 9.5). Поэтому центральная часть ц
о
_
пгкулы этого белка способна стимулировать реакцию дефосфолирированц
я
\ \Л\ что приводит к активации факторов транскрипции. В свою очеред
ь
i
фрагмент BCR-протеина обладает ГТФазной активностью и таким образ
0
^
учпгтвует
в активации RAS-белков, регулирующих полимеризацию актиц
а
pl45ABL
NIL
МЫ
la
cde2 PKC
(P) (P)
cde2 PKC
?
:SH1:
Рис. 9.4. Тонкая структура гена ABL (Deininger M. W. N. [et al.],
2000)

pi 60
13
CK
5 1Y177 Р190
(1-426)
NH
2
\У\ I
DD
P210
(1-902/927)
P230
(1-1176)
RHO-GEF
<clbl
like
and PII domenin>
COOH
CQ
1271
PHC.
9.5. Тонкая структура гена BCR (Deininger M. W. N. [et al.J,
2000)
а также в функционировании НАДН-оксидазы в фагоцитах. Кроме того, через
связывание с Grb2 BCR-протеин оказывает влияние на передачу сигналов по
RAS-пути, что усиливает пролиферацию клеток. Наконец, через активацию
PI3P
этот протеин подавляет апоптоз.
Во время реципрокной транслокации поломка
ABL-гена
может произойти в
любой точке. Чаще всего она происходит
между
1а- и lb-экзонами, при этом
часть BCR присоединяется к экзону а2. Точка поломки BCR-гена может нахо-
диться в одном из
трех
регионов (break-cluster regions). В
результате
альтерна-
тивного сплайсинга формируются либо Ь2а2-, либо Ь3а2-транскрипты, коди-
рующие белок BCR-ABL с молекулярной массой 210 кДа, что характерно для
большинства больных с ХМЛ (см. рис. 9.2).
Как
установлено недавно, продукт химерного гена BCR-ABL обладает высо-
кой
тирозинкиназной активностью. Так, благодаря аутофосфолирированию в
структуре
молекулы резко увеличивается число остатков фосфотирозина, что
создает большее количество участков для связывания с 5Н2-доменами
других
протеинов.
Субстратами химерной тирозин-киназы являются и так называемые
адаптерные молекулы (Crkl и p62DOC), участвующие в организации цитоскеле-
та и клеточной мембраны, а также ферменты каталитических реакций.
В итоге в онкогенной трансформации клетки при ХМЛ задействованы три
основных патогенетических механизма: а) постоянная активность митогенов;
б) подавление апоптоза; в) нарушение адгезии к клеткам стромы и к экстрацел-
люлярному матриксу. Механизм увеличения пролиферативной способности кле-
ток
заключается в постоянной активации ряда сигнальных путей (рис. 9.6).
В частности, BCR-ABL-тирозин-киназа способна связываться с Grb 2-протеи-
ном,
который вместе с SOS-белком активирует сигнальную систему RAS и спо-
собствует
стимуляции деления клетки. В запуске этого сигнального пути
участ-
вуют
также Crkl и p62DOC, активируемые BCR-ABL. Кроме того, увеличению
пролиферативной
способности лейкемических клеток способствует увеличение
активности ИЛ-3 и циклинкиназ на фоне подавления активности ингибиторов
последних.
Ингибирование
апоптоза осуществляется за счет способности химерной ти-
розин-киназы
активировать белки анти-апоптотического Jak-Stat-пути, PI3 и
Akt-пути,
а также активации myc-протоонкогена. Кроме того, в
ходе
онкогенной
трансформации
клеток снижается их чувствительность к проапоптотическим
стимулам (гены р53, BAD, TRAIL) и усиливается устойчивость к апоптозу
(Deininger M. W. N. [et al.], 2000).
I'm
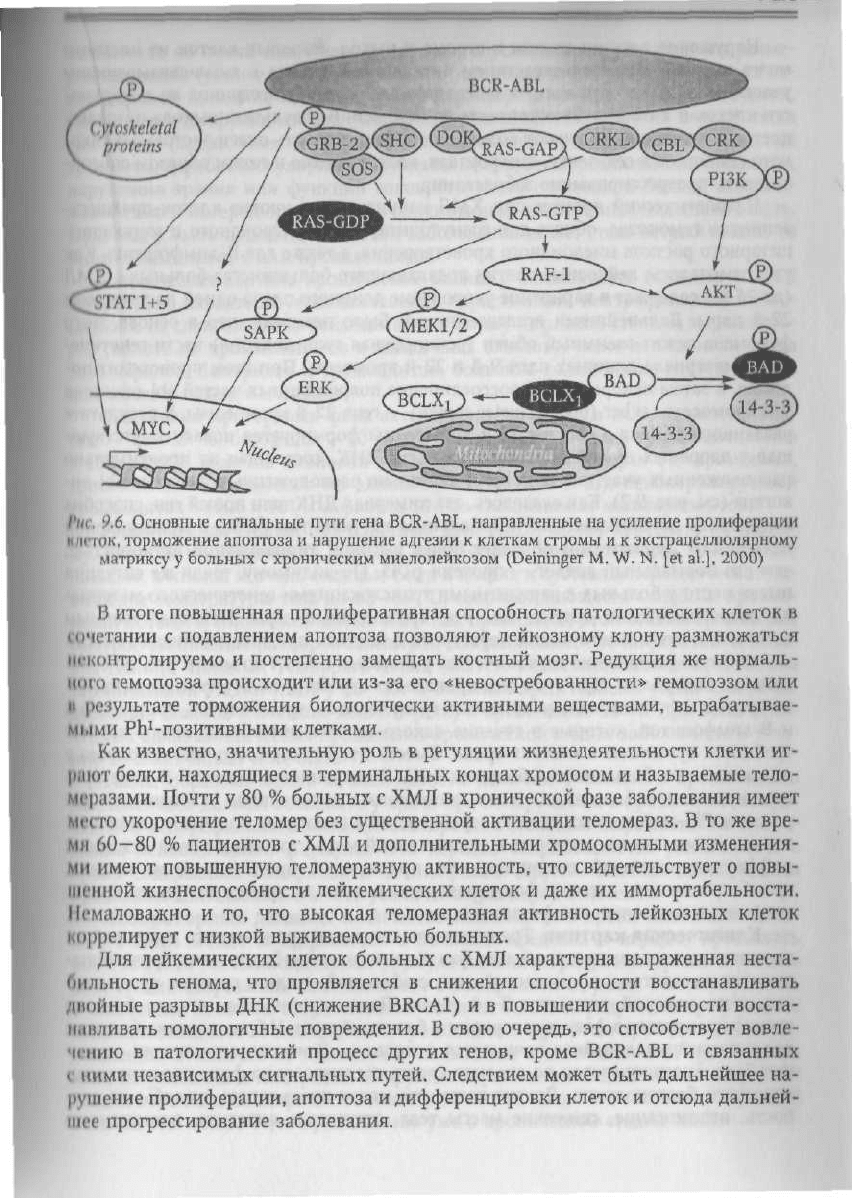
9.6. Основные сигнальные пути гена BCR-ABL, направленные на усиление пролиферации
I'
irroK, торможение апоптоза и нарушение адгезии к клеткам стромы и к экстрацеллюлярному
матриксу у больных с хроническим миелолейкозом (Deininger M. W. N. [et al.J,
2000)
В итоге повышенная пролиферативная способность патологических клеток в
i
очетании с подавлением апоптоза позволяют лейкозному клону размножаться
неконтролируемо и постепенно замещать костный мозг. Редукция же нормаль-
ппт
гемопоэза происходит или из-за его «невостребованности» гемопоэзом или
it
результате
торможения биологически активными веществами, вырабатывае-
мыми
Ph
1
-позитивными клетками.
Как
известно, значительную роль в регуляции жизнедеятельности клетки иг-
рают
белки, находящиеся в терминальных концах хромосом и называемые тело-
меразами.
Почти у 80 % больных с ХМЛ в хронической фазе заболевания имеет
Место
укорочение теломер без существенной активации теломераз. В то же вре-
мя
60—80
% пациентов с ХМЛ и дополнительными хромосомными изменения-
ми
имеют повышенную теломеразную активность, что свидетельствует о повы-
шенной
жизнеспособности лейкемических клеток и
даже
их иммортабельности.
Немаловажно и то, что высокая теломеразная активность лейкозных клеток
коррелирует с низкой выживаемостью больных.
Для лейкемических клеток больных с ХМЛ характерна выраженная неста-
ыпп.ность
генома, что проявляется в снижении способности восстанавливать
щойные
разрывы ДНК (снижение
BRCA1)
и в повышении способности восста-
п.шливать гомологичные повреждения. В свою очередь, это способствует вовле-
чению в патологический процесс
других
генов, кроме BCR-ABL и связанных
•
ними
независимых сигнальных путей. Следствием может быть дальнейшее на-
рушение пролиферации, апоптоза и дифференцировки клеток и отсюда дальней-
шее прогрессирование заболевания.

Нарушение адгезии клеток
к
строме
и
выход
незрелых клеток
из
копишо
мозга
в
кровь является следствием активации F-актина
с
актинсвязывающим
участком
c-abl,
что
приводит
к
снижению экспрессии интегринов
на поверхно
сти клеток
и к
ослаблению контакта
со
стромой.
В
результате
выхода
незрелы!
клеток
в
кровь
они
получают возможность формировать очаги экстрамедулляр-
ного гемопоэза
в
селезенке, лимфоузлах, костях
и
коже
и
таким образом
способ
ствовать прогрессированию заболевания.
Патологический процесс
при ХМЛ
начинается
на
уровне клеток-предшест-
венников
гемопоэза, общих
для
гранулоцитарного, эритроидного
и
мегакарио-
цитарного ростков миелоидного кроветворения,
а
также
для
В-лимфоцитов.
Как
уже отмечалось, лейкозные клетки подавляющего большинства больных
с ХМЛ
(до
95 %)
содержат
в
кариотипе укорочение длинного плеча одной
из
хромосом
22-й пары. Дальнейшими исследованиями было показано,
что в
основе этого
феномена
лежит взаимный обмен (реципрокная транслокация) части генетиче-
ского материала длинных плеч
9-й и 22-й
хромосом.
При
этом происходит
по-
ломка,
а
затем ненормальное воссоединение поврежденных частей abl-онкогена
9-й хромосомы
и bcr
(break-cluster region)
—
гена
22-й
хромосомы.
В
результате
указанного обмена
в
составе
22-й
хромосомы формируется новая,
отсутствую-
щая
у
здоровых людей последовательность ДНК, состоящая
из
проксимально
расположенных участков гена
bcr и
дистально расположенных участков аЫ-он-
когена (см. рис.
9.2).
Как оказалось,
эта
химерная ДНК,
или
новый ген, способна
кодировать
не
свойственный нормальным клеткам
тип
белка
с
молекулярной
массой
210 Да,
который обладает более высокой тирозиназной активностью,
чем
его
нормальный аналог
—
протеин
р145.
По-видимому, такая
же
ситуация
имеет место
у
больных
с
вариантными транслокациями генетического материа-
ла, затрагивающими другие,
чем 9-я,
хромосомные пары. Непосредственным
следствием этих генетических перестроек
в
клетках-предшественниках гемопо-
эза
является увеличение
их
количества
у
больных
с
ХМЛ
во
много раз,
по
срав-
нению
с
контролем. При этом
они
производят огромное количество относитель-
но
зрелых
и
функционально активных гранулоцитов, тромбоцитов, эритроцитов
и
В-лимфоцитов, которые
в
течение какого-то времени обеспечивают
все по-
требности организма
в
клетках крови. Вместе
с тем
такое состояние гемопоэза
у
подавляющего большинства больных
с ХМЛ
сохраняется недолго.
В
ходе
про-
грессирования заболевания, тесно связанного
с
дальнейшим усложнением
ка-
риотипа РЫ-позитивных клеток, верховенство
в
гемопоэзе получают злокачест-
венные
клоны клеток, которые
в
значительной мере утрачивают свой исходный
дифференцировочный
потенциал,
что
проявляется присоединением анемии,
тромбоцитопении,
а
также формированием очагов экстрамедуллярного крове-
творения
в
селезенке, лимфоузлах, коже
и т. д.
Клиническая картина.
Традиционное описание хронического миелолейко-
за включает несколько стадий,
или
фаз. Большинство наблюдаемых врачами
па-
циентов
находятся
в
хронической,
или
стабильной, стадии, средняя продолжи-
тельность которой равняется
3~-4
годам. Далее хроническая стадия болезни
трансформируется
в
фазу акселерации
и
бластный
криз.
У
большинства больных
хронический миелолейкоз начинается исподволь.
В
некоторых случаях
он мо-
жет быть диагностирован
по
анализу крови, сделанному
на
фоне полного сома-
тического благополучия.
Другие
пациенты
могут
предъявлять жалобы
на сла-
бость, недомогание, снижение массы тела, отсутствие аппетита, повышенную

m
morn,
no
ночам
или
иметь симптомы,
обусловленные
увеличением разме-
рим
i
елезенки (раннее насыщение, боли
и (или)
наличие опухолевой массы
в ле-
пим
верхней половине живота). Менее характерны тромбозы
и
кровотечения,
стланные
с
дисфункцией гранулоцитов
и
тромбоцитов. Реже
на
первый план
выступают проявления лейкостаза
или
высокого тромбоцитоза: сосудистые
Громбозы, цереброваскулярные нарушения, инфаркты, тромбозы вен, приапизм,
и.фушения
зрения
или
функций головного мозга
с
головной болью, затормо-
i
пшосгью
и
потерей ориентации
в
окружающем, дыхательная недостаточность.
I
Ыконец,
у
части пациентов дебютом заболевания может стать острый лейкоз
со
Ктми
связанными
с ним
проявлениями.
Клиническая
картина хронической стадии
у
большинства больных
с ХМЛ
I
(одна.
Она
характеризуется постепенно нарастающим нейтрофильным лейко-
цитозом
со
сдвигом влево лейкоцитарной формулы разной степени выраженно-
i
HI
(вплоть
до
промиелоцитов
и
единичных бластов), увеличением количества
мнинофилов,
базофилов
и
тромбоцитов, большим количеством клеток
в
кост-
ном
мозге
и
спленомегалией.
Основными
критериями фазы акселерации,
по
данным ВОЗ, являются:
бла-
,
и,, - Ю—19 %,
базофилы
> 20 %, не
связанная
с
терапией тромбоцитопения
ЮОхЮул, наличие клоновой эволюции кариотипа (вторая Рг^-хромосома,
тртомия
8,
изохромосома
по
длинному плечу
17 и т. д.),
неконтролируемый
г|м)мбоцитоз
>1000
х 10
9
/л и
фиброз КМ
со
скоплениями мегакариоцитов.
Терминальная
стадия,
или
бластный криз ХМЛ, может протекать по-разно-
му. Обычно
в
клинической картине доминируют резкая слабость, длительные
моющие,
а
иногда
и
очень сильные боли
в
костях
и
суставах,
периодическое
по-
ш.имение
температуры тела
до
38—39
°С,
сопровождающееся ознобом, пролив-
ными
потами
и
снижением массы тела. Как правило,
на
этой стадии происходит
быстрое увеличение размеров селезенки, осложняющееся
ее
инфарктом,
и
пече-
ни
Налицо тяжелый геморрагический диатез. Гематологические проявления
поминальной
стадии
ХМЛ у
80—85
%
больных представлены увеличением
со-
/(гржания
бластов
в
костном мозге
и (или) в
крови выше
30 %. При
этом отме-
ченных выше клинических проявлений хронической стадии заболевания
в
тече-
ии1'
1—2 лет
может
и не
быть.
Таким
образом, мысль
о
возможности наличия
у
больного хронического
мпслолейкоза должна возникать
у
врача
при
обнаружении
в
крови немотивиро-
II,итого
нейтрофильного лейкоцитоза
с
разной степенью выраженности омоло-
мния
лейкоцитарной формулы.
Это
нередко сопровождается увеличением
в
крови
содержания базофилов
и
эозинофилов. Другим важным клиническим
признаком
ХМЛ
можно считать увеличение размеров селезенки.
Лабораторные данные. Количество лейкоцитов
в
крови нелеченых боль-
ных
с ХМЛ
может варьироваться
в
больших пределах
и
нередко превышать
I
(Ю-300
х
10
9
/л.
Лейкоцитарная формула выявляет гранулоцитарные элементы
Всех
стадий созревания, сочетающиеся
с
базофилией
и,
реже,
с
эозинофилией.
v половины больных
с
хронической стадией
ХМЛ,
наряду
с
нейтрофильным
'и-йкоцитозом,
может наблюдаться тромбоцитоз.
При
этом тромботические
ос-
нижнения,
в
отличие
от
истинной полицитемии
и
эссенциальной тромбоците-
мии,
встречаются очень редко.
С
другой
стороны, тромбоцитопения
на
ранней
• гадии заболевания встречается лишь
у 10 %
больных.
Что
касается умеренной
•шемии,
она
может быть представлена
уже в
хронической стадии
ХМЛ.

Костный мозг
больных
с ХМЛ
богат клеточными элементами.
Подавляющи
часть
их
представлена миелоцитами
и
зрелыми нейтрофилами
(см. цв. вкл.,
рис.
9.7).
Из-за этого соотношение миелоидных
и
эритроидных клеток
реэкш
сдвинуто
в
сторону первых
(10—30
: 1).
Процентное содержание бластных
эле-
ментов
в
костном мозге больных
с
хронической стадией
ХМЛ не
превышает
10
%.
Созревание миелоидных элементов практически
не
нарушено,
а
какие-ли-
бо черты дисплазии
не
представлены. Может регистрироваться абсолютный
мо-
ноцитоз,
хотя доля моноцитов
не
превышает
3 %.
Количество мегакариоцитов
в
костном мозге может быть увеличено. Часть
из них с
чертами дисплазии,
в ча-
стности
с
гиполобулярными ядрами. Могут встречаться ложные клетки Гоше
и
видоизмененные гистиоциты. Трепанобиопсия подтверждает наличие
в
костном
мозге миелоидной гиперплазии
и
избыточное выпадение ретикулиновых воло-
кон.
Вместе
с тем
умеренный
или
тяжелый миелофиброз встречается нечасто.
Цитохимическое исследование,
как
правило, обнаруживает низкое содержа-
ние
щелочной фосфатазы
в
нейтрофилах. Между
тем на
фоне терапии, присо-
единения
инфекции,
а
также
на
этапе прогрессирования заболевания этот пока-
затель может повышаться.
Биохимическое исследование крови обнаруживает повышенное содержание
лактатдегидрогеназы, мочевой кислоты, витамина
В
12
и
транскобаламина. Хотя
клинические
проявления нарушения
в
системе гемостаза
у
больных
с
хрониче-
скими
стадиями ХМЛ встречается редко, при лабораторном исследовании может
быть зарегистрировано существенное удлинение тромбопластинового времени.
У пациентов
с
продвинутыми стадиями
ХМЛ
могут
отмечаться анемия, тромбо-
цитопения,
увеличение содержания
в
крови базофилов
и
бластов.
В
терминаль-
ной
стадии заболевания
(при
бластном кризе ХМЛ) содержание бластов
в
кост-
ном
мозге, селезенке,
а
затем
и в
крови нарастает
до 30 % и
более
(см. цв. вкл.,
рис.
9.8),
причем
по
своей природе
они
могут
быть
не
только миелоидными,
но
и
лимфоидными
и
бифенотипическими.
Цитогенетические исследования у
подавляющего большинства больных
с
ХМЛ
обнаруживают классическую реципрокную транслокацию генетического
материала дистальных отделов длинных плеч
9 и 22-й
хромосом
—
t(9;22)
(q34;qll).
В
результате
этой транслокации BCR-ABL-позитивными становятся
гранулоциты, эритроидные клетки, моноциты
и
мегакариоциты. Хотя лимфоид-
ные
клетки вовлекаются
в
этот патологический процесс редко,
у 25 %
больных
постоянно
обнаруживают
Ph
+
В-лимфоциты,
а у
некоторых
из них — и Ph*
Т-лимфоциты.
В то же
время наличие
у
некоторых пациентов
с ХМЛ Ph
+
эндо-
телиальных клеток свидетельствует
о том, что
указанная мутация возникла
как
минимум
на
уровне ранней стволовой гемопоэтической клетки. Здесь необходи-
мо отметить,
что у 5 %
больных
с ХМЛ
отмеченная выше хромосомная поломка
может отсутствовать
или
быть вариантной,
т. е.
затрагивать иную,
чем 9-я, до-
норскую хромосому.
При
этом характерная
для
данной транслокации поломка
генов
ABL и
BCR
у
большинства Ph
1
-негативных пациентов обнаруживается
ме-
тодами
FISH
и (или)
ПЦР. Немаловажно
и то, что
основные клинические прояв-
ления,
так же как
ответ
на
терапию
и
прогноз,
у
этих больных принципиально
не
отличаются
от
таковых
у
«типичных» Ph
1
-позитивных пациентов.
В то же
время отсутствие
в
клетках больных
с ХМЛ
отмеченного выше молекулярного
дефекта больше свойственно пожилым пациентам, имеющим более выраженную
тромбоцитопению, моноцитоз, наличие очагов экстрамедуллярного кроветворе-

мин.
но
низкую базофилию
и лейкоцитоз.
Другими особенностями клинического
и'Инин
этого варианта
ХМЛ
являются ранняя трансформация заболевания
в
ф«
iv
акселерации
и
бластный
криз,
что,
естественно,
ухудшает
прогноз,
по
срав-
нению
с
классической РЫ-позитивной лейкемией.
v (юльшинства больных
с
продвинутыми стадиями ХМЛ,
в
дополнение
к ти-
пичном
Ph'-хромосоме, обнаруживаются дополнительные изменения хромосом,
i
пторые включают:
а)
дупликацию РЫ-хромосомы;
б)
изохромосому
по
длин-
ному плечу хромосомы
17; в)
трисомию
8; г)
трисомию
19; д)
другие
менее часто
in
грсчающиеся хромосомные поломки.
Настоящим
откровением современной цитогенетики
ХМЛ
стало
то, что вы-
пиленные
при
этом лейкозе изменения генома обнаружили четкий молекуляр-
К<1
цитогенетический полиморфизм.
В
частности,
у 20 %
обследованных стан-
i
|ртная транслокация
t(9;22)(q34;qll)
была осложнена делецией
в
маркерной
Хромосоме
9q+
части важных генов хромосом
9-й и (или) 22-й
пар,
что
ассоции-
ровалось
с
плохим прогнозом (Домрачева
Е. В. [и
др.],
2005).
Диагностика и дифференциальная диагностика.
Таким образом, мысль
и
11п;шожности развития
у
больного хронического миелолейкоза должна возни-
i
т. у
врача
при
обнаружении
в
крови немотивированного нейтрофильного
лейкоцитоза
с
разной степенью выраженности омоложения лейкоцитарной
фор-
Иулы.
Это
нередко сопровождается увеличением
в
крови содержания базофилов
И
ш.шнофилов.
Другим
важным клиническим признаком
ХМЛ
можно считать
уигличение размеров селезенки.
Для
подтверждения диагноза важно выявить
шпкое
содержание щелочной фосфатазы
в
нейтрофилах
и
отмеченные выше
из-
менения
хромосом.
В
случае
отсутствия видимых
под
микроскопом изменений
i
i|
и
ютипа оправдано молекулярно-биологическое исследование
на
предмет
вы-
пи
пения специфических перестроек генов
ABL и BCR.
Дифференциальную диагностику
ХМЛ
проводят,
с
одной стороны,
с
лейке-
моилными реакциями костного мозга
в
ответ
на
инфекцию
и
опухоли,
с дру-
гой
— с
иными видами миелопролиферативных заболеваний,
в
частности
i
пдиопатическим миелофиброзом, эссенциальной тромбоцитемией, хрониче-
i
ким
нейтрофильным
и
хроническим миеломоноцитарным лейкозами.
Что
каса-
ется анализов крови
и
костного мозга пациентов
с
бластным кризом
ХМЛ, они,
прежде всего, напоминают таковые
при
острых лейкозах.
В отличие
от
лейкемоидных реакций,
у
больных
с ХМЛ
степень омоложения
лейкоцитарной формулы (сдвиг влево) может быть выражена сильнее
— до мие-
1итов, промиелоцитов
и
даже
бластов. Содержание щелочной фосфатазы
м нейтрофилах,
как
правило, низкое,
а
кариотип лейкозных клеток содержит
ти-
пичную Ph
1
-хромосому.
Наличие
у
больных
с
идиопатическим миелофиброзом выраженного лейко-
цитоза
и
немотивированного сдвига лейкоцитарной формулы влево сочетается
i
наличием
в
крови каплевидных эритроцитов
и
нормобластов,
с
более доброка-
чественным течением заболевания, ранней спленомегалией
и
бедным пунктатом
ынтного мозга.
В
отличие
от ХМЛ,
концентрация щелочной фосфатазы
в ней-
Грофилах
крови больных
с ИМ
повышена,
а
тестирование клеток
на
РгЛхро-
мосому
дает
негативные результаты.
Наконец,
в
трепанатах костного мозга этих
больных
обнаруживают
не
свойственный
ХМЛ
выраженный коллагеновый
фиброз.

Содержание тромбоцитов в крови у 10 % больных с ХМЛ может быть
сувд
ственно повышено, что
диктует
необходимость дифференцировать данное забо
левание с эссенциальной тромбоцитемией. Решающими признаками при разгр!
ничении
этих заболеваний являются свойственные ЭТ очень высокие тромбоцп
тозы (более 1—2 х
10
12
/л)
при отсутствии в крови выраженного нейтрофильногм
лейкоцитоза, низкого содержания щелочной фосфатазы в нейтрофилах крови и
РЫ-хромосомы.
Создается впечатление, что редко встречающийся хронический нейтрофиль
ный
лейкоз протекает доброкачественнее, чем ХМЛ. При этом степень выражен
ности омоложения лейкоцитарной формулы минимальная, концентрация ще
лочной фосфатазы в нейтрофилах нормальная или высокая, в то время как
РЬ^хромосома в
опухолевых
элементах не представлена.
Главным отличительным признаком хронического миеломоноцитарного
лейкоза является абсолютный моноцитоз (более 1 х 10
9
/л), а не характерная для
ХМЛ эозинофильно-базофильная ассоциация. Кроме того, в патологических
элементах больных с ХММЛ
отсутствуют
характерные для ХМЛ изменения ка-
риотипа, в частности Рп^хромосома.
При
классическом стадийном течении ХМЛ разграничение бластного криза
и
острых лейкозов трудностей не вызывает. Главным аргументом при проведе-
нии
дифференциальной диагностики выступает сам факт формирования бласт-
ного криза на фоне предшествующих ему хронических стадий заболевания, а
также наличие в клетках больных с острыми лейкозами
других,
чем Рп^хромо-
сома, изменений кариотипа, например t(8;21), t(15;17),
t(9;ll)
и т. д. Ситуация
существенно осложняется, когда бластный криз становится дебютом ХМЛ.
В этом
случае
отграничение ХМЛ от РЫ-позитивных острых лимфобластных и
бифенотипических лейкозов строится по
результатам
проведенной терапии.
Дело в том, что при достижении полной клинико-гематологической ремиссии
у больных с острыми лейкозами РЫ-хромосома исчезает, а при ХМЛ остается во
всех
созревающих патологических элементах. Кроме того, в
ходе
успешной тера-
пии
бластного криза у таких пациентов
могут
появиться изменения крови и ко-
стного мозга, характерные для хронической стадии ХМЛ, что не свойственно
Ph
1
-позитивным
острым лейкозам.
Лечение хронического миелолейкоза начинается сразу после постановки ди-
агноза. При наличии в крови высокого нейтрофильного лейкоцитоза показана
терапия препаратами гидроксимочевины в комбинации с аллопуринолом. Если
лейкоцитоза нет или он нормализован с помощью гидроксимочевины, то пока-
зан
гливек, а при его отсутствии — длительный (до
года
и более) курс терапии
ИФ-а
в дозе 3—6 млн ME 6 раз в неделю, дополняемый при необходимости пе-
риодическими курсами малых доз цитозара. В
случае
прогрессирования заболе-
вания,
в том числе на фоне приема достаточных доз гливека, показана транс-
плантация
костного мозга.
История
использования гидроксимочевины (гидреа) и бусульфана (миелоса-
на) для лечения ХМЛ насчитывает полвека. Накопленный опыт показал, что та-
кая
терапия на какое-то время позволяла эффективно снижать лейкоцитоз и
уменьшать количество опухолевой массы. Однако достигаемая у небольшого
числа пациентов клинико-гематологическая ремиссия (т. е. нормализация
всех
показателей периферической крови,
отсутствие
спленомегалии или
других
экст-
рамедуллярных очагов) оказалась нестойкой. Выживаемость больных с хрони-

Phenylaminopyrimidine
Рис.
9.9.
Химическая формула гливека (STI571)
чй стадией ХМЛ на фоне такой терапии в среднем равнялась 3—5 годам,
it it фазе акселерации и бластного криза -
даже
нескольким месяцам.
Крупным событием в лечении ХМЛ стало появление в
1980-х
гг. препаратов
нн11|)ферона, применение которых позволяло достичь клинико-гематологиче-
•
Кий ремиссии у
50—80
% больных, а у 8—15 % из них — с полным цитогенети-
•III
ким ответом. Хотя молекулярный
ответ
на терапию интерфероном достигал-
райне редко, общая продолжительность жизни больных стала больше.
оы.пно
лечение интерфероном начинали в дозе 1 мМЕ/сут, а затем в течение
1
3 недель
дозу
повышали до стандартной, т. е. 5 мМЕ/м
2
в сутки. Одним из не-
Востатков терапии интерфероном были многочисленные побочные эффекты, в
том числе гриппоподобный синдром, гематологическая токсичность, снижение
м.и сы
тела,
депрессия и психастения, развитие аутоиммунных заболеваний и др.
v рила больных интерферон назначался в сочетании с малыми дозами цитозара,
что делало терапию еще более токсичной.
Принципиально
новым подходом лечения ХМЛ стало использование инги-
ьмюров тирозинкиназной активности
BCR-ABL.
Первым препаратом этой груп-
пы
был иматиниб мезилат — гливек (рис. 9.9). Благодаря присоединению
и ЛТФ-связывающей части химерной тирозин-киназы (рис.
9.10),
он блокирует
I'm.
9.10.
Молекулярный механизм действия гливека, связанный
с
блокированием процесса
фш
форилирования тирозина
и
выключения основных сигнальных путей действия
в
клетке
патологического гена BCR-ABL

фосфорилирование
целого ряда субстратов и передачу отмеченных выше сиена
лов,
приводящих к лейкозной трансформации клетки (см. рис. 9.3). Поскольку
иматиниб
оказывает антипролиферативное и проапоптотическое влияние к|
лейкемические клетки и практически не
действует
на нормальные аналоги, пи
является высокоэффективным препаратом для лечения как больных в раннем
хронической фазе ХМЛ, так и пациентов, ранее получавших терапию интерфе-
роном
или интерфероном в сочетании с цитозаром.
Накопленный
опыт показал, что в хронической фазе заболевания клили
ко-гематологическую ремиссию с помощью гливека можно получить у 95
"<>
больных, а после 12 месяцев постоянной терапии в 60 % случаев достигается и
полный
цитогенетический ответ. Большой молекулярный ответ удается полу
чить у 63 % больных, а полный молекулярный ответ — у 28 %, что с помощью
всех используемых прежде режимов было недостижимо. В итоге 5-летняя выжм
ваемость больных с ХМЛ на фоне терапии гливеком достигла 95 %. При этом
было
показано,
что
более
раннее
достижение полного ЦГО сопровождается бо-
лее длительной безрецидивной заболеваемостью по сравнению с такокой
у больных без ЦГО (93 и 65 % к 12 месяцам терапии соответственно). Совре
менные
критерии цитогенетического и молекулярно-биологического ответов u.i
применение
гливека представлены ниже (табл. 9.1 и 9.2).
Кроме
того, было показано, что безрецидивная выживаемость существенно
увеличивается при наличии у больных большого молекулярного
ответа
на
фоне
полного ЦГО (93 % против 67 %) и уменьшается риск потери ЦГО до 2—5 %
(против
35 % у больных без большого МО на фоне ПЦГО).
Следует
также отме
тить, что возможность сохранения полного ЦГО на фоне терапии гливеком за
висит от длительности заболевания и предшествующей терапии. Чем больше
Таблица
9.1
Критерии
цитогенетического
ответа
на
применение
гливека
при
хроническом
миелолейкозе
Вид
цитогенетического
ответа
Полный
Частичный
Малый
Минимальный
Нет
ответа
Число
Ph-позитивных
метафаэ, %
0
1—35
35—65
65—95
100
Таблица
9.2
Критерии
молекулярно-биологического
ответа
на
применение
гливека
при
хроническом
миелолейкозе
Вид
молекулярного
ответа
Большой
молекулярный
ответ
Полный
молекулярный
ответ
Критерии
молекулярного
ответа
(уровень
BCR-ABL
транскрипта
по ПЦР)
Редукция
BCR -ABL более чем в
1000
раз {> 3 log) или со-
отношение
BCR-A8L/ABL < 0,05 %
Отсутствие
химерного
транскрилта
BCR-ABL по данным
ПЦР
