Мамаев Н.Н. Гематология: руководство для врачей
Подождите немного. Документ загружается.


I
t
развитием соврмпиньга молекулярио-биологических
методов
станет
воз
ожным изучение маркеров,
позволяющих предсказать течение
ОМЛ,
на
осно-
IIIIIMI
анализа экспрессии различных генов (micro array technology).
В
связи с тем, что
ФАБ-классификация
в
течение многих
лет
являлась доми-
нирующей
в
диагностике острых лейкозов, основные выводы
при
оценке
эффек-
гипмости
химиотерапии
и
ТГСК
у
больных
с ОМЛ
сделаны
на ее
основе.
Как
Ирпиило,
М0-М2
и
М4-М7 варианты
ОМЛ
требуют
проведения консолидации
ремиссии с
помощью высокодозной химиотерапии,
в том
числе выполнением
|)
го
ТГСК/алло-ТТСК,
на
одном
из
этапов программного лечения. Исключение
составляет острый промиелоцитарный лейкоз (МЗ), когда комбинация диффг
рпщировочной (ретиноиды)
и
цитостатическои терапии приводит
к
излечении»
Вибо
длительной ремиссии
у
большинства больных.
Тип
предполагаемой трансплантации зависит
от
наличия донора
ГСК, ВО|-
раста
больного, стадии заболевания, стратегии работы центра трансплантации
и
IT»
участия
в
кооперативных исследованиях
по
выбору оптимальных программ
Ирапии ОМЛ.
При
этом возможно применение ауто-ТГСК, алло-ТГСК
от
родственного
и
неродственного донора
ГСК с
различной степенью совместимости
по
HLA-сиг
теме (совместимого, частично совместимого, гаплоидентичного)
с
использова-
нием
миелоаблативного режима кондиционирования
или
режимов
с
уменьшен
мой интенсивностью дозы.
Оценка
эффективности различных типов ТГСК
при ОМЛ
выполнена CIBMTK
И
основании информации
о
тысячах трансплантаций, ежегодно поступающей
из
центров, зарегистрированных
в
этой организации (около
1000
центров).
Аутологичная
трансплантация гемопоэтических стволовых клеток.
Но
результатам
CIBMTR, 3-летняя общая выживаемость после ауто-ТГСК
у больных
с ОМЛ в
первой
ПР
равна
55 %, во
второй
ПР — 35 %, при
выполпг
нии
трансплантации
в
рецидиве
— 18 % (рис. 16.4)
Необходимо отметить,
что в
настоящее время мнение
об
эффективности
ауто-ТГСК
при ОМЛ
неоднозначно, поскольку
ее
результаты
часто сопоставимы
со стандартными протоколами химиотерапии
или
превышают
их
незначитель-
100
#
80
л
§
60
x
|
40
&
<v
ад
20
0
_
p
=
0,0001
Ремиссия
не
получена
(и » 29)
0
12 3 4 5 6
Количество
лет
после трансплантации
Рис.
16А.
Общая выживаемость после аутологичной трансплантации гемопоэтических стволо-
вых клеток
у
больных старше
20 лет с
острым миелобластным лейкозом
в
зависимости
от стадии заболевания
(1994—1999)
но.
Применение современных программ химиотерапии
при ОМЛ позволяет Л
тичь
5-летней
безрецидивной выживаемости
у
25-50
% взрослых, у 60 Ж)
детей, однако риск развития рецидива
при
этом составляет
25—80
%.
Высокая вероятность развития рецидива также является основным
фак1
ром,
лимитирующим широкое применение ауто-ТГСК
при ОМЛ. Это свящ
с невозможностью полной эрадикации злокачественного клона клеток H:I
Х<К
ного мозга
при
проведений химиотерапии
и
неминуемым присутствием
•
клеток
в
аутологичном трансплантате.
Аргументом
в
пользу проведения
аут
ТГСК
при ОМЛ у
взрослых является наличие возможности
для
пациента
HOCJ
трансплантации полностью отказаться
от
длительной поддерживающей тераш
и
достаточно быстро реабилитироваться вплоть
до
полного восстановления тру\
доспособности.
Применение
ауто-ТГСК
при ОМЛ у
детей
не
является общепринятым
и ocjl
ществляется
при
невозможности использования алло-ТГСК
в
центрах, изучаю-
щих различные аспекты этого метода лечения (внедрение новых режимов
KOHJ
диционирования,
влияние
«очистки»
аутологичного трансплантата
от
примет
злокачественных клеток).
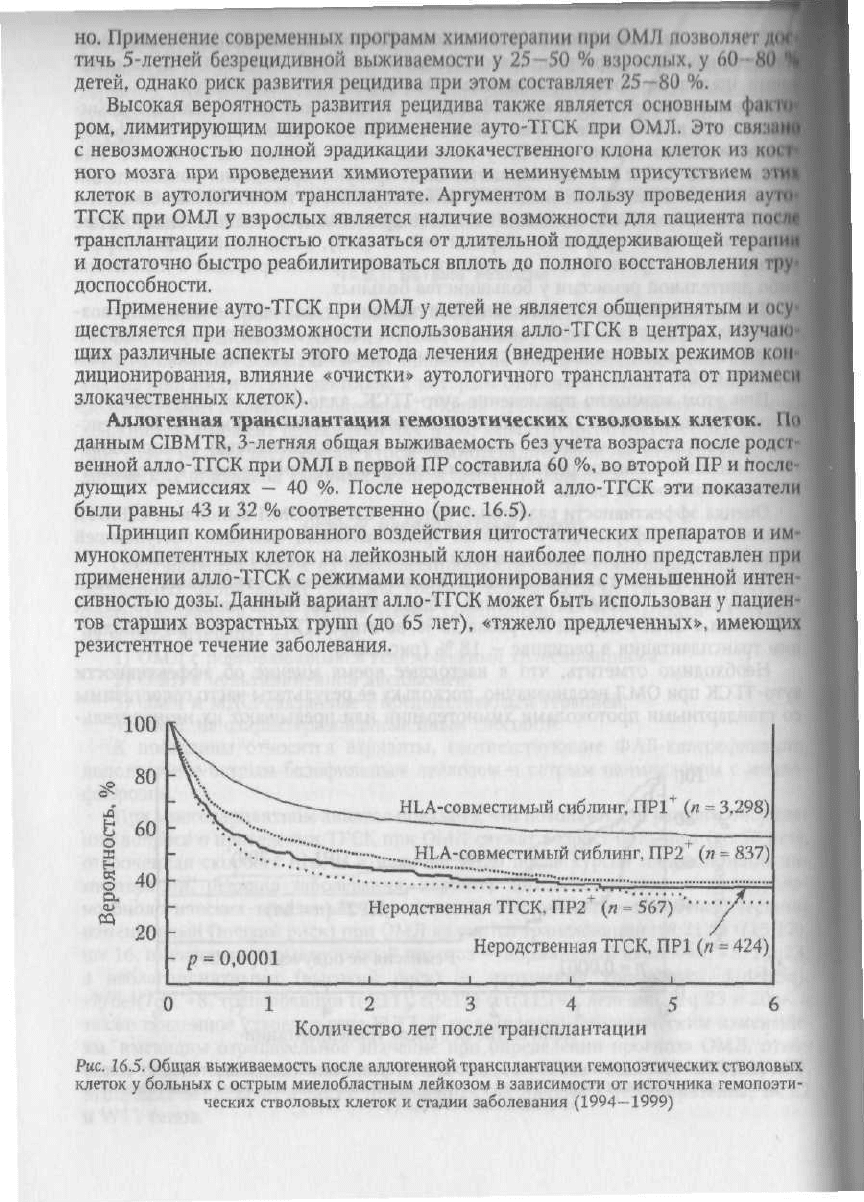
Аллогенная трансплантация гемопоэтических стволовых клеток. По
данным CIBMTR, 3-летняя общая выживаемость
без
учета
возраста после родст-
венной
алло-ТГСК
при
ОМЛ
в
первой ПР составила
60 %, во
второй
ПР и
После
дующих
ремиссиях
— 40 %.
После неродственной алло-ТГСК
эти
показатели
были равны
43 и 32 %
соответственно
(рис.
16.5),
Принцип
комбинированного воздействия цитостатических препаратов
и им-
мунокомпетентных клеток
на
лейкозный клон наиболее полно представлен
при
применении
алло-ТГСК
с
режимами кондиционирования
с
уменьшенной интен-
сивностью дозы. Данный вариант алло-ТГСК может быть использован
у
пациен-
тов старших возрастных групп
(до 65 лет),
«тяжело
предлеченных», имеющих
резистентное течение заболевания.
100
80
g
о
к
с
о
а,
а>
ОД
60
40
20
-
р
=
0,0001
0
HLA-совместимый сиблинг,
ПР1
(л
= 3,298)
HLA-совместимый сиблинг,
ПР2
(л
• 837)
Неродственная ТГСК,
ПР2
(«-567)
•••••/••••
Неродственная ТГСК,
ПР1
(п
= 424)
12
3 4 5
Количество
лет
после трансплантации
Рис. 16.S. Общая выживаемость после аллогенной трансплантации гемопоэтических
стволовых
клеток
у
больных
с
острым миелобластным лейкозом
в
зависимости
от
источника гемопоэти-
ческих
стволовых
клеток
и
стадии заболевания
(1994-1999)

При
imi
гановке
днагноим они
не
возникает
необходимости рассматривать
•
дение ТГСК.
Прогресс
и герапии
мои»
заболевания, снизанный
с
внедре-
•
it
клиническую практику препаратов
из
группы ретиноевой кислоты
(nil
п.иг,
u'tinoid acid
ATRA) и мышьяка
(arsenic
trioxide
-
Trisenox), позво-
нзлечить
70-80
%
больных.
Тем не
менее,
у 20 %
пациентов
с ОПЛ воз-
им
[Н'цидивы заболевания,
что
существенно изменяет прогноз. Достижение
ни
ИР при ОПЛ
возможно
с
использованием
тех же
препаратов, однако
>м
случае
применение алло-ТГСК может быть обосновано. Пятилетняя
без-
|нцидпиная
выживаемость больных
с ОПЛ
после алло-ТГСК
во
второй
ПР со-
чил
57 %.
Ауто-ТГСК
при
ОПЛ
не
имеет преимуществ
по
сравнению
со
стан-
i
ipinoii химиотерапией.
Острый
лимфоблзстный
лейкоз
У
75-85
%
взрослых
с ОЛЛ
возможно получение полной ремиссии
при ис-
нпш,:ювании
современных протоколов химиотерапии, однако 3-5-летняя безре-
цидивная
выживаемость
при
этом составляет
30-45
%.
В отличие
от
взрослых,
у
детей химиотерапия является чрезвычайно
эффек-
Гивным
и,
несомненно, основным методом лечения
ОЛЛ,
поскольку 5-летияя
' "^рецидивная выживаемость
у них
составляет
80-90
%.
Несмотря
на
отсутствие
удовлетворяющих
результатов
применения химио-
терапии
у
взрослых
и
выдающиеся
результаты
у
детей, продолжаются многочис-
ленные дискуссии относительно необходимости
и
сроков выполнения
Т1Ш/ТПСКК
(аутологичной, аллогенной)
при ОЛЛ у
данной категории боль-
ных.
Аргументами
в
пользу более осторожного
подхода
являются следующие
обстоятельства: высокая частота рецидивирования
ОЛЛ
после высокодозной
хи-
мио/лучевой терапии
с
ТГСК,
отсутствие
явных преимуществ
при
оценке
отда-
ленных
результатов
по
сравнению
со
стандартной химиотерапией
(в
первую
очередь, после ауто-ТГСК)
и
высокая вероятность развития тяжелых,
в том чис-
ле несовместимых
с
жизнью, осложнений (особенно после алло-ТГСК).
В настоящее время степень интенсивности предполагаемой цитостатической
терапии
при
постановке диагноза
ОЛЛ
выбирается
на
основании риска (стан-
дартный, высокий) заболевания.
Для
определения показаний
к
проведению
од-
ного
из
видов ТГСК
при ОЛЛ
учитываются факторы, влияющие
на
прогноз
и
определяющие возможность назначения больному сверхвысокодозной лучевой
и
цитостатической терапии,
а
именно: возраст, индекс Карновского, количество
лейкоцитов
в
момент постановки диагноза более
100,0 х Ю
9
/л,
цитогенетиче-
ские
изменения
—
t(9;22), t(4;ll), число курсов химиотерапии, необходимых
для достижения первой ПР, иммунологический вариант
ОЛЛ,
наличие призна-
ков
МОБ
при
молекулярно-биологическом исследовании после курсов индукци-
онной
химиотерапии.
Большинство современных протоколов цитостатической терапии
ОЛЛ у
взрос-
лых включает выполнение одного
из
видов ТГСК
в
первой
ПР в
качестве этапа
программного лечения
при
высоком риске
ОЛЛ.
Для детей показаниями
к
проведению алло-ТГСК
в
первой
ПР
являются
на-
личие признаков высокого риска заболевания
в
момент постановки диагноза,
к
которым относится возраст
(до 6
мес), гиперлейкоцитоз
на
момент постанов-
ки
диагноза (более
25-50,0
х
10
9
/л), Т~иммуналогический вариант (Т-ОЛЛ),
филадельфийская хромосома
- Ph
1
',
идентификация
патологического
MLL, гипоплоидия, отсроченное достижение ремиссии
на
фоне
индукциоН!
курса химиотерапии (более
35
дней).
Больные
с
ОЛЛ,
как
взрослые,
так и
дети, находящиеся
в
состоянии
ктороЙ
последующих
ПР,
являются абсолютными кандидатами
для
родственней
щ
неродственной алло-ТГСК.
Аутологичная
трансплантация гемопоэтических стволовых клетц
Применение
ауто-ТГСК
у
взрослых
при ОЛЛ
возможно
в
первой
ПР и
посл(
дующих
ремиссиях,
что
связано
с
отсутствием удовлетворительных
результат!
при
назначении стандартной химиотерапии
и
необходимостью поиска мош.П
направлений лечения.
Применение
ауто-ТГСК
при ОЛЛ у
детей может рассматриваться только
случае
наличия комбинации неблагоприятных прогностических факторок
и
в
отсутствии какой-либо возможности проведения одного
из
видов алло-ТГС1
(родственной, неродственной).
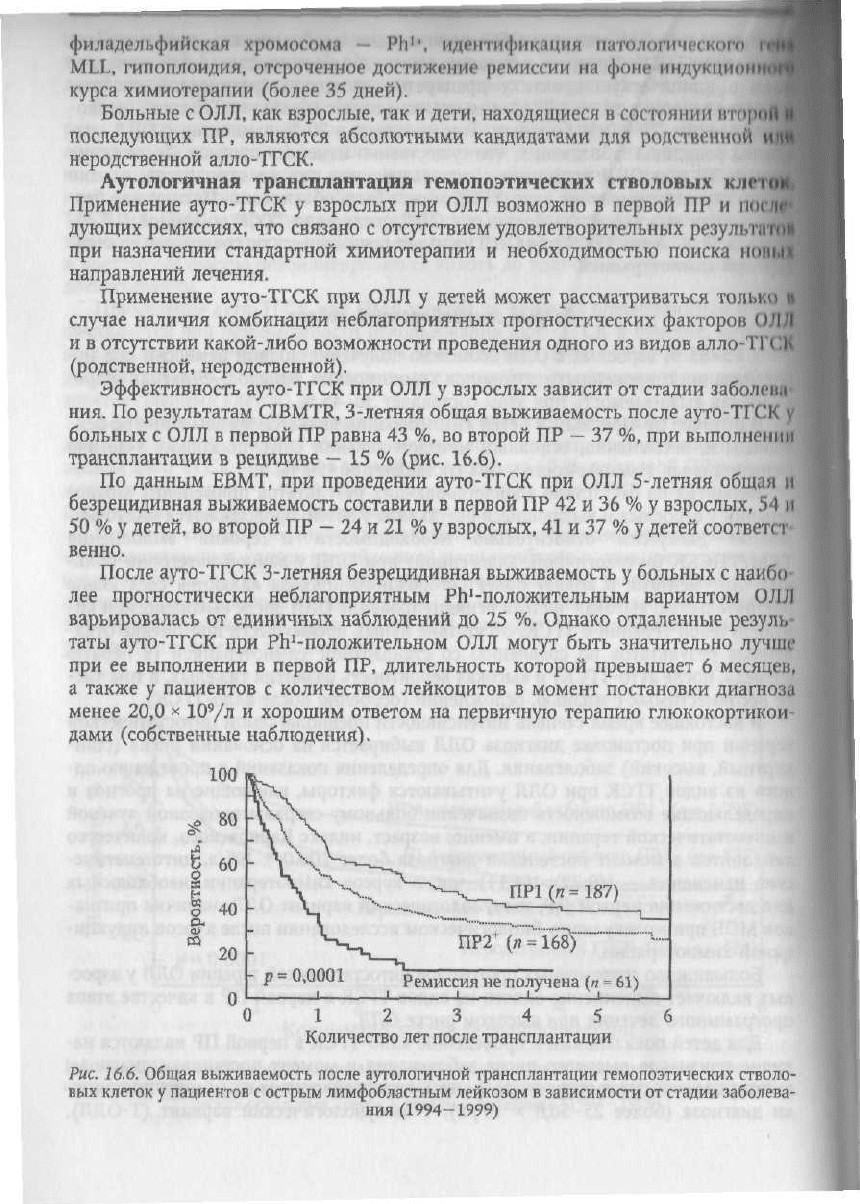
Эффективность ауто-ТГСК
при ОЛЛ у
взрослых зависит
от
стадии заболит
ния.
По
результатам
CIBMTR, 3-летняя общая выживаемость после ауто-ТГСК
больных
с ОЛЛ в
первой
ПР
равна
43 %, во
второй
ПР — 37 %, при
выполнен!и
трансплантации
в
рецидиве
— 15 % (рис.
16.6).
По
данным ЕВМТ,
при
проведении ауто-ТГСК
при ОЛЛ
5-летняя общая
и
безрецидивная выживаемость составили
в
первой
ПР 42 и 36 % у
взрослых,
54 и
50
% у
детей,
во
второй
ПР — 24 и 21 % у
взрослых,
41 и 37 % у
детей соответп-
венно.
После ауто-ТГСК 3-летняя безрецидивная выживаемость
у
больных
с
наибо-
лее прогностически неблагоприятным РЫ-положительным вариантом
ОЛЯ
варьировалась
от
единичных наблюдений
до 25 %.
Однако отдаленные резуль-
таты ауто-ТГСК
при
Ph
1
-положительном
ОЛЛ
могут
быть значительно
лучше
при
ее
выполнении
в
первой
ПР,
длительность которой превышает
6
месяцев,
а также
у
пациентов
с
количеством лейкоцитов
в
момент постановки диагноза
менее
20,0 * 10
9
/л и
хорошим ответом
на
первичную терапию глюкокортикои-
дами (собственные наблюдения).
100
80
g
60
g
I
40
OJ
20
0
т
0,0001
Ремиссия
не
получена
(л
=
61)
12
3 4 5
Количество
лет
после трансплантации
Рис.
16.6.
Общая выживаемость после аутологичной трансплантации гемопоэтических стволо-
вых клеток
у
пациентов
с
острым лимфобластным лейкозом
в
зависимости
от
стадии заболева-
ния
(1994-1999)

Риск
возникновения рецидии
пе
ауто
I тек мри
олл
коррелирует
с
ре-
|уц|.1лглми количественного
определения
методом
1ЩР
признаков МОБ, свиде-
тим.етиунмцих
об отсутствии молекулярно
биологической ремиссии после
ин-
поимой
химиотерапии,
во
время получения
ГСК,
непосредственно перед
трат
плантацией
или
после
ее
проведения. Большая вероятность развития
ран-
1м
ч)
рецидива наблюдается
при
количестве резидуальных бластов выше
10
2
по-
i
м
курса индукции
и
выше 10'
3
на фоне проведения химиотерапии.
Эти
данные
инниются
более значимыми,
чем
иммунофенотипический вариант
ОЛЛ,
возраст
Пациента,
показатель прогноза
и
число лейкоцитов
в
момент постановки диаг-
цоза.
Таким
образом, ауто-ТГСК
при ОЛЛ у
взрослых
и
детей может быть эффек-
Гивным
методом консолидации ремиссии,
а при
отсутствии родственного
или
неродственного донора
ГСК
рассматриваться
как
альтернативный метод тера-
пии.
Решение
в
пользу
ее
проведения зависит
от
факторов риска
и
стадии забо-
пгнания,
эффективности предшествующей химиотерапии,
а
также стратегии
ра-
боты
центра трансплантации.
Аллогенная трансплантация гемопоэтических стволовых клеток. При
оценке
эффективности алло-ТГСК
у
взрослых
и
детей
с ОЛЛ
имеется очевидная
инисимость
результатов
от
стадии заболевания, возраста, продолжительности
первой
ПР и
ремиссии
до
алло-ТГСК, иммунологического варианта
ОЛЛ,
нали-
•imi прогностически неблагоприятных цитогенетических изменений
и
признаков
МОБ
после курсов индукционной терапии.
Прогностическое значение вышеуказанных параметров является общим
практически
для
всех
вариантов острых лейкозов
при
выполнении ТГСК. Из-за
отсутствия единого мнения
и
результатов, полученных
из
рандомизированных
источников,
продолжаются исследования, направленные
на
сравнение различ-
ных видов алло-ТГСК
у
больных
с ОЛЛ.
По
данным CIBMTR, 3-летняя общая выживаемость после родственной
ал-
ло-ТГСК
при ОЛЛ в
первой
ПР
составила
52 %, во
второй
ПР и
последующих
ремиссиях
— 42 %. Те же
показатели после неродственной алло-ТГСК были
рав-
ны
44 и 33 %
соответственно. Зависимость
результатов
алло-ТГСК
у
больных
с
ОЛЛ
от
возраста, стадии
и
источника
ГСК
(родственный, неродственный донор)
представлена
на рис. 16.7 и 16.8.
Необходимо отметить,
что
алло-ТГСК является абсолютно показанной
при
наиболее прогностически неблагоприятном варианте Рп'-положительного
ОЛЛ
как
у
взрослых,
так и у
детей. Эффективность алло-ТГСК
при
Ph
1
-положитель-
ном
ОЛЛ во
многом зависит
от
стадии заболевания
на
момент выполнения.
Так,
5-летняя общая выживаемость
у
детей
и
взрослых составила
38 %
после выпол-
нения
родственной
и
неродственной алло-ТГСК
в
первой
ПР и 0 % в
последую-
щих ремиссиях. Общая выживаемость
при
данном варианте
ОЛЛ
после
ал-
ло-ТГСК
и
ауто-ТГСК
у
пациентов моложе
30 лет
была равна
62 %, а у
пациен-
тов старше
30 лет — 11 %.
В отличие
от
ОМЛ, алло-ТГСК
с
«немиелоаблативными» режимами конди-
ционирования
при ОЛЛ
используется реже,
что
связано
с
низкой вероятностью
достижения эффекта, обусловленного реакций «трансплантат против лейкоза»
(у
10-15 %
больных).
Тем не
менее
не
исключено,
что в
последующем показа-
ния
к
выполнению данного вида алло-ТГСК
при ОЛЛ
будут
расширены.
100
Ъ
о
X
н
те
о
е\
в
60
40
20
HLA-совместимый сибс, ПР 2* (л • 962)
HLA-совместимый сибс, ПР 1 (л
=
561)
Неродственная ТГСК, ПР 2 (л - 805)
Неродственная ТГСК, ПР 1 (п
=
280)
=
0,0001
0 12 3 4 5 6
Количество лет после трансплантации
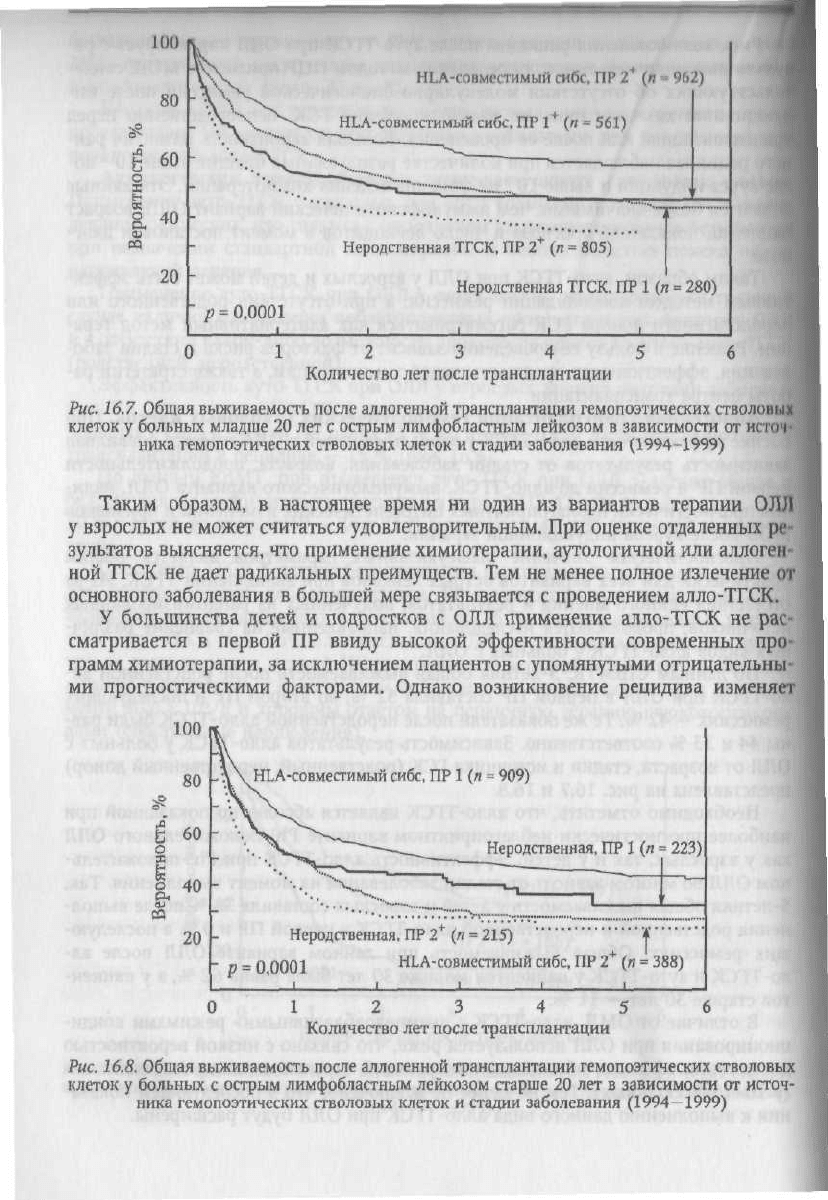
Рис. 16.7. Общая выживаемость после аллогенной трансплантации гемопоэтических стволоных
клеток у больных младше 20 лет с острым лимфобластным лейкозом в зависимости от источ
ника
гемопоэтических
стволовых
клеток и стадии заболевания
(1994-1999)
Таким
образом, в настоящее время ни один из вариантов терапии ОЛЛ
у взрослых не может считаться удовлетворительным. При оценке отдаленных ре-
зультатов
выясняется, что применение химиотерапии, аутологичной или аллоген-
ной
ТГСК не
дает
радикальных преимуществ. Тем не менее полное излечение от
основного заболевания в большей мере связывается с проведением алло-ТГСК.
У большинства
детей
и подростков с ОЛЛ применение алло-ТГСК не рас-
сматривается в первой ПР
ввиду
высокой эффективности современных про-
грамм химиотерапии, за исключением пациентов с упомянутыми отрицательны-
ми
прогностическими факторами. Однако возникновение рецидива изменяет
100
80
60
40
20
HLA-совместимый сибс, ПР 1 (и = 909)
Неродственная, ПР 1 (л = 223)
р =
0,0001
Неродственная, ПР 2
+
(п « 215) '""$
HLA-совместимый сибс, ПР 2
+
(я - 388)
0 12 3 4 5 6
Количество лет после трансплантации
Рис. 16.8, Общая выживаемость после аллогенной трансплантации гемопоэтических
стволовых
клеток у больных с острым лимфобластным лейкозом старше 20 лет в зависимости от источ-
ника
гемопоэтических
стволовых
клеток и стадии заболевания
(1994-1999)

нршшп
течении
ОЛЛ v
деи-ii
и
подростков.
В
этом
случае
показания к
выполне-
нию
одного
из видов алло
TICK
во
второй
и
последующих ремиссиях
у
детей
и
подростков становятся несомненными.
16.9.2.
Миелодиспластические синдромы
Применение
стандартной химиотерапии
при МДС у
взрослых
и
детей,
как
Правило,
не
бывает успешным,
что
делает
алло-ТГСК одним
из
самых эффектив-
ных методов лечения данного заболевания.
Хорошо известно,
что
общая выживаемость
при
МДС
у
взрослых зависит
от
вшраста,
прогноза согласно IPSS (International
Prognosis
Score System), индекса
К.фновского,
морфологического варианта
по ВОЗ или
ФАБ-классификации
и
цмтогенетических изменений
в
момент постановки диагноза.
Эти параметры оказывают влияние
на
сроки постановки вопроса
о
необхо-
димости выполнения алло-ТГСК
от
родственного
или
неродственного донора.
I.с'рецидивная продолжительность жизни больных после алло-ТГСК,
в
зависи-
мости
от
IPSS, колеблется
от 23 до 63 %.
Несмотря
на то, что в
настоящее время определяющей классификацией
МДС
Иляется
классификация, предложенная кооперативной группой
ВОЗ,
основные
результаты
по
эффективности алло-ТГСК
при МДС
представлены ранее выпол-
ненными
исследованиями
с
учетом
ФАБ-классификации.
В зависимости
от
ФАБ-классификации, 3-летняя общая выживаемость после
ллло-ТГСК
при
рефрактерной анемии
и
рефрактерной анемии
с
кольцевыми
си-
деробластами была равна
53 %, при
рефрактерной анемии
с
избытком бластов
(трансформации)
и
хроническом миеломоноцитарном лейкозе
— 36 %.
Основными источниками, свидетельствующими
об
эффективности одного
из
иидов ТГСК, являются публикации
двух
регистров, аккумулирующих информа-
цию
о
ТГСК, выполненных
в
различных центрах мира. Так,
по
данным CIBMTR,
3-летняя общая выживаемость после родственной алло-ТГСК
у
больных
с МДС
в
возрасте
от 2 до 64 лет
составила
42 %,
безрецидивная выживаемость
— 40 %,
смертность, непосредственно связанная
с
алло-ТГСК,
— 37 %. При
выполне-
нии
неродственной алло-ТГСК 3-летняя общая выживаемость
при МДС
была
равна
23 %.
По
данным ЕВМТ, 3-летняя общая выживаемость
при
МДС после родственной
алло-ТГСК составила
36 %, а
после алло-ТГСК
от
неродственного донора
— 25 %.
Возможно,
что эти
результаты
могут
показаться неубедительными, посколь-
ку выживаемость пациентов редко превышает
50 %. Тем не
менее, оценивая
их,
необходимо учитывать,
что
только
25 %
больных
с МДС
находятся
в
возрасте
до
60 лет на
момент постановки диагноза,
что
существенно повышает смерт-
ность, связанную
с
осложнениями раннего периода после алло-ТГСК.
Полученные данные
свидетельствуют
об
эффективности родственной
и
неродственной алло-ТГСК
у
больных
с
МДС. Поэтому применение алло-ТГСК
при
МДС является
не
только оправданным,
но и
должно обсуждаться
с
момента
постановки диагноза,
что
связано
с
отсутствием альтернативных алло-ТГСК эф-
фективных методов лечения данного заболевания.
До сих пор
пациенты
с
МДС,
не
получившие алло-ТГСК, имеют плохой прогноз
при
долгосрочной оценке
об-
щей
и
безрецидивной выживаемости.

DUU V
Внедрение режимов кондиционироилмин с уменьшенной шпгнсинн
дозы у больных с МДС представляется наиболее обоснованным. Это обуслови
но
тем, что терапия МДС может быть наиболее эффективна при сочетании «я1
миелоаблативного» цитостатического эффекта с иммунологической реакция
«трансплантат против лейкоза». Это обстоятельство также позволяет увеличив
возрастной диапазон применения алло-ТГСК за счет уменьшения токсичносЛ
связанной
с трансплантацией и наличием сопутствующих заболеваний.
С
особым вниманием рассматривается эффективность алло-ТГСК у больших
с ОМЛ, возникших из МДС. За последнее время не получено убедительных дам*
ных, свидетельствующих о необходимости проведения в этом
случае
индукци-
онного
курса химиотерапии с целью уменьшения опухолевой массы и достиже-
ния
ремиссии заболевания перед проведением алло-ТГСК. Назначение цитоста
тических препаратов не оправдано, в основном из-за отсутствия вероятности
достижения полной ремиссии, а также возможного развития токсических ос-
ложнений,
осложняющих проведение алло-ТГСК. Тем не менее известно, что
выполнение
алло-ТГСК при рецидиве ОМЛ имеет существенно худший прогноз
по
сравнению с трансплантацией в ремиссии заболевания, что в полной мере от-
носится
к осуществлению алло-ТГСК при МДС, трансформировавшемся в ОМЛ.
Классификация
МДС для взрослых (ФАБ, ВОЗ) не может быть однозначно
использована у детей и подростков. В детской возрастной группе редко наблю-
даются такие варианты МДС, как рефрактерная анемия и рефрактерная анемия
с кольцевыми сидеробластами. В то же время намного чаще встречаются моно-
сомия
7-й хромосомы (7q-CHHflpoM) и ювенильный хронический миеломоноци-
тарный лейкоз (в прошлом — ювенильная форма хронического миелолейкоза).
МДС
у детей в 10 % случаев имеет генетическую предрасположенность, напри-
мер развивается у больных с синдромом Дауна, анемией
Фанкони,
нейрофибро-
матозом, тяжелой формой врожденной нейтропении, либо является следствием
предшествующей цитостатической терапии по поводу
другого
злокачественного
новообразования.
По сравнению со взрослыми, МДС у детей чаще отражает со-
стояние
предлеикемическои стадии острого лейкоза и поэтому лучше реагирует
на
применение химиотерапии с восстановлением в последующем нормального
кроветворения.
При оценке результатов лечения у детей с МДС, достигших ре-
миссии,
применение алло-ТГСК позволило увеличить
5-летнюю
общую выжи-
ваемость до 80 %.
Общая выживаемость при МДС у детей, как и у взрослых, зависит от IPSS,
морфологического варианта МДС по классификации ВОЗ (ФАБ) и цитогенети-
ческих изменений. Все эти показатели, так же как тип трансплантации (родст-
венный,
неродственный донор), оказывают влияние на результаты после ал-
ло-ТГСК.
Например, 3-летняя безрецидивная выживаемость вне зависимости от
варианта МДС после родственной и неродственной алло-ТГСК у детей составила
56 и 59 % соответственно, но 4-летняя безрецидивная выживаемость после
неродственной алло-ТГСК при РА составила 35 %, при РАИБ — 35 %, при
РАИБ-Т
- 18 %.
Применение
ауто-ТГСК при МДС теоретически возможно, однако до настоя-
щего времени не получило широкого распространения ввиду невозможности
в
подавляющем большинстве случаев получения трансплантата ГСК адекватного
качества.

Несмотря
HI
определенные
успехи,
связанные с алло-ТГСК при
МДС, веро-
Ч'го
и
будущем
использование алло-ТГСК
у
данной категории больных
бу-
iMt'Tb более дифференцированный подход. Надежду
на это
дает
появление
1
чих
новых лекарственных препаратов, находящихся
в
стадии клинических
ис-
Ш.гганий,
как
талидомид, СС5013-ревимид, ингибиторы белка фарнезил-транс-
феразы, ингибиторы метилтрансферазы ДНК, ингибиторы фермента, вызываю-
щею деацетилирование гистона, гливек
и др.
Таким
образом,
в
настоящее время факторами, определяющими применение
1ЛЛ0-ТГСК
у
взрослых
с
МДС, являются возраст
и
общее состояние пациента,
т.пение
IPSS,
наличие/отсутствие донора ГСК. Постановка
же
диагноза
МДС
V детей
уже
является показанием
к
поиску аллогенного донора
ГСК в
кратчай-
шие сроки.
16.9.3.
Миелопролиферативные
заболевания
Хронический
миелолейкоз
До последнего времени постановка диагноза
ХМЛ
являлась абсолютным
по-
казанием
к
проведению алло-ТГСК. Таким образом, роль алло-ТГСК
при ХМЛ
у детей
и
взрослых оценена достаточно широко. Внедрение этого метода терапии
увеличило
5-летнюю
общую выживаемость
у
больных
с ХМЛ
после родственной
ллло-ТГСК
до 67 %,
5-летнюю
безрецидивную выживаемость
— до 55 %. Эти же
показатели после неродственной алло-ТГСК составили
52 и 40 %
соответственно.
На
отдаленные
результаты
после алло-ТГСК
у
больных
с ХМЛ
влияют
воз-
раст пациента, стадия заболевания,
а
также сроки проведения алло-ТГСК
с мо-
мента постановки диагноза
(до или
после
1
года).
По
данным CIBMTR, 3-летняя общая выживаемость больных
с ХМЛ в хро-
нической
стадии,
в
зависимости
от
сроков выполнения алло-ТГСК
и
источника
ГСК
(родственный, неродственный донор),
при
родственной алло-ТГСК, выпол-
ненной
в
течение
1
года
с
момента постановки диагноза, составила
69 %, а
после
2
лет — 57 %. Те же
показатели
при
алло-ТГСК
от
неродственного донора
рав-
нялись
54 % и 46 %
соответственно
(рис.
16.9).
5-летняя безрецидивная выживаемость
в
зависимости
от
стадии заболевания
при
выполнении родственной алло-ТГСК составляет:
в
хронической стадии
—
60-80
%; в
стадии акселерации
-
40-50
%; в
бластном кризе
- 10-20 %. При
неродственной алло-ТГСК получены следующие результаты: 5-летняя безреци-
дивная выживаемость
в
хронической стадии была равна
43 %, в
стадии акселе-
рации
— 18 %, а в
бластном кризе
— 7 %.
Вышеизложенные факты являются подтверждением возможности полного
излечения больных
с ХМЛ с
помощью проведения алло-ТГСК.
Несмотря
на
расхождения
в
результатах
при
проведении алло-ТГСК
от род-
ственного
и
неродственного донора
в
хронической стадии
ХМЛ, эти
различия
не
достигают статистически значимого уровня.
Их
характер
не
может повлиять
на
окончательное решение
о
целесообразности применения одного
из
видов
ал-
ло-ТГСК
при
данном заболевании.
Более существенным фактором, ограничивающим применение алло-ТГСК,
явилось внедрение альтернативных методов терапии
ХМЛ. В
настоящее время
ХМЛ
из
категории заболеваний
с
абсолютными показаниями
к
алло-ТГСК пере-

100
80
g 60
о
I
40
о.
M
20
HLA-совместимый
сибс,
< 1 г. (п =
2876)
HLA-совместимый
сибс, Й
1 Г. (л - 1391)
Неродственная ТГСК,
к 1 г. (я - 936)
Неродственная ТГСК,
< 1 г. (л
613)
р т
0,0001
0 12 3 4 5 6
Количество лет после трансплантации
Рис. 16.9, Общая выживаемость после аллогенной трансплантации гемопоэтических стволо »
клеток у больных с хронической стадией хронического миелолейкоза в зависимости от
ИСТОФ
ника
гемопоэтических
стволовых
клеток и длительности заболевания
(1994-1999)
шел в более сложную
группу
состояний для принятия решения по ее выполнг
нию.
Это связано с хорошими результатами консервативной терапии ХМЛ с ни
мощью ингибиторов тирозинкиназы — гливека, дазатиниба. Предварительные
результаты
лечения ХМЛ с помощью гливека
свидетельствуют
о высокой верп
ятности достижения и гематологической (у 95 % больных), и цитогенетической,
и
молекулярно-биологической (у 60 % больных) ремиссий. С
другой
стороны,
несмотря на
убедительные
данные об эффективности этих препаратов, оконча-
тельные выводы в отношении долгосрочного прогноза при лечении ХМЛ гливе-
ком
преждевременны из-за недостаточного срока наблюдения за пациентами.
Таким образом, при ХМЛ показана высокая эффективность
двух
альтерна-
тивных методов терапии — с помощью ингибиторов тирозинкиназы (гливека и
др.) и алло-ТГСК от родственного и неродственного донора. В момент постанов-
ки
диагноза ХМЛ выбор в пользу алло-ТГСК неоднозначен. Основным препят-
ствием является вероятность развития различных осложнений после алло-ТГСК
как
в ранние сроки после трансплантации, так и в отдаленный период. С целью
уменьшения риска их развития особое внимание
уделяется
применению при
ХМЛ алло-ТГСК с «немиелоаблативными» режимами кондиционирования.
Попытки
внедрения ауто-ТГСК как
метода
терапии ХМЛ до сих пор не полу-
чили широкого распространения. Это связано со сложностью в достижении при-
емлемой эрадикации злокачественного клона клеток из костного мозга с помо-
щью ранее известных протоколов терапии (гидроксимочевина, 1СЕ-протокол,
интерферон).
Полная ремиссия, в том числе молекулярно-биологическая,
у больных с ХМЛ может быть получена на фоне терапии гливеком. Это создает
условия для выделения аутологичных ГСК из нормального клона клеток, что,
в свою очередь, повысит интерес к применению ауто-ТГСК у данной категории
пациентов.
Таким образом, алло-ТГСК у взрослых с ХМЛ до настоящего времени оста-
ется одним из основных методов лечения. Определение суммы прогностических
параметров (Sokol, European индекс) позволяет принять решение о сроках про-
